Trichothecene
Trichothecenerna är en stor familj av kemiskt besläktade mykotoxiner . De produceras av olika arter av Fusarium , Myrothecium , Trichoderma / Podostroma , Trichothecium , Cephalosporium , Verticimonosporium och Stachybotrys . Kemiskt sett är trichothecener en klass av seskviterpener .
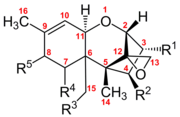
De avgörande strukturella egenskaperna som orsakar den biologiska aktiviteten hos trikotekener är 12,13-epoxiringen, närvaron av hydroxyl- eller acetylgrupper i lämpliga positioner på trikotecenkärnan och sidokedjans struktur och position. De produceras på många olika sädesslag såsom vete, havre eller majs av olika Fusarium -arter inklusive F. graminearum , F. sporotrichioides , F. poae och F. equiseti .
Vissa mögelsvampar som producerar trichothecene mykotoxiner, till exempel Stachybotrys chartarum , kan växa i fuktiga inomhusmiljöer. Det har visat sig att makrocykliska trichothecener producerade av S. chartarum kan bli luftburna och därmed bidra till hälsoproblem för byggnadsbrukare. En giftig svamp med ursprung i Japan och Kina , Podostroma cornu-damae , innehåller sex trichothecener, inklusive satratoxin H , roridin E och verrucarin.
Klassificering
Allmänna klassificeringen
Trichothecener är en grupp av över 150 kemiskt besläktade mykotoxiner . Varje trikotecen uppvisar en kärnstruktur som består av en enda sexledad ring som innehåller en enda syreatom, flankerad av två kolringar. Denna kärnringstruktur innehåller en epoxid , eller tricyklisk eter, vid 12,13 kolpositionerna, såväl som en dubbelbindning vid 9,10 kolpositionerna. Dessa två funktionella grupper är primärt ansvariga för trikotecens förmåga att hämma proteinsyntes och ådra sig generella cytotoxiska effekter. Noterbart är att denna kärnstruktur är amfipatisk och innehåller både polära och opolära delar. Alla trikotecener är besläktade genom denna gemensamma struktur, men varje trikotecen har också ett unikt substitutionsmönster av syreinnehållande funktionella grupper på möjliga platser på kolen 3,4,7,8 och 15. Dessa funktionella grupper styr egenskaperna hos en individuell trikotecen och tjänar också som grund för det vanligaste klassificeringssystemet för denna familj av toxiner. Detta klassificeringssystem delar upp trichothecene-familjen i fyra grupper: Typ A, B, C och D.
Typ A tricothecener har hydroxyl- , ester- eller inga funktionella gruppsubstitutioner runt kärnringens struktur. Vanliga exempel på dessa är Neosolaniol med en hydroxylsubstitution vid kol 8 och T-2-toxin med en estersubstitution vid kol 8.
Typ B-trikotecener klassificeras genom närvaron av karbonylfunktionella grupper substituerade runt kärnringstrukturen. Vanliga exempel på dessa inkluderar nivalenol och trichotecin, som båda har en funktionell ketongrupp vid kol 8.
Typ C trichothecener har en extra kol 7, kol 8 epoxidgrupp. Det vanliga exemplet på dessa är crotocin. som också har en esterfunktionell grupp vid kol 4.
Typ D trichothecener har en extra ring mellan kol 4 och kol 15. Dessa ringar kan ha olika ytterligare funktionella grupper. Vanliga exempel på dessa är roridin A och satratoxin H.
Även om de distinkta funktionella grupperna av dessa klassificeringstyper ger varje trichothecen unika kemiska egenskaper, indikerar deras klassificeringstyp inte explicit deras relativa toxicitet. Medan typ D trichothecener anses vara de mest giftiga, har typ A och B relativt blandad toxicitet.
Alternativa klassificeringar
Klassificeringssystemet som beskrivs ovan är det vanligaste som används för att gruppera molekyler från trichothecene-familjen. Emellertid finns en mängd alternativa klassificeringssystem också för dessa komplexa molekyler. Trichothecener kan också allmänt beskrivas som enkla eller makrocykliska. Enkla trikotecener inkluderar typ A, B och C, medan makrocykliska trikotecener inkluderar typ D och kännetecknas av närvaron av en kol 4 - kol 15 brygga. Dessutom föreslog JF Grove en klassificering av tricothecener i tre grupper som också var baserad på de funktionella substitutionsmönstren för ringskelettet. Grupp 1 tricothecener har endast funktionella grupper substituerade på den tredje, helt mättade kolringen. Grupp 2 tricothecener innehåller ytterligare funktionella grupper på kärnringen som innehåller dubbelbindningen med 9,10 kol. Slutligen innehåller grupp 3 trichothecenes en funktionell ketongrupp vid kol 8; detta är samma kriterier för typ B trichothecener.
Framsteg inom området evolutionär genetik har också lett till förslaget om trichothecen-klassificeringssystem baserade på vägen för deras biosyntes. Gener som är ansvariga för biosyntesen av ett mykotoxin är vanligtvis lokaliserade i kluster; i Fusariumi är dessa kända som TRI-gener. TRI-gener är var och en ansvariga för att producera ett enzym som utför ett specifikt steg i biosyntesen av trichothecener. Mutationer i dessa gener kan leda till produktion av varianter av trichothecenes och därför kan dessa molekyler grupperas på basis av delade biosyntessteg. Till exempel styrs ett delat steg i biosyntesen av trichothecener av genen TRI4 . Denna enzymprodukt styr tillsatsen av antingen tre eller fyra syre till trikodien för att bilda antingen isotrichodiol respektive isotrichotriol. En mängd olika trikotecener kan sedan syntetiseras från någon av dessa mellanprodukter och de skulle därför kunna klassificeras som antingen t-typ om de syntetiseras från isotrichotriol eller d-typ om de syntetiserades från isotrichodiol.
Handlingsmekanism
Toxiciteten hos tricothecener är främst resultatet av deras allmänt citerade verkan som proteinsyntesinhibitorer; denna hämning sker vid ribosomer under alla tre stadier av proteinsyntes: initiering, förlängning och avslutning. Under initiering kan trichothecener antingen hämma associationen av de två ribosomala subenheterna eller hämma funktionen hos den mogna ribosomen genom att förhindra associationen av det första tRNA :t med startkodonet. Hämning vid förlängning uppstår troligen på grund av att trikotecener förhindrar funktionen peptidyltransferas , enzymet som katalyserar bildningen av nya peptidbindningar på 60-talets ribosomala subenhet. Inhibering under avslutning kan också vara resultatet av peptidyltransferas-inhibering eller förmågan hos trichothecener att förhindra den hydrolys som krävs vid detta sista steg.
Det är intressant att notera att substitutionsmönstret för ringkärnan hos trichothecener påverkar toxinets verkan som antingen en inhibitor av initiering eller som en inhibitor av förlängning/terminering. Trichothecener har också förmågan att påverka den allmänna cellulära enzymfunktionen på grund av tiolgruppernas tendens att attackera 12,13-kolepoxidringen. Dessa hämmande effekter ses mest dramatiskt i aktivt prolifererande celler såsom i mag- tarmkanalen eller benmärgen .
Proteinsyntes sker både i cellens cytoplasma och i det luminala utrymmet i mitokondrierna , den cytoplasmatiska organellen som är ansvarig för att producera cellens energi. Detta görs genom en enzymatisk väg som genererar starkt oxiderade molekyler som kallas reaktiva syrearter , till exempel väteperoxid . Reaktiva syrearter kan reagera med och orsaka skada på många kritiska delar av cellen inklusive membran, proteiner och DNA . Trikotecen-hämning av proteinsyntesen i mitokondrierna gör att reaktiva syrearter kan byggas upp i cellen, vilket oundvikligen leder till oxidativ stress och induktion av den programmerade celldödsvägen, apoptos .
Induktionen av apoptos i celler med höga nivåer av reaktiva syrearter beror på en mängd olika cellsignaleringsvägar. Den första är p53- vägen som visas vara uppreglerad av T-2-toxinet. p53 är ett protein som ansvarar för att kontrollera cellcykeln, men en ökning av aktiviteten av detta protein leder också till ökad aktivering av BAX -proteiner i cellen. Dessa BAX-proteiner är primärt ansvariga för att öka permeabiliteten hos mitokondriella membranet och leda till frisättning av cytokrom c och reaktiva syrearter. Frisättning av cytokrom c från mitokondrierna inducerar apoptos genom att initiera sammansättningen av kaspaser , eller proteiner som ansvarar för att bryta ned cellen inifrån.
Dessutom har trichothecener som T-2 också visat sig öka signalvägen för c-Jun N-Terminal Kinase i celler. Här kan c-Jun N-Terminal Kinase öka till fosforylering av sitt mål, c-Jun, till sin aktiva form. Aktiverad c-jun fungerar som en transkriptionsfaktor i cellkärnan för proteiner som är viktiga för att underlätta den nedströms apoptotiska vägen.
Symptomologi
Trichothecene mykotoxiner är giftiga för människor, andra däggdjur, fåglar, fiskar, en mängd olika ryggradslösa djur, växter och eukaryota celler. Den specifika toxiciteten varierar beroende på det speciella toxinet och djurarten, men administreringsvägen spelar en betydligt större roll vid bestämning av dödlighet. Effekterna av förgiftning beror på exponeringskoncentrationen, hur lång tid och hur personen exponeras. En högkoncentrerad lösning eller stor mängd av toxinets gasform är mer sannolikt att orsaka allvarliga effekter, inklusive dödsfall. Vid konsumtion hämmar toxinet ribosomalt protein-, DNA- och RNA-syntes, mitokondriella funktioner celldelning samtidigt som det aktiverar en cellulär stressrespons som kallas ribotoxisk stressrespons.
Trichothecene mykotoxiner kan absorberas genom topikala , orala och inhalationsvägar och är mycket toxiska på subcellulär, cellulär och organisk systemnivå.
Trichothecener skiljer sig från de flesta andra potentiella vapengifter eftersom de kan verka genom huden, vilket tillskrivs deras amfipatiska och lipofila egenskaper. Den lilla amfipatiska naturen hos trichothecener gör att de enkelt kan korsa cellmembran och interagera med olika organeller såsom mitokondrierna, endoplasmatiskt retikulum (ER). och kloroplast Trichothecenernas lipofila karaktär gör att de lätt kan absorberas genom hudens lungslemhinna och tarmarna. Direkt dermal applicering eller oralt intag av trichothecene orsakar snabb irritation av huden eller tarmslemhinnan. Som hudirriterande och blåsbildningsmedel påstås det vara 400 gånger mer berusande än svavelsenap .
Responsen i kroppen på mykotoxinet, matsmältningsgiftig aleukia, inträffar flera dagar efter konsumtion, i fyra steg:
- Det första steget inkluderar inflammation i mag- och tarmslemhinnan .
- Det andra stadiet kännetecknas av leukopeni , granulopeni och progressiv lymfocytos .
- Det tredje steget kännetecknas av utseendet av ett rött utslag på kroppens hud, såväl som blödning i huden och slemhinnan. Om det är allvarligt afoni och död genom strypning inträffa.
- Vid det fjärde stadiet är cellerna i lymfoidorganen och erytropoesen i benmärgen och mjälten uttömda och immunsvaret är nere.
Infektion kan utlösas av en så liten skada som ett skärsår, repa eller skavsår.
Följande symtom visas:
- Svår klåda och rodnad i huden, sår, utsöndring av huden
- Förvrängning av något av sinnena, förlust av förmågan att koordinera muskelrörelser
- Illamående, kräkningar och diarré
- Smärta i näsa och hals, flytningar från näsan, klåda och nysningar
- Hosta, andningssvårigheter, väsande andning, bröstsmärtor och spottande blod
- Tillfälliga blödningsrubbningar
- Förhöjd kroppstemperatur
Regleringsfrågor
När det gäller djur- och människoföda är typ A trichothecener (t.ex. T-2-toxin , HT-2-toxin, diacetoxyscirpenol ) av speciellt intresse eftersom de är mer toxiska än de andra livsmedelsburna trichothecenerna dvs typ B-grupp (t.ex. deoxynivalenol , nivalenol , 3- och 15-acetyldeoxinivalenol). Deoxynivalenol är dock oroande eftersom det är den vanligaste trichothecenen i Europa. De viktigaste effekterna av trichothecener – relaterade till deras koncentration i varan – är minskat foderupptag, kräkningar och immunsuppression. Ett relativt fåtal länder, främst inom EU , har rekommenderat maxgränser för dessa mykotoxiner i livsmedel och djurfoder. Trichothecener testas dock ofta på andra ställen för att förhindra att de kommer in i näringskedjan och för att förhindra förluster i animalieproduktionen.
Historia
Trichothecenes tros ha upptäckts 1932 i Orenburg, Ryssland, under andra världskriget , av Sovjetunionen. Omkring 100 000 människor (60 % dödlighet) började lida och dö av toxisk aleukia , en dödlig sjukdom med symptom som liknar strålning. Man tror att de sovjetiska civila hade blivit sjuka av att få i sig förorenat bröd och andas in mögel genom förorenat hö, damm och ventilationssystem. Boven tros vara toxinerna Fusarium sporotrichioides och Fusarium poae som är höga producenter av T-2-toxin . Fusarium- arter är förmodligen de vanligast citerade och bland de mest förekommande av de trichothecene-producerande svamparna.
Trichothecener är en idealisk biologisk krigföringsmedel, är dödlig och billig att producera i stora mängder, stabil som en aerosol för spridning och utan effektiv vaccination/behandling. Bevis tyder på att mykotoxiner redan har använts som biologisk krigföring.
- 1964 finns det obekräftade rapporter om att egyptiska eller ryska styrkor använde T-2 med senapsgas
- 1974-1981 incidenter med " gult regn " i Sydostasien (Laos, Kambodja) och Afghanistan
- 1975 och 1981 under Vietnamkriget påstods Sovjetunionen ha tillhandahållit mykotoxiner till Vietnams och Laos arméer för användning mot motståndsstyrkor i Laos och Kambodja
- 1985-1989 Iran-Irakkriget, rapporter om mykotoxintransporter till Irak (i form av pulver och rök)
Sedan dess har trichothecener rapporterats över hela världen. De har haft en betydande ekonomisk inverkan på världen på grund av orsaker som: förlust av människo- och djurliv, ökade kostnader för sjukvård och veterinärvård, minskad boskapsproduktion, bortskaffande av förorenade livsmedel och foder samt investeringar i forskning och tillämpningar för minska svårighetsgraden av mykotoxinproblemet. Dessa mykotoxiner står för miljontals dollar årligen i förluster, på grund av faktorer som ofta ligger utanför mänsklig kontroll (miljömässig, ekologisk eller lagringsmetod).
Matförorening
Farliga koncentrationer av trichothecener har upptäckts i majs, vete, korn, havre, ris, råg, grönsaker och andra grödor. Sjukdomar som härrör från infektion inkluderar fröröta, fröröta, rotröta , stjälkröta och öronröta. Trichothecener är också vanliga föroreningar i fjäderfäfoder och deras negativa effekter på fjäderfäns hälsa och produktivitet har studerats omfattande.
Flera studier har visat att optimala förutsättningar för svamptillväxt inte nödvändigtvis är optimala för toxinproduktion. Toxinproduktionen är störst med hög luftfuktighet och temperaturer på 6-24 °C. Svampförökningen och produktionen förbättras under tropiska förhållanden med höga temperaturer och fuktnivåer; monsuner , snabba översvämningar och otidsenligt regn under skörden. Trichothecener har upptäckts i luftprover som tyder på att de kan aerosoliseras på sporer eller små partiklar
Naturlig förekomst av TCT har rapporterats i Asien , Afrika , Sydamerika , Europa och Nordamerika
- Akakabibyo, en sjukdom med liknande etiologi, har också associerats med trichothecen-förorenade spannmål i Japan.
- I Kina har spannmål eller deras produkter kontaminerade med trichothecener inklusive DON, T-2-toxin och NIV också associerats med utbrott av gastrointestinala störningar.
- I Jugoslavien har studier av mykotoxigena svampar i obehandlad mjölk visat att 91 % av de testade proverna var kontaminerade
- I USA genomfördes en studie i sju delstater i Mellanvästern 1988–1989 och fann mykotoxiner i 19,5 %-24,7 % av majsproverna. Sedan början av 1900-talet, förekomster [ stavning? ] av kräkningar hos djur och människor efter konsumtion av spannmål infekterade med Fusarium-arter har beskrivits.
- I en studie i Bihar-regionen från 1985 till 1987 var 51 % av de testade proverna kontaminerade med mögel.
- I en annan studie I Bihar-regionen rapporterades höga halter av jordnötsmjöl som används för mjölkboskap.
- I Ludhiana och Punjab fann forskare att 75 % av proverna från mjölkgårdar var kontaminerade.
- I Indien gick uppskattningsvis 10 miljoner dollar förlorade på grund av jordnötskontamination med mykotoxiner.
Säkerhet
Det finns inga kända direkta motgifter mot trichothecenexponering. Därför definieras riskhantering i förorenade områden i första hand av behandling av exponeringssymtom samt förebyggande av framtida exponering.
Behandling
Typiska exponeringsvägar för trichothecen-toxiner inkluderar topisk absorption, intag och inandning. Symtomens svårighetsgrad beror på dos och typ av exponering, men behandlingen är främst inriktad på att stödja kroppssystem som skadats av mykotoxinet. Det första steget i de flesta exponeringsfall är att ta bort potentiellt förorenade kläder och att spola exponeringsställena noggrant med vatten. Detta förhindrar offret från upprepad exponering. Vätskor och elektrolyter kan ges till offer med höga nivåer av gastrointestinala skador för att mildra effekterna av minskad absorption i tarmkanalen. Frisk luft och assisterad andning kan också administreras vid utveckling av lätt andningsbesvär. Allt svårare symtom kan kräva tillämpning av avancerad medicinsk hjälp. Uppkomsten av leukopeni , eller minskning av antalet vita blodkroppar, kan behandlas med plasma- eller blodplättstransfusion . Hypotension kan behandlas med administrering av noradrenalin eller dopamin . Utveckling av allvarliga hjärt- och lungbesvär kan kräva intubation och ytterligare läkemedelsbehandlingar för att stabilisera hjärt- och lungaktiviteten.
Dessutom finns det en mängd olika kemikalier som indirekt kan minska de skadliga effekterna av trichothecener på celler och vävnader. Lösningar med aktivt kol administreras ofta till intagsfall som adsorbent . Här fungerar kolet som ett poröst ämne för giftet att binda, förhindrar dess absorption genom mag-tarmkanalen och ökar dess avlägsnande från kroppen genom tarmutsöndring. Liknande avgiftande adsorbenter kan också tillsättas till djurfoder vid kontaminering för att minska biotillgängligheten av toxinet vid konsumtion. Antioxidanter är också användbara för att mildra de skadliga effekterna av trichothecener som svar på ökningen av reaktiva syrearter som de producerar i celler. Generellt sett anses en bra kost rik på probiotika, vitaminer och näringsämnen, proteiner och lipider vara effektiv för att minska symptomen på trikotecenförgiftning. Till exempel vitamin E motverka bildningen av lipidperoxider inducerade av T-2-toxin hos kycklingar. På liknande sätt minskade tillägg av modifierade glukomannaner och selen i kosten för kycklingar som också konsumerade T-2-toxin de skadliga effekterna av toxinassocierad utarmning av antioxidanter i levern. Trots att de inte är ett direkt motgift kan dessa antioxidanter vara avgörande för att minska svårighetsgraden av trichothecenexponeringar.
Förebyggande
Trichothecener är mykotoxiner som produceras av mögelsvampar som ofta förorenar förråd av spannmålsprodukter. Detta gör trichothecenkontamination till ett betydande folkhälsoproblem, och många områden har strikta gränser för tillåtet trichotheceninnehåll. Till exempel, i Europeiska unionen är endast 0,025 ppm T-2-toxin tillåtet i bageriprodukter avsedda att användas som livsmedel. Mögelsvamparna som kan producera trichothecener växer bra på mörka, tempererade platser med hög fukthalt. Därför är ett av de bästa sätten att förhindra trichothecenkontamination i livsmedelsprodukter att lagra resurserna under lämpliga förhållanden för att förhindra tillväxt av mögel. Till exempel rekommenderas det generellt att endast lagra spannmål i områden med en fukthalt på mindre än 15 %. Men om ett område redan har kontaminerats med trichothecene toxiner, finns det en mängd olika möjliga dekontamineringsstrategier för att förhindra ytterligare exponering. Behandling med 1 % natriumhypoklorit (NaOCl) i 0,1 M natriumhydroxid (NaOH) under 4–5 timmar har visat sig hämma den biologiska aktiviteten av T-2-toxin. Inkubation med vattenhaltigt ozon vid cirka 25 ppm har också visat sig bryta ned en mängd olika trichothecener genom en mekanism som involverar oxidation av dubbelbindningen med 9,10 kol. UV- exponering har också visat sig vara effektiv under rätt förhållanden.
Utöver strategierna för fysisk och kemisk sanering har framskridande forskning inom molekylär genetik också gett upphov till potentialen för en biologisk saneringsmetod. Många mikrober, inklusive bakterier, jäst och svampar, har utvecklat enzymatiska genprodukter som underlättar den specifika och effektiva nedbrytningen av trichothecene mykotoxiner. Många av dessa enzymer bryter specifikt ned 12,13-kolepoxidringen som är viktig för toxiciteten hos trichothecener. Till exempel producerar Eubacteria-stammen BBSH 797 de-epoxidasenzymer som reducerar 12,13-kolepoxidringen till en dubbelbindningsgrupp. Dessa, tillsammans med andra mikrober som uttrycker trichothecene avgiftande egenskaper, kan användas i foderbutiker för att förhindra toxisk effekt av kontaminerat foder vid konsumtion. Vidare molekylär kloning av generna som är ansvariga för att producera dessa avgiftande enzymer vara användbar för att producera stammar av jordbruksprodukter som är resistenta mot trikotecenförgiftning.
Epoxitrichothecener
Epoxitrichothecener är en variant av ovanstående och undersöktes en gång för militär användning i Östtyskland, och möjligen hela sovjetblocket. Det finns ingen genomförbar behandling när symtom på epoxitikotecenförgiftning väl har kommit, även om effekterna kan avta utan att lämna några permanenta skador.
Planerna för användning som ett storskaligt biovapen lades ner, eftersom de relevanta epoxitrichothecenerna bryts ned mycket snabbt under UV-ljus och värme, såväl som klorexponering, vilket gör dem oanvändbara för öppna attacker och förgiftning av vattenförsörjning. [ citat behövs ]
externa länkar
- Strukturer av några av de vanligaste trichothecene mykotoxiner.
- Robert W. Wannemacher och Stanley L. Weiner: Trichothecene mycotoxins, kapitel 34, Medical Aspects of Chemical and Biological Warfare Archived 2018-04-18 at the Wayback Machine



