Pikrotoxin
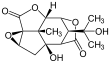
Picrotoxinin (vänster) och picrotin (höger)
| |||
| Kliniska data | |||
|---|---|---|---|
| ATC-kod |
|
||
| Identifierare | |||
| CAS-nummer | |||
| PubChem CID | |||
| IUPHAR/BPS | |||
| DrugBank | |||
| ChemSpider | |||
| UNII | |||
| KEGG | |||
| ChEBI | |||
| ChEMBL | |||
| CompTox Dashboard ( EPA ) | |||
| ECHA InfoCard | 100.004.288 | ||
| Kemiska och fysikaliska data | |||
| 3D-modell ( JSmol ) | |||
| |||
| |||
|
| |||
Picrotoxin , även känd som cocculin , är en giftig kristallin växtförening. Det isolerades först av den franske apotekaren och kemisten Pierre François Guillaume Boullay (1777–1869) 1812. Namnet "picrotoxin" är en kombination av de grekiska orden "picros" (bitter) och "toxicon" (gift). En blandning av två olika föreningar, pikrotoxin förekommer naturligt i frukten av Anamirta cocculus- växten, även om det också kan syntetiseras kemiskt.
På grund av dess interaktioner med den hämmande signalsubstansen GABA, fungerar pikrotoxin som ett stimulerande och krampaktigt medel. Det påverkar främst det centrala nervsystemet och orsakar kramper och andningsförlamningar i tillräckligt höga doser.
Kemisk struktur och syntes
Pikrotoxin är en ekvimolär blandning av två föreningar , pikrotoxinin (C15H16O6 ; CAS # 17617-45-7 ) och picrotin (C15H18O7; CAS # 21416-53-5 ) . Av de två föreningarna är pikrotin mindre aktivt.
Pikrotoxin förekommer naturligt i frukten av Anamirta cocculus , en klätterväxt från Indien och andra delar av Sydostasien. Växten är känd för sina stora stjälkar av vitt trä och sött doftande blommor. Den producerar små stenfrukter, Cocculus indicus , som vanligtvis torkas. [ citat behövs ]
För närvarande finns det så många som fem totala synteser av pikrotoxinin - varav en publicerades så sent som i juni 2020 av Shenvi-labbet på Scripps. Denna syntes, som de flesta för denna molekyl, involverade användningen av karvon som en stereokemisk mall. Strategin använde den snabba bildningen av den polycykliska kärnan, följt av manipulation av oxidationstillstånd för nyckelkolatomer för att producera målmolekylen. Viss forskning tyder på att det kan göras genom cyklofunktionalisering av cykloalkenylsystem. Under kinetiskt kontrollerade förhållanden resulterar denna process i allmänhet i exo- cyklisering och bildar överbryggade ringsystem som de som finns i pikrotoxin. Dessutom har flera synteser föreslagits för pikrotoxin och pikrotin, de två molekylerna som utgör pikrotoxin. 1980 upptäcktes en process för att omvandla pikrotoxinin till pikrotin. Denna syntes börjar med att behandla pikrotoxin med trifluorättiksyraanhydrid i pyridin för att separera komponenterna.
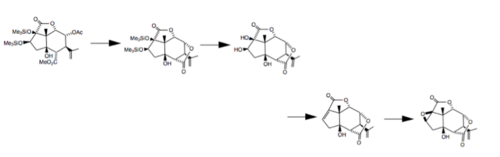
1988 fullbordade forskare från Tohoku University i Japan en total stereoselektiv syntes av både (-)-pikrotoxinin och (-)-pikrotin som började med (+)-5β- hydroxikarvon . I denna syntes framställdes åtta asymmetriska centra stereoselektivt på ett cis-fuserat hydrindanringsystem med användning av flera olika reaktioner: en Claisen-omläggning för att introducera det kvartära centret, en organoselen-medierad reduktion av en epoxiketon och en stereospecifik konstruktion av en glycidester . De sista stegen i denna process visas nedan.
Pikrotoxin har också använts som utgångsmaterial i flera syntetiska processer, inklusive skapandet av dl -pikrotoxadien, som bibehåller vissa egenskaper hos pikrotoxinskelettet.
Handlingsmekanism
Vissa kräftdjurs muskelfibrer har excitatorisk och hämmande innervation. Pikrotoxin blockerar hämning. Två olika men relaterade teorier har föreslagits för mekanismen genom vilken pikrotoxin verkar på synapser . En teori är att den fungerar som en icke-konkurrerande kanalblockerare för GABAA - receptorkloridkanaler , särskilt den gamma-aminosmörsyraaktiverade kloridjonoforen. En studie från 2006 fann att, även om den inte strukturellt liknar GABA, förhindrar pikrotoxin jonflöde genom kloridkanalerna som aktiveras av GABA. Det verkar troligen inom jonkanalerna själva, snarare än på GABA-igenkänningsplatser. Eftersom det hämmar kanaler som aktiveras av GABA, kan GABA-förstärkande läkemedel som barbiturater och bensodiazepiner användas som motgift.
Annan forskning tyder på att toxinet istället fungerar som en icke-konkurrensantagonist , eller hämmare, för GABA-receptorer. En studie av Newland och Cull-Candy fann att, i tillräckligt höga koncentrationer, minskade pikrotoxin amplituden av GABA-strömmar. Deras data visade att det var osannolikt att pikrotoxin helt enkelt fungerade som en spänningsstyrd kanalblockerare, även om det minskade frekvensen av kanalöppningar. Snarare fann de att pikrotoxin "binder företrädesvis till en agonistbunden form av receptorn." Detta innebär att, även i närvaro av låga koncentrationer av pikrotoxin, reduceras svaret från neuroner på GABA.
Giftighet
Pikrotoxin fungerar som ett centralt nervsystem och andningsstimulerande medel. Det är extremt giftigt för fiskar och människor, såväl som gnagare och andra däggdjur. Enligt registret över toxiska effekter av kemiska ämnen är LDLo, eller lägsta rapporterade dödliga dos, 0,357 mg/kg. Symtom på pikrotoxinförgiftning inkluderar hosta, andningssvårigheter, huvudvärk, yrsel, förvirring, mag-tarmbesvär, illamående eller kräkningar och förändringar i hjärtfrekvens och blodtryck. Även om det är särskilt farligt vid förtäring kan systemiska effekter också uppstå från inandning eller absorption i blodomloppet genom lesioner i huden. Pikrotoxin fungerar också som ett konvulsivt medel. I större doser har det visat sig inducera kloniska anfall eller hjärtrytmrubbningar, med särskilt höga doser som slutligen visar sig vara dödliga, vanligtvis på grund av andningsförlamning.
Kliniska tillämpningar och andra användningsområden
På grund av dess toxicitet är pikrotoxin nu vanligast som ett forskningsverktyg. På grund av dess antagonistiska effekt på GABA-receptorer har den emellertid använts som ett stimulerande medel i centrala nervsystemet. Det har också tidigare använts som ett motgift mot förgiftning av CNS-depressiva medel, särskilt barbiturater .
Även om det inte används ofta, är pikrotoxin effektivt som både bekämpningsmedel och pedikulicid . På 1800-talet användes det vid framställning av hård multum, som tillsattes öl för att göra det mer berusande. Denna beredning har sedan dess förbjudits.
Trots dess potentiella toxicitet för däggdjur i tillräckligt stora doser, används pikrotoxin också ibland som en prestationshöjare hos hästar. Det klassificeras som ett olagligt "klass I-ämne" av American Quarter Horse Association . Ämnen som klassificeras som "Klass I" påverkar sannolikt prestationsförmågan och har ingen terapeutisk användning inom hästmedicin. 2010 stängdes quarter horse-tränaren Robert Dimitt av efter att hans häst, Stoli Signature, testats positivt för ämnet. Precis som för människor används det för att motverka barbituratförgiftning.
Se även
Vidare läsning
- Ehrenberger K, Benkoe E, Felix D (1982). "Undertryckande verkan av pikrotoxin, en GABA-antagonist, på labyrintisk spontan nystagmus och svindel hos människan". Acta Oto-Laryngologica . 93 (1–6): 269–73. doi : 10.3109/00016488209130882 . PMID 7064710 .
- Dupont L, Dideberg O, Lamotte-Brasseur J, Angenot L (1976). et moléculaire de la picrotoxine , C15H16O6 · C15H18O7 " . " Structure cristalline Acta Crystallographica B (på franska). 32 (11): 2987–2993. doi : 10.1107/S0567740876009424 .
- Olsen RW, DeLorey TM (1999). "GABA-receptorfysiologi och farmakologi" . I Siegel GJ, Agranoff BW, Albers RW, et al. (red.). Grundläggande neurokemi: molekylära, cellulära och medicinska aspekter (6:e upplagan). Philadelphia, PA, USA: Lippincott-Raven.