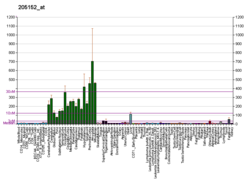
GABA transportör typ 1
| SLC6A1- | |||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| identifierare | |||||||||||||||||||||||||||||||||||||||||||||||
| , GABATHG, GABATR, GAT1, MAE, GABA-transportör 1, bärarfamilj för lösta ämnen 6 medlem 1 | |||||||||||||||||||||||||||||||||||||||||||||||
| Externa ID:n | |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
| Wikidata | |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
GABA-transportör 1 ( GAT1 ) även känd som natrium- och kloridberoende GABA-transportör 1 är ett protein som hos människor kodas av SLC6A1 -genen och tillhör familjen lösta bärare 6 (SLC6) av transportörer. Det förmedlar gamma-aminosmörsyras translokation från de extracellulära till intracellulära utrymmena i hjärnvävnaden och det centrala nervsystemet som helhet.
Strukturera
GAT1 är ett protein på 599 aminosyror som består av 12 transmembrandomäner med en intracellulär N-terminal och C-terminal .
Fungera
GAT1 är en transportör för gamma-aminosmörsyra (GABA), som tar bort GABA från den synaptiska klyftan genom att transportera den till presynaptiska neuroner (där GABA kan återvinnas) och astrocyter (där GABA kan brytas ned). GABA Transporter 1 använder energi från spridningen av en Na + -gradient, med hjälp av närvaron av en Cl - gradient, för att translokera GABA över CNS-neuronala membran. Stökiometrin för GABA Transporter 1 är 2 Na + : 1 Cl − : 1 GABA. Närvaron av ett Cl − /Cl − utbyte föreslås också eftersom Cl − som transporteras över membranet inte påverkar nettoladdningen. GABA är också den primära hämmande signalsubstansen i hjärnbarken och har den högsta nivån av uttryck inom sig. GABA-affiniteten ( Km ) för musisoformen av GAT1 är 8 μM.
I hjärnan hos ett moget däggdjur omvandlas glutamat till GABA av enzymet glutamatdekarboxylas (GAD) tillsammans med tillsats av vitamin B6. GABA packas sedan och frisätts i de postsynaptiska terminalerna av neuroner efter syntes. GABA kan också användas för att bilda succinat, som är involverat i citronsyracykeln . Vesikelupptag har visat sig prioritera nysyntetiserad GABA framför förformad GABA, även om resonemanget bakom denna mekanism för närvarande inte är helt förstått.
Regleringen av GATs modulära funktion är starkt beroende av en mängd andra budbärare och synaptiska proteiner.
Translokationscykel
Under hela translokationscykeln antar GAT1 tre olika konformationer:
- Öppen till ut. I denna konformation samtransporteras 2 extracellulära Na + -joner in i neuronen tillsammans med 1 GABA och 1 Cl - som binder till den tomma transportören, vilket gör den fulladdad. Hos prokaryoter har man funnit att transport inte kräver Cl − . Hos däggdjur krävs Cl - jonen för att kompensera den positiva laddningen av Na + för att upprätthålla den rätta membranpotentialen.
- Utestängd. När den väl är fulladdad förhindrar denna konformation frisättning av joner/substrat till cytoplasman eller det extracellulära utrymmet/synapsen. Na + , Cl − och GABA är bundna till transportören tills den ändrar konformation.
- Öppen för in. Transportören, som tidigare var vänd mot synapsen, blir inåtvänd och kan nu släppa ut jonerna och GABA i neurons cytoplasma. När transportören är tom täpper den till sitt bindningsställe och vänder så att den blir utåtvänd så att en ny translokationscykel kan börja.
Klinisk signifikans
Forskning har visat att schizofrenipatienter har förändrats GABA-syntes och uttryck, vilket leder till slutsatsen att GABA Transporter-1, som lägger till och tar bort GABA från synaptisk klyfta, spelar en roll i utvecklingen av neurologiska störningar som schizofreni . GABA och dess prekursor glutamat har motsatta funktioner i nervsystemet. Glutamat anses vara en excitatorisk signalsubstans, medan GABA är en hämmande signalsubstans. Glutamat- och GABA-obalanser bidrar till olika neurologiska patologier.
Obalans i den GABAergiska neurotransmissionen är involverad i patofysiologin för olika neurologiska sjukdomar som epilepsi, Alzheimers och stroke.
En studie på råttor med genetisk frånvaro av epilepsi från Strasbourg ( GAERS ) fann att dåligt GABA-upptag av GAT1 orsakade en ökning av tonisk ström av GABA A. I de två mest kända formerna av frånvaroepilepsi spelar synaptiska GABAA- receptorer inklusive GAT1 en viktig roll i utvecklingen av anfall. Blockering av GAT1 hos råttor med icke-epileptisk kontroll (NEC) fick tonisk ström att öka till en hastighet som liknar den för GAERS i samma ålder. Denna vanliga cellulära kontrollplats visar ett möjligt mål för framtida anfallsbehandlingar.
Glutamat och GABA har också visat sig interagera inom nucleus tractus solitarii (NTS), paraventricular nucleus (PVN) och rostral ventrolateral medulla (RVLM) i hjärnan för att modulera blodtrycket.
Interaktioner
SLC6A1 har visats interagera med STX1A .
Se även
Vidare läsning
- Nelson H, Mandiyan S, Nelson N (augusti 1990). "Klonning av den mänskliga hjärnans GABA-transportör" . FEBS Bokstäver . 269 (1): 181–184. doi : 10.1016/0014-5793(90)81149-I . PMID 2387399 . S2CID 34636220 .
- Bennett ER, Kanner BI (januari 1997). "Membrantopologin för GAT-1, en (Na+ + Cl-)-kopplad gamma-aminosmörsyratransportör från råtthjärna" . Journal of Biological Chemistry . 272 (2): 1203–1210. doi : 10.1074/jbc.272.2.1203 . PMID 8995422 .
- Bismuth Y, Kavanaugh MP, Kanner BI (juni 1997). "Tyrosin 140 av gamma-aminosmörsyratransportören GAT-1 spelar en avgörande roll vid igenkänning av signalsubstanser" . Journal of Biological Chemistry . 272 (26): 16096–16102. doi : 10.1074/jbc.272.26.16096 . PMID 9195904 .
- DeFelipe J, González-Albo MC (februari 1998). "Ljuskronans cellaxoner är immunreaktiva för GAT-1 i den mänskliga neocortexen". NeuroReport . 9 (3): 467–470. doi : 10.1097/00001756-199802160-00020 . PMID 9512391 . S2CID 27446580 .
- Conti F, Melone M, De Biasi S, Minelli A, Brecha NC, Ducati A (juni 1998). "Neuronal och glial lokalisering av GAT-1, en högaffinitet gamma-aminosmörsyra plasmamembrantransportör, i mänsklig hjärnbark: med en anteckning om dess distribution i apa cortex". Journal of Comparative Neurology . 396 (1): 51–63. doi : 10.1002/(SICI)1096-9861(19980622)396:1<51::AID-CNE5>3.0.CO;2-H . PMID 9623887 . S2CID 33438310 .
- Augood SJ, Waldvogel HJ, Münkle MC, Faull RL, Emson PC (januari 1999). "Lokalisering av kalciumbindande proteiner och GABA-transportör (GAT-1) budbärar-RNA i den mänskliga subthalamuskärnan". Neurovetenskap . 88 (2): 521–534. doi : 10.1016/S0306-4522(98)00226-7 . PMID 10197772 . S2CID 2514970 .
- Ong WY, Yeo TT, Balcar VJ, Garey LJ (oktober 1998). "En ljus- och elektronmikroskopisk studie av GAT-1-positiva celler i hjärnbarken hos människa och apa". Journal of Neurocytology . 27 (10): 719–730. doi : 10.1023/A:1006946717065 . PMID 10640187 . S2CID 39552099 .
- Whitworth TL, Quick MW (november 2001). "Substratinducerad reglering av handel med gamma-aminosmörsyratransportörer kräver tyrosinfosforylering" . Journal of Biological Chemistry . 276 (46): 42932–42937. doi : 10.1074/jbc.M107638200 . PMID 11555659 .
- Hachiya Y, Takashima S (november 2001). "Utveckling av GABAergiska neuroner och deras transportör i mänsklig temporal cortex". Pediatrisk neurologi . 25 (5): 390–396. doi : 10.1016/S0887-8994(01)00348-4 . PMID 11744314 .
- Kanner BI (februari 2003). "Transmembrandomän I av gamma-aminosmörsyratransportören GAT-1 spelar en avgörande roll i övergången mellan katjonläckage och transportsätt. " Journal of Biological Chemistry . 278 (6): 3705–3712. doi : 10.1074/jbc.M210525200 . PMID 12446715 .
- Zomot E, Kanner BI (oktober 2003). "Interaktionen mellan gamma-aminosmörsyratransportören GAT-1 och neurotransmittorn försämras selektivt av sulfhydrylmodifiering av en konformationskänslig cysteinrest som konstruerats i extracellulär loop IV" . Journal of Biological Chemistry . 278 (44): 42950–42958. doi : 10.1074/jbc.M209307200 . PMID 12925537 .
- Zhou Y, Bennett ER, Kanner BI (april 2004). "Den vattenhaltiga tillgängligheten i den externa halvan av transmembrandomän I av GABA-transportören GAT-1 moduleras av dess ligander" . Journal of Biological Chemistry . 279 (14): 13800–13808. doi : 10.1074/jbc.M311579200 . PMID 14744863 .
- Hu JH, Ma YH, Jiang J, Yang N, Duan SH, Jiang ZH, et al. (januari 2004). "Kognitiv försämring hos möss som överuttrycker gamma-aminosmörsyratransportör 1 (GAT1)". NeuroReport . 15 (1): 9–12. doi : 10.1097/00001756-200401190-00003 . PMID 15106822 . S2CID 6407617 .
- Korkhov VM, Farhan H, Freissmuth M, Sitte HH (december 2004). "Oligomerisering av {gamma}-aminosmörsyratransportören-1 drivs av ett samspel av polära och hydrofoba interaktioner i transmembranhelix II" . Journal of Biological Chemistry . 279 (53): 55728–55736. doi : 10.1074/jbc.M409449200 . PMID 15496410 .
Denna artikel innehåller text från United States National Library of Medicine, som är allmän egendom .