Alkaloid

Alkaloider är en klass av basiska , naturligt förekommande organiska föreningar som innehåller minst en kväveatom . Denna grupp inkluderar också några besläktade föreningar med neutrala och till och med svagt sura egenskaper. Vissa syntetiska föreningar med liknande struktur kan också kallas alkaloider. Förutom kol , väte och kväve kan alkaloider också innehålla syre , svavel och, mer sällan, andra ämnen som klor , brom och fosfor .
Alkaloider produceras av en mängd olika organismer inklusive bakterier , svampar , växter och djur . De kan renas från råextrakt av dessa organismer genom syra-basextraktion eller lösningsmedelsextraktioner följt av silikagelkolonnkromatografi . Alkaloider har ett brett spektrum av farmakologiska aktiviteter inklusive antimalaria ( t.ex. kinin ), antiastma ( t.ex. efedrin ), anticancer ( t.ex. homoharringtonin ), kolinomimetikum ( t.ex. galantamin ), kärlvidgande ( t.ex. vincamin ), antiarytmika ( t.ex. kinidin, t.ex. ) , smärtstillande ( t.ex. ) , antibakteriella ( t.ex. chelerytrin ) och antihyperglykemiska aktiviteter ( t.ex. piperin ). [ misslyckad verifiering ] Många har funnit användning i traditionell eller modern medicin , eller som utgångspunkt för upptäckt av läkemedel . Andra alkaloider har psykotropa ( t.ex. psilocin ) och stimulerande aktiviteter ( t.ex. kokain , koffein , nikotin , teobromin ) och har använts i enteogena ritualer eller som rekreationsdroger . Alkaloider kan också vara giftiga ( t.ex. atropin , tubokurarin ). Även om alkaloider verkar på en mångfald av metaboliska system hos människor och andra djur, framkallar de nästan jämnt en bitter smak .
Gränsen mellan alkaloider och andra kvävehaltiga naturliga föreningar är inte tydlig. Föreningar som aminosyrapeptider , proteiner , nukleotider , nukleinsyra , aminer och antibiotika kallas vanligtvis inte alkaloider . Naturliga föreningar som innehåller kväve i den exocykliska positionen ( meskalin , serotonin , dopamin , etc.) klassificeras vanligtvis som aminer snarare än som alkaloider. Vissa författare anser dock att alkaloider är ett specialfall av aminer.
Namngivning
Namnet "alkaloider" (tyska: Alkaloide ) introducerades 1819 av den tyske kemisten Carl Friedrich Wilhelm Meißner , och kommer från sen latinsk rot alkali och det grekiskspråkiga suffixet -οειδής -('lika'). Begreppet kom dock till stor användning först efter publiceringen av en översiktsartikel av Oscar Jacobsen i Albert Ladenburgs kemiska ordbok på 1880-talet.
Det finns ingen unik metod för att namnge alkaloider. Många individuella namn bildas genom att lägga till suffixet "ine" till art- eller släktnamnet. Till exempel isoleras atropin från växten Atropa belladonna ; stryknin erhålls från fröet från strykninträdet ( Strychnos nux-vomica L.). När flera alkaloider extraheras från en växt kännetecknas deras namn ofta av variationer i suffixet: "idin", "anin", "aline", "inine" etc. Det finns också minst 86 alkaloider vars namn innehåller roten "vin". " eftersom de utvinns från vincaväxter som Vinca rosea ( Catharanthus roseus ) ; dessa kallas vinca- alkaloider .
Historia

Alkaloidhaltiga växter har använts av människor sedan urminnes tider för terapeutiska och rekreationsändamål. Till exempel har medicinalväxter varit kända i Mesopotamien från omkring 2000 f.Kr. The Odyssey of Homer hänvisade till en gåva som gavs till Helen av den egyptiska drottningen, en drog som för med sig glömska. Man tror att gåvan var ett läkemedel som innehåller opium. En kinesisk bok om krukväxter skriven under 1:a–3:e århundradena f.Kr. nämnde en medicinsk användning av efedra och opiumvallmo . Dessutom kokablad använts av inhemska sydamerikaner sedan urminnes tider.
Extrakt från växter som innehåller giftiga alkaloider, såsom akonitin och tubokurarin , har använts sedan antiken för att förgifta pilar.
Studier av alkaloider började på 1800-talet. År 1804 isolerade den tyske kemisten Friedrich Sertürner från opium en "soporisk princip" (latin: principium somniferum ), som han kallade "morphium", med hänvisning till Morpheus , den grekiska drömguden; på tyska och några andra centraleuropeiska språk är detta fortfarande namnet på drogen. Termen "morfin", som används på engelska och franska, gavs av den franske fysikern Joseph Louis Gay-Lussac .
Ett betydande bidrag till alkaloidernas kemi under de första åren av dess utveckling gjordes av de franska forskarna Pierre Joseph Pelletier och Joseph Bienaimé Caventou , som upptäckte kinin (1820) och stryknin (1818). Flera andra alkaloider upptäcktes runt den tiden, inklusive xantin (1817), atropin (1819), koffein (1820), koniin (1827), nikotin ( 1828), kolchicin (1833), spartein (1851) och kokain (1860) . Utvecklingen av alkaloidernas kemi accelererades av uppkomsten av spektroskopiska och kromatografiska metoder under 1900-talet, så att 2008 hade mer än 12 000 alkaloider identifierats.
Den första fullständiga syntesen av en alkaloid uppnåddes 1886 av den tyske kemisten Albert Ladenburg . Han producerade konin genom att reagera 2-metylpyridin med acetaldehyd och reducera den resulterande 2-propenylpyridinen med natrium.

Klassificeringar
Jämfört med de flesta andra klasser av naturliga föreningar kännetecknas alkaloider av en stor strukturell mångfald. Det finns ingen enhetlig klassificering. Till en början, när kunskap om kemiska strukturer saknades, förlitade man sig på botanisk klassificering av källväxterna. Denna klassificering anses nu vara föråldrad.
mellan kolskelettet ( t.ex. indol- , isokinolin- och pyridinliknande ) eller biokemisk prekursor ( ornitin , lysin , tyrosin , tryptofan , etc.). De kräver dock kompromisser i gränsfall; till exempel nikotin ett pyridinfragment från nikotinamid och en pyrrolidindel från ornitin och kan därför hänföras till båda klasserna.
Alkaloider delas ofta in i följande huvudgrupper:
- "Äkta alkaloider" innehåller kväve i heterocykeln och kommer från aminosyror . Deras karakteristiska exempel är atropin , nikotin och morfin . Denna grupp inkluderar också några alkaloider som förutom kväveheterocykeln innehåller terpen ( t.ex. evonin) eller peptidfragment ( t.ex. ergotamin ). Piperidinalkaloiderna coniine och coniceine kan betraktas som äkta alkaloider (snarare än pseudoalkaloider: se nedan) även om de inte härrör från aminosyror.
- "Protoalkaloider", som innehåller kväve (men inte kvävets heterocykel) och även härstammar från aminosyror. Exempel inkluderar meskalin , adrenalin och efedrin .
- Polyaminalkaloider – derivat av putrescin , spermidin och spermin .
- Peptid- och cyklopeptidalkaloider.
- Pseudoalkaloider – alkaloidliknande föreningar som inte kommer från aminosyror. Denna grupp inkluderar terpenliknande och steroidliknande alkaloider, såväl som purinliknande alkaloider såsom koffein , teobromin , teakrin och teofyllin . Vissa författare klassificerar som pseudoalkaloider sådana föreningar som efedrin och katinon . De härstammar från aminosyran fenylalanin , men får inte sin kväveatom från aminosyran utan genom transaminering .
Vissa alkaloider har inte det kolskelett som är karakteristiskt för sin grupp. Så galantamin och homoaporfiner innehåller inte isokinolinfragment , utan hänförs i allmänhet till isokinolinalkaloider.
Huvudklasser av monomera alkaloider listas i tabellen nedan:
| Klass | Stora grupper | Huvudsyntessteg | Exempel |
|---|---|---|---|
| Alkaloider med kväve heterocykler (äkta alkaloider) | |||
| Pyrrolidinderivat _ | Ornitin eller arginin → putrescin → N-metylputrescin → N-metyl-Δ 1 - pyrrolin | Cuscohygrine , hygrine , hygrolin, stachydrine | |
| Tropanderivat _ |
Atropingrupp Substitution i positionerna 3, 6 eller 7 |
Ornitin eller arginin → putrescin → N-metylputrescin → N-metyl-Δ 1 - pyrrolin | Atropin , skopolamin , hyoscyamin |
|
Kokaingruppsersättning på position 2 och 3 |
Kokain , ekgonin | ||
| Pyrrolizidinderivat _ | Icke-estrar | I växter: ornitin eller arginin → putrescin → homospermidin → retronecin | Retronecin , heliotridin, laburnin |
| Komplexa estrar av monokarboxylsyror | Indicine, lindelofin, sarracin | ||
| Makrocykliska diestrar | Platyphylline, trichodesmine | ||
| 1-aminopyrrolizidiner ( lolines ) | Hos svampar : L -prolin + L -homoserin → N- (3-amino-3-karboxipropyl)prolin → norlolin | Lolin, N -formyllolin, N -acetyllolin | |
| Piperidinderivat _ | Lysin → kadaverin → Ai - piperidein | Sedamin, lobelin, anaferin, piperin | |
| Oktansyra → konicein → konin | Coniine , coniceine | ||
| Kinolizidinderivat _ | Lupiningruppen _ | Lysin → kadaverin → Ai - piperidein | Lupinin , nufaridin |
| Cytisingrupp _ | Cytisin | ||
| Sparteinska gruppen | Spartein , lupanin, anahygrin | ||
| Matringrupp . | Matrin, oxymatrin, allomatridin | ||
| Ormosanine grupp | Ormosanin, piptantin | ||
| Indolizidinderivat _ | Lysin → δ-semialdehyd av α-aminoadipinsyra → pipekolsyra → 1 indolizidinon | Swainsonin , kastanospermin | |
| Pyridinderivat _ | Enkla derivat av pyridin | Nikotinsyra → dihydronikotinsyra → 1,2-dihydropyridin | Trigonellin , ricinin , arecoline |
| Polycykliska icke-kondenserande pyridinderivat | Nikotin , nornikotin , anabasin , anatabin | ||
| Polycykliska kondenserade pyridinderivat | Aktinidin , gentianin , pedikulinin | ||
| Sesquiterpen pyridinderivat | Nikotinsyra , isoleucin | Evonin, hippokratein, triptonin | |
| Isokinolinderivat och relaterade alkaloider | Enkla derivat av isokinolin | Tyrosin eller fenylalanin → dopamin eller tyramin (för alkaloider Amarillis) | Salsolin , lophocerin |
| Derivat av 1- och 3-isokinoliner | N-metylkoridaldin, noroxihydrastinin | ||
| Derivat av 1- och 4-fenyltetrahydroisokinoliner | Kryptostilin | ||
| Derivat av 5-naftil-isokinolin | Ancistrokladin | ||
| Derivat av 1- och 2-bensylisokinoliner | Papaverin , laudanosin , sendaverin | ||
| Kularingrupp | Cularine, yagonine | ||
| Paviner och isopaviner | Argemonine, amurensine | ||
| Bensopyrrokoliner | Kryptaustolin | ||
| Protoberberiner | Berberin , kanadin , ofiokarpin, mecambridin, corydalin | ||
| Ftaliisokinoliner | Hydrastin , narkotin (Noscapin) | ||
| Spirobensylisokinoliner | Fumaricine | ||
| Ipecacuanha alkaloider | Emetin, protoemetin, ipecoside | ||
| Bensofenantridiner | Sanguinarin, oxynitidin, corynoloxin | ||
| Aporfiner | Glaucin , koridin, liriodenin | ||
| Proaporfiner | Pronuciferin, glaziovin | ||
| Homoaporfiner | Kreysiginin, multifloramin | ||
| Homoproporfiner | Bulbokodin | ||
| Morfin | Morfin , kodein , tebain , sinomenin | ||
| Homomorfiner | Kreysiginin, androcymbine | ||
| Tropoloisokinoliner | Imerubrine | ||
| Azofluorantener | Rufescin, imelutein | ||
| Amaryllis alkaloider | Lykorin , ambellin, tazettin, galantamin , montanin | ||
| Erythrina alkaloider | Erysodin, erytroidin | ||
| Fenantrenderivat _ | Atherosperminin | ||
| Protopiner | Protopin , oxomuramin, corycavidin | ||
| Aristolactam | Doriflavin | ||
| Oxazolderivat _ | Tyrosin → tyramin | Annulolin, halfordinol, texaline, texamin | |
| Isoxazolderivat _ | Ibotensyra → Muscimol | Ibotensyra, Muscimol | |
| Tiazolderivat _ | 1-deoxi-D-xylulos 5-fosfat (DOXP), tyrosin , cystein | Nostocyklamid, tiostrepton | |
| Kinazolinderivat _ | 3,4-dihydro-4-kinazolonderivat | Antranilsyra eller fenylalanin eller ornitin | Febrifugine |
| 1,4-dihydro-4-kinazolonderivat | Glykorin, arborin, glykosminin | ||
| Pyrrolidin och piperidin kinazolinderivat | Vazicin (peganin) | ||
| Akridinderivat _ | Antranilsyra | Rutakridon, akronicin | |
| Kinolinderivat _ | Enkla derivat av kinolinderivat av 2-kinoloner och 4-kinoloner | Antranilsyra → 3-karboxikinolin | Kusparin, echinopsin, evokarpin |
| Tricykliska terpenoider | Flindersine | ||
| Furanokinolinderivat | Dictamnine, fagarine, skimmianine | ||
| Kininer | Tryptofan → tryptamin → strictosidin (med secologanin ) → korinanteal → cinhoninon | Kinin , kinidin , cinchonin , cinhonidin | |
| Indolderivat _ | Icke-isoprenindolalkaloider | ||
| Enkla indolderivat | Tryptofan → tryptamin eller 5-hydroxitryptofan | Serotonin , psilocybin , dimetyltryptamin (DMT), bufotenin | |
| Enkla derivat av β-karbolin | Harman, harmine , harmaline , eleganine | ||
| Pyrroloindolalkaloider | Fysiostigmin (eserin), eteramin, fysovenin, eptastigmin | ||
| Semiterpenoid indol alkaloider | |||
| Ergotalkaloider | Tryptofan → kanoklavin → agroklavin → elimoklavin → paspalinsyra → lyserginsyra | Ergotamin , ergobasin, ergosin | |
| Monoterpenoid indol alkaloider | |||
| Alkaloider av Corynanthe -typ | Tryptofan → tryptamin → strictosidin (med secologanin ) | Ajmalicin, sarpagin, vobasin, ajmalin , yohimbin , reserpin , mitragynin , gruppstrychnin och ( strychnine brucin , aquamicine, vomicine) | |
| Alkaloider av Iboga -typ | Ibogamin , ibogain , voacangine | ||
| Alkaloider av aspidosperma -typ | Vincamine , vinca alkaloider , vinkotin, aspidospermin | ||
| Imidazolderivat _ | Direkt från histidin | Histamin , pilokarpin, pilosin, stevensin | |
| Purinderivat _ | Xantosin (bildas i purinbiosyntes) → 7 metylxantosin → 7-metylxantin → teobromin → koffein | Koffein , teobromin , teofyllin , saxitoxin | |
| Alkaloider med kväve i sidokedjan (protoalkaloider) | |||
| β- Fenyletylaminderivat _ | Tyrosin eller fenylalanin → dioxifenilalanin → dopamin → adrenalin och meskalin tyrosin → tyramin fenylalanin → 1-fenylpropan-1,2-dion → katinon → efedrin och pseudoefedrin | Tyramin , efedrin , pseudoefedrin , meskalin , katinon , katekolaminer ( adrenalin , noradrenalin , dopamin ) | |
| Colchicin alkaloider | Tyrosin eller fenylalanin → dopamin → höstlin → kolchicin | Kolkicin , kolkamin | |
| Muskarin | Glutaminsyra → 3-ketoglutaminsyra → muskarin (med pyrodruvsyra ) | Muskarin , allomuskarin, epimuskarin, epiallomuskarin | |
| Bensylamin | Fenylalanin med valin , leucin eller isoleucin | Capsaicin , dihydrocapsaicin , nordihydrocapsaicin, vanillylamin | |
| Polyaminer alkaloider | |||
| Putrescin- derivat | ornitin → putrescin → spermidin → spermin | Paucine | |
| Spermidinderivat _ | Lunarine, codonokarpin | ||
| Sperminderivat _ | Verbascenin, afelandrin | ||
| Peptid (cyklopeptid) alkaloider | |||
| Peptidalkaloider med en 13-ledad cykel | Nummularine C typ | Från olika aminosyror | Nummularine C, Nummularine S |
| Ziziphin typ | Ziziphine A, sativanin H | ||
| Peptidalkaloider med en 14-ledad cykel | Frangulanin typ | Frangulanine, scutianine J | |
| Scutianine A typ | Scutianine A | ||
| Helgerrin typ | Integerrin, discarine D | ||
| Amfibin F typ | Amfibin F, spinanin A | ||
| Amfibin B typ | Amfibin B, lotusin C | ||
| Peptidalkaloider med en 15-ledad cykel | Mucronine A typ | Mucronine A | |
| Pseudoalkaloider ( terpener och steroider ) | |||
| Diterpener | Lykoktonin typ | Mevalonsyra → Isopentenylpyrofosfat → geranylpyrofosfat | Akonitin , delfinin |
| Steroida alkaloider | Kolesterol , arginin | Solanidin , cyklopamin , batrakotoxin | |
Egenskaper

De flesta alkaloider innehåller syre i sin molekylstruktur; dessa föreningar är vanligtvis färglösa kristaller vid omgivningsförhållanden. Syrefria alkaloider, såsom nikotin eller konin , är vanligtvis flyktiga, färglösa, oljiga vätskor. Vissa alkaloider är färgade, som berberin (gul) och sanguinarin (orange).
De flesta alkaloider är svaga baser, men vissa, såsom teobromin och teofyllin , är amfotera . Många alkaloider löser sig dåligt i vatten men löser sig lätt i organiska lösningsmedel , såsom dietyleter , kloroform eller 1,2-dikloretan . Koffein , kokain , kodein och nikotin är svagt lösliga i vatten (med en löslighet på ≥1g/L), medan andra, inklusive morfin och yohimbin , är mycket svagt vattenlösliga (0,1–1 g/L). Alkaloider och syror bildar salter av olika styrka. Dessa salter är vanligtvis fritt lösliga i vatten och etanol och dåligt lösliga i de flesta organiska lösningsmedel. Undantag inkluderar skopolaminhydrobromid , som är lösligt i organiska lösningsmedel, och det vattenlösliga kininsulfatet.
De flesta alkaloider har en bitter smak eller är giftiga vid intag. Alkaloidproduktion i växter verkade ha utvecklats som svar på utfodring av växtätande djur; dock har vissa djur utvecklat förmågan att avgifta alkaloider. Vissa alkaloider kan ge utvecklingsdefekter hos avkomman till djur som konsumerar men inte kan avgifta alkaloiderna. Ett exempel är alkaloiden cyklopamin , som produceras i bladen på majslilja . Under 1950-talet hade upp till 25 % av de lamm som föddes av får som hade betat på majslilja allvarliga ansiktsdeformationer. Dessa sträckte sig från deformerade käkar till cyklopi (se bild). Efter årtionden av forskning, på 1980-talet, identifierades den förening som var ansvarig för dessa missbildningar som alkaloiden 11-deoxyjervin, senare omdöpt till cyklopamin.
Utbredning i naturen
Alkaloider genereras av olika levande organismer, särskilt av högre växter - cirka 10 till 25% av dem innehåller alkaloider. Därför associerades termen "alkaloid" tidigare med växter.
Alkaloidhalten i växter ligger vanligtvis inom några få procent och är inhomogen över växtvävnaderna. Beroende på typen av växter observeras den maximala koncentrationen i bladen (till exempel svart hönsbane ), frukter eller frön ( Strychnine tree ), rot ( Rauvolfia serpentina ) eller bark ( cinchona ). Dessutom kan olika vävnader av samma växter innehålla olika alkaloider.
Förutom växter finns alkaloider i vissa typer av svampar , såsom psilocybin i fruktkropparna av släktet Psilocybe , och i djur, såsom bufotenin i huden på vissa paddor och ett antal insekter, markant myror. Många marina organismer innehåller också alkaloider. Vissa aminer , såsom adrenalin och serotonin , som spelar en viktig roll i högre djur, liknar alkaloider i sin struktur och biosyntes och kallas ibland alkaloider.
Extraktion
På grund av den strukturella mångfalden av alkaloider finns det ingen enskild metod för att utvinna dem från naturliga råvaror. De flesta metoder utnyttjar egenskaperna hos de flesta alkaloider att vara lösliga i organiska lösningsmedel men inte i vatten, och deras salter har en motsatt tendens.
De flesta växter innehåller flera alkaloider. Deras blandning extraheras först och sedan separeras individuella alkaloider. Växter mals noggrant före extraktion. De flesta alkaloider finns i de råa växterna i form av salter av organiska syror. De extraherade alkaloiderna kan förbli salter eller förändras till baser. Basextraktion uppnås genom att bearbeta råmaterialet med alkaliska lösningar och extrahera alkaloidbaserna med organiska lösningsmedel, såsom 1,2-dikloretan, kloroform, dietyleter eller bensen. Sedan löses föroreningarna av svaga syror; detta omvandlar alkaloidbaser till salter som tvättas bort med vatten. Om nödvändigt görs en vattenlösning av alkaloidsalter igen alkalisk och behandlas med ett organiskt lösningsmedel. Processen upprepas tills önskad renhet uppnås.
I den sura extraktionen bearbetas det råa växtmaterialet av en svag sur lösning ( t.ex. ättiksyra i vatten, etanol eller metanol) . En bas tillsätts sedan för att omvandla alkaloider till basiska former som extraheras med organiskt lösningsmedel (om extraktionen utfördes med alkohol, avlägsnas den först och resten löses i vatten). Lösningen renas såsom beskrivits ovan.
Alkaloider separeras från sin blandning med hjälp av deras olika löslighet i vissa lösningsmedel och olika reaktivitet med vissa reagens eller genom destillation .
Ett antal alkaloider identifieras från insekter , bland vilka brandmyrgiftalkaloider som kallas solenopsiner har fått större uppmärksamhet från forskare . Dessa insektsalkaloider kan effektivt extraheras genom lösningsmedelsnedsänkning av levande eldmyror eller genom centrifugering av levande myror följt av silikagelkromatografirening. Spårning och dosering av de extraherade solenopsin-antalkaloiderna har beskrivits som möjligt baserat på deras absorbanstopp runt 232 nanometer.
Biosyntes
Biologiska prekursorer för de flesta alkaloider är aminosyror , såsom ornitin , lysin , fenylalanin , tyrosin , tryptofan , histidin , asparaginsyra och antranilsyra . Nikotinsyra kan syntetiseras från tryptofan eller asparaginsyra. Metoderna för alkaloidbiosyntes är för många och kan inte lätt klassificeras. Det finns emellertid några typiska reaktioner involverade i biosyntesen av olika klasser av alkaloider, inklusive syntes av Schiff-baser och Mannich-reaktion .
Syntes av Schiff-baser
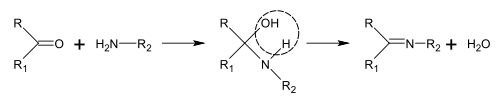
Schiff-baser kan erhållas genom att reagera aminer med ketoner eller aldehyder. Dessa reaktioner är en vanlig metod för att producera C=N-bindningar.
Vid biosyntesen av alkaloider kan sådana reaktioner äga rum inom en molekyl, såsom vid syntesen av piperidin:
Mannich reaktion
En integrerad komponent i Mannich-reaktionen, förutom en amin och en karbonylförening , är en karbanjon , som spelar rollen som nukleofilen i den nukleofila tillsatsen till jonen som bildas genom reaktionen mellan aminen och karbonylen.
Mannich-reaktionen kan fortgå både intermolekylärt och intramolekylärt:
Dimer alkaloider
Förutom de ovan beskrivna monomera alkaloiderna finns det även dimera och till och med trimera och tetramera alkaloider som bildas vid kondensation av två, tre och fyra monomera alkaloider. Dimeriska alkaloider bildas vanligtvis av monomerer av samma typ genom följande mekanismer:
- Mannich-reaktion , vilket resulterar i t.ex. voacamine
- Michael reaktion (villalstonine)
- Kondensering av aldehyder med aminer (toxiferin)
- Oxidativ tillsats av fenoler (dauricin, tubokurarin)
- Laktonisering (karpain).
Det finns också dimera alkaloider som bildas av två distinkta monomerer, såsom vinca -alkaloiderna vinblastin och vincristine, som bildas från kopplingen av katharantin och vindolin . Det nyare halvsyntetiska kemoterapeutiska medlet vinorelbin används vid behandling av icke-småcellig lungcancer . Det är ett annat derivat dimer av vindolin och katarantin och syntetiseras från anhydrovinblastin , med utgångspunkt från antingen leurosin eller själva monomererna.
Biologisk roll
Alkaloider är bland de viktigaste och mest kända sekundära metaboliterna , dvs biogena ämnen som inte är direkt involverade i den normala tillväxten , utvecklingen eller reproduktionen av organismen. Istället förmedlar de i allmänhet ekologiska interaktioner , vilket kan ge en selektiv fördel för organismen genom att öka dess överlevnadsförmåga eller fruktbarhet . I vissa fall är deras funktion, om någon, fortfarande oklar. , att alkaloider är slutprodukterna av kvävemetabolism i växter, som urea och urinsyra är i däggdjur, tillbakavisades av upptäckten att deras koncentration fluktuerar snarare än att stadigt öka.
De flesta av de kända funktionerna hos alkaloider är relaterade till skydd. Till exempel aporfinalkaloid liriodenin som produceras av tulpanträdet det från parasitiska svampar . Dessutom förhindrar närvaron av alkaloider i växten insekter och kordatdjur från att äta den. Vissa djur är dock anpassade till alkaloider och använder dem till och med i sin egen ämnesomsättning. Sådana alkaloidrelaterade ämnen som serotonin , dopamin och histamin är viktiga signalsubstanser hos djur. Alkaloider är också kända för att reglera växternas tillväxt. Ett exempel på en organism som använder alkaloider för skydd är Utetheisa ornatrix , mer allmänt känd som den utsmyckade malen. Pyrrolizidinalkaloider gör dessa larver och vuxna nattfjärilar obehagliga för många av deras naturliga fiender som coccinelidbaggar, gröna spetsvingar, insektsätande hemiptera och insektsätande fladdermöss. Ett annat exempel på att alkaloider används förekommer i den giftiga hemlockmalen ( Agonopterix alstroemeriana). Denna nattfjäril livnär sig på sin mycket giftiga och alkaloidrika värdväxtgift ( Conium maculatum ) under dess larvstadium. A. alstroemeriana kan gynnas dubbelt av toxiciteten hos de naturligt förekommande alkaloiderna, både genom artens osmaklighet för rovdjur och genom förmågan hos A. alstroemeriana att känna igen Conium maculatum som den korrekta platsen för äggläggning. En brandmyrgiftalkaloid känd som solenopsin har visat sig skydda drottningar av invasiva eldmyror under grundandet av nya bon, och spelar därmed en central roll i spridningen av denna art av skadedjur över hela världen .
Ansökningar
I medicin
Medicinsk användning av alkaloid-innehållande växter har en lång historia, och därför, när de första alkaloiderna isolerades på 1800-talet, fann de omedelbart tillämpning i klinisk praxis. Många alkaloider används fortfarande inom medicin, vanligtvis i form av salter som används ofta, inklusive följande:
| Alkaloid | Handling |
|---|---|
| Ajmaline | antiarytmika |
| Emetine | antiprotozomedel , |
| Ergotalkaloider | Vasokonstriktion , hallucinogen , Uterotonisk |
| Glaucin | Hostdämpande |
| Morfin | Analgetikum |
| Nikotin | Stimulerande , nikotinacetylkolinreceptoragonist |
| Fysiostigmin | hämmare av acetylkolinesteras |
| Kinidin | Antiarytmik |
| Kinin | Antipyretisk , antimalariamedel |
| Reserpin | antihypertensiva |
| Tubokurarin | Muskelavslappnande |
| Vinblastin , vinkristin | antitumör |
| Vincamine | vasodilaterande , antihypertensiva |
| Yohimbine | stimulerande , afrodisiakum |
Många syntetiska och semisyntetiska droger är strukturella modifieringar av alkaloiderna, som utformades för att förstärka eller förändra läkemedlets primära effekt och minska oönskade biverkningar. Till exempel naloxon , en opioidreceptorantagonist , ett derivat av tebain som finns i opium .
I jordbruket
Före utvecklingen av ett brett spektrum av relativt lågtoxiska syntetiska bekämpningsmedel , användes vissa alkaloider, såsom salter av nikotin och anabasin , som insekticider . Deras användning begränsades av deras höga toxicitet för människor.
Använd som psykoaktiva droger
Preparat av växter som innehåller alkaloider och deras extrakt, och senare rena alkaloider, har länge använts som psykoaktiva ämnen . Kokain , koffein och katinon är stimulantia för det centrala nervsystemet . Meskalin och många indolalkaloider (som psilocybin , dimetyltryptamin och ibogain ) har hallucinogen effekt. Morfin och kodein är starka narkotiska smärtstillande medel.
Det finns alkaloider som inte har någon stark psykoaktiv effekt själva, utan är prekursorer för halvsyntetiska psykoaktiva droger. Till exempel används efedrin och pseudoefedrin för att producera metkatinon och metamfetamin . Tebain används i syntesen av många smärtstillande medel som oxikodon .
Se även
Förklarande anteckningar
Citat
Allmänna och citerade referenser
- Aniszewski, Tadeusz (2007). Alkaloider: livets hemligheter . Amsterdam: Elsevier . ISBN 978-0-444-52736-3 .
- Begley, Tadhg P. (2009). Encyclopedia of Chemical Biology . ChemBioChem . Vol. 10. Wiley. s. 1569–1570. doi : 10.1002/cbic.200900262 . ISBN 978-0-471-75477-0 .
- Brossi, Arnold (1989). Alkaloiderna: Kemi och farmakologi . Akademisk press.
- Dewick, Paul M. (2002). Medicinal Natural Products: A Biosynthetic Approach (andra upplagan). Wiley. ISBN 978-0-471-49640-3 .
- Fattorusso, E.; Taglialatela-Scafati, O. (2008). Moderna alkaloider: struktur, isolering, syntes och biologi . Wiley-VCH. ISBN 978-3-527-31521-5 .
- Grinkevitj NI; Safronich LN, red. (1983). Den kemiska analysen av medicinalväxter (på ryska). Moskva: Vysshaya Shkola.
- Hesse, Manfred (2002). Alkaloider: Naturens förbannelse eller välsignelse? . Wiley-VCH. ISBN 978-3-906390-24-6 .
- Knunyants, IL (1988). Kemisk uppslagsverk . Sovjetiskt uppslagsverk.
- Orekhov, AP (1955). Kemi-alkaloider (Acad. 2:a uppl.). Moskva.
- Plemenkov, VV (2001). Introduktion till naturliga föreningars kemi . Kazan.
- Saxton, JE (1971). Alkaloiderna: en periodisk rapport för specialister . London: The Chemical Society.
- Veselovskaya, NB; Kovalenko, AE (2000). Droger . Moskva: Triada-X.
- Wink, M (2009). "Verkande och toxikologi för växtgifter och giftiga växter". Mitt. Julius Kühn-Inst . 421 : 93–112x.
externa länkar
-
 Media relaterade till alkaloider på Wikimedia Commons
Media relaterade till alkaloider på Wikimedia Commons -
 Citat relaterade till Alkaloid på Wikiquote
Citat relaterade till Alkaloid på Wikiquote