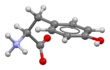
Tyrosin
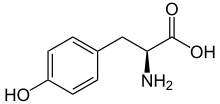
Skelettformel av L -tyrosin
|
|||

L -Tyrosin vid fysiologiskt pH
|
|||
|
|
|||
| Namn | |||
|---|---|---|---|
|
IUPAC namn
( S )-tyrosin
|
|||
| Andra namn
L -2-amino-3-(4-hydroxifenyl)propansyra
|
|||
| Identifierare | |||
|
|||
|
3D-modell ( JSmol )
|
|||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard | 100.000.419 | ||
| KEGG | |||
|
PubChem CID
|
|||
| UNII | |||
|
CompTox Dashboard ( EPA )
|
|||
|
|||
|
|||
| Egenskaper | |||
| C9H11NO3 _ _ _ _ _ _ | |||
| Molar massa | 181,191 g·mol -1 | ||
| 0,0453 g/100 ml | |||
| -105,3·10 -6 cm3 / mol | |||
| Faror | |||
| NFPA 704 (branddiamant) | |||
| Kompletterande datasida | |||
| Tyrosine (datasida) | |||
|
Om inte annat anges ges data för material i standardtillstånd (vid 25 °C [77 °F], 100 kPa).
|
|||
L -tyrosin eller tyrosin (symbol Tyr eller Y ) eller 4-hydroxifenylalanin är en av de 20 standardaminosyrorna som används av celler för att syntetisera proteiner . Det är en icke-essentiell aminosyra med en polär sidogrupp . Ordet "tyrosin" kommer från grekiskans tyrós , som betyder ost , eftersom det först upptäcktes 1846 av den tyske kemisten Justus von Liebig i proteinet kasein från ost. Det kallas tyrosyl när det hänvisas till som en funktionell grupp eller sidokedja. Medan tyrosin i allmänhet klassificeras som en hydrofob aminosyra, är det mer hydrofilt än fenylalanin . Det kodas av kodonen UAC och UAU i budbärar-RNA .
Funktioner
Förutom att vara en proteinogen aminosyra har tyrosin en speciell roll i kraft av fenolfunktionaliteten . Det förekommer i proteiner som ingår i signaltransduktionsprocesser och fungerar som en mottagare av fosfatgrupper som överförs via proteinkinaser . Fosforylering av hydroxylgruppen kan ändra aktiviteten hos målproteinet, eller kan utgöra en del av en signalkaskad via SH2-domänbindning .
En tyrosinrest spelar också en viktig roll i fotosyntesen . I kloroplaster ( fotosystem II ) fungerar den som en elektrondonator i reduktionen av oxiderat klorofyll . I denna process förlorar den väteatomen i sin fenoliska OH-grupp. Denna radikal reduceras därefter i fotosystemet II av de fyra kärnmanganklustren.
Kostbehov och källor
Referensintaget i kosten för tyrosin uppskattas vanligtvis tillsammans med fenylalanin . Det varierar beroende på en uppskattningsmetod, men den ideala andelen av dessa två aminosyror anses vara 60:40 (fenylalanin:tyrosin) eftersom en människokropp har en sådan sammansättning. Tyrosin, som också kan syntetiseras i kroppen från fenylalanin, finns i många proteinrika livsmedel såsom kyckling , kalkon , fisk , mjölk , yoghurt , keso , ost , jordnötter , mandlar , pumpafrön , sesamfrön , soja produkter och limabönor , men även i avokado och bananer . Till exempel har äggvitan cirka 250 mg per ägg, medan magert nötkött, lamm, fläsk, lax, kyckling och kalkon innehåller cirka 1 g per 3 ounce (85 g) portion.
Biosyntes

I växter och de flesta mikroorganismer produceras tyrosin via prefenat , en mellanprodukt på shikimatvägen . Prefenat dekarboxyleras oxidativt med retention av hydroxylgruppen för att ge p -hydroxifenylpyruvat, som transamineras med glutamat som kvävekälla för att ge tyrosin och a-ketoglutarat .
Däggdjur syntetiserar tyrosin från den essentiella aminosyran fenylalanin (Phe), som härrör från mat. Omvandlingen av Phe till Tyr katalyseras av enzymet fenylalaninhydroxylas , ett monooxygenas. Detta enzym katalyserar reaktionen och orsakar tillsats av en hydroxylgrupp till änden av den aromatiska 6-kolsringen av fenylalanin , så att det blir tyrosin.
Ämnesomsättning
Fosforylering och sulfatering
Vissa av tyrosinresterna kan märkas (vid hydroxylgruppen) med en fosfatgrupp ( fosforylerad ) av proteinkinaser . I sin fosforylerade form kallas tyrosin fosfotyrosin . Tyrosinfosforylering anses vara ett av nyckelstegen i signaltransduktion och reglering av enzymatisk aktivitet. Fosfotyrosin kan detekteras genom specifika antikroppar . Tyrosinrester kan också modifieras genom tillsats av en sulfatgrupp, en process som kallas tyrosinsulfatering . Tyrosinsulfatering katalyseras av tyrosylproteinsulfotransferas (TPST). Liksom fosfotyrosinantikropparna som nämnts ovan har antikroppar nyligen beskrivits som specifikt detekterar sulfotyrosin.
Prekursor till neurotransmittorer och hormoner
I dopaminerga celler i hjärnan omvandlas tyrosin till L-DOPA av enzymet tyrosinhydroxylas (TH). TH är det hastighetsbegränsande enzymet som är involverat i syntesen av signalsubstansen dopamin . Dopamin kan sedan omvandlas till andra katekolaminer , såsom noradrenalin (noradrenalin) och adrenalin (adrenalin).
Sköldkörtelhormonerna trijodtyronin (T 3 ) och tyroxin ( T 4 ) i sköldkörtelns kolloid härrör också från tyrosin .
|
|
Prekursor till alkaloider
Latexen från Papaver somniferum , opiumvallmo, har visat sig omvandla tyrosin till alkaloid morfin och den biosyntetiska vägen har etablerats från tyrosin till morfin genom att använda Carbon-14 radiomärkt tyrosin för att spåra in vivo-syntesvägen .
Prekursor till naturliga fenoler
Tyrosinammoniaklyas (TAL) är ett enzym i den naturliga fenolernas biosyntesväg. Det omvandlar L-tyrosin till p-kumarsyra .
Föregångare till pigment
Tyrosin är också föregångaren till pigmentet melanin .
Roll i syntesen av koenzym Q10
Tyrosin (eller dess prekursor fenylalanin) behövs för att syntetisera bensokinonstrukturen som utgör en del av koenzym Q10 .
Degradering

Nedbrytningen av L-tyrosin (syn. para -hydroxifenylalanin) börjar med en a-ketoglutaratberoende transaminering genom tyrosintransaminaset till para -hydroxifenylpyruvat . Positionsbeskrivningen para , förkortad p , betyder att hydroxylgruppen och sidokedjan på fenylringen är mittemot varandra (se illustrationen nedan).
Nästa oxidationssteg katalyserar med p -hydroxifenylpyruvatdioxygenas och avspjälkning av CO2 - homogenisat (2,5-dihydroxifenyl-1-acetat). För att dela den aromatiska ringen av homogentisat krävs ytterligare ett dioxygenas, homogentiserat 1,2-dioxygenas . Därigenom, genom inkorporering av ytterligare en O 2 -molekyl, skapas maleylacetoacetat .
Fumarylacetoacetat skapas av maleylacetoacetat cis - trans - isomeras genom rotation av karboxylgruppen som skapas från hydroxylgruppen via oxidation. Detta cis-trans -isomeras innehåller glutation som ett koenzym . Fumarylacetoacetat delas slutligen av enzymet fumarylacetoacetathydrolas genom tillsats av en vattenmolekyl.
Därigenom frigörs fumarat (även en metabolit i citronsyracykeln) och acetoacetat (3-ketobutyroat). Acetoacetat är en ketonkropp , som aktiveras med succinyl-CoA, och därefter kan den omvandlas till acetyl-CoA, som i sin tur kan oxideras av citronsyracykeln eller användas för fettsyrasyntes .
Phloretinsyra är också en urinmetabolit av tyrosin hos råttor.
Orto- och meta-tyrosin

Tre strukturella isomerer av L-tyrosin är kända. Förutom den vanliga aminosyran L-tyrosin, som är para-isomeren ( para -tyr, p -tyr eller 4-hydroxifenylalanin), finns det ytterligare två regioisomerer, nämligen meta - tyrosin (även känd som 3-hydroxifenylalanin , L- m -tyrosin och m -tyr) och orto -tyrosin ( o -tyr eller 2-hydroxifenylalanin), som förekommer i naturen. M - tyr- och o -tyr-isomererna, som är sällsynta, uppstår genom icke-enzymatisk friradikal- hydroxylering av fenylalanin under oxidativ stress .
m-tyrosin och analoger (sällsynta i naturen men tillgängliga syntetiskt) har visat sig användas vid Parkinsons sjukdom , Alzheimers sjukdom och artrit .
Medicinsk användning
Tyrosin är en föregångare till neurotransmittorer och ökar plasmanivåerna av neurotransmittorer (särskilt dopamin och noradrenalin), men har liten om någon effekt på humöret hos normala försökspersoner. Ett antal studier har funnit att tyrosin är användbart under stress, kyla, trötthet (hos möss), långvarigt arbete och sömnbrist, med minskningar av stresshormonnivåer, minskningar av stressinducerad viktminskning sett i djurförsök och förbättringar i kognitiva och fysisk prestation sett i mänskliga försök.
Tyrosin verkar inte ha någon signifikant effekt på kognitiva eller fysiska prestationer under normala omständigheter, men hjälper till att upprätthålla arbetsminnet bättre under multitasking.
Interaktioner
Det är okänt om MAO-hämmare interagerar med tyrosin.
Industriell syntes
L-tyrosin och dess derivat ( L-DOPA , melanin , fenylpropanoider och andra) används i läkemedel , kosttillskott och livsmedelstillsatser . Två metoder användes tidigare för att tillverka L-tyrosin. Den första innefattar extraktion av den önskade aminosyran från proteinhydrolysat med användning av ett kemiskt tillvägagångssätt. Den andra använder enzymatisk syntes från fenoler, pyruvat och ammoniak genom användning av tyrosin fenol-lyas . Framsteg inom genteknik och tillkomsten av industriell fermentering har flyttat syntesen av L-tyrosin till användningen av konstruerade stammar av E. coli .
Se även
- Albinism
- Alkaptonuria
- Betalain
- Joderade tyrosinderivat
- Paulys reaktion
- Tyramin
- Tyrosinsulfatering
- Tyrosinemi
externa länkar
- Tyrosin MS Spectrum
- Tyrosinmetabolism Arkiverad 2019-07-26 på Wayback Machine
- Fenylalanin och tyrosinbiosyntes
- Biosyntes av fenylalanin, tyrosin och tryptofan
- Tyrosin i ChemIDplus-databasen