Aromatisk aminosyra
En aromatisk aminosyra är en aminosyra som innehåller en aromatisk ring.
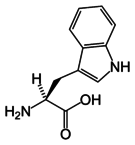
Bland de 20 standardaminosyrorna anses följande klassiskt vara aromatiska: fenylalanin , tryptofan och tyrosin . Även om histidin innehåller en aromatisk ring, gör dess grundläggande egenskaper att den till övervägande del klassificeras som en polär aminosyra.
Kemisk struktur och egenskaper
Aromatiska aminosyror absorberar ultraviolett ljus vid en våglängd över 250 nm och producerar fluorescens . Denna egenskap används i kvantitativ analys, särskilt för att bestämma koncentrationerna av dessa aminosyror i lösning. Detta uppnåddes genom användningen av en UV-spektrofotomer och Beer-Lambert Law- ekvationen. De flesta proteiner kommer att ha ett absorptionsmaximum vid 280 nm på grund av närvaron av aromatiska aminosyror i deras primära struktur. Men eftersom det finns flera aromatiska aminosyror har denna metod låg noggrannhet; för att mildra detta problem måste det önskade proteinet vara rent och dess molära absorptionsförmåga är känd. Dessutom kommer ett protein utan aromatiska aminosyror inte att ha ett absorptionsmaximum vid ungefär 280 nm. Närvaron av nukleinsyror i proteinet kan ytterligare minska metodens noggrannhet på grund av närvaron av purin- och pyrimidinringar , som har ett absorptionsmaximum vid cirka 260 nm. Fenylalanin har en relativt svag absorbans i jämförelse med de andra vanliga aromatiska aminosyrorna; dess närvaro i ett protein kan endast detekteras om tryptofan och tyrosin inte är närvarande. Dess absorptionsmaximum inträffar vid 257 nm. Följaktligen har den en relativt svag fluorescens. Tryptofan har den högsta relativa absorbansen i jämförelse med de andra aromatiska standardaminosyrorna; dess absorptionsmaximum inträffar vid 280 nm. Sidokedjan av tryptofan titreras inte. Absorptionsmaximum för tyrosin inträffar vid 274 nm. I kemiska reaktioner kan tyrosin fungera som en nukleofil. Aromatiska aminosyror spelar också en avgörande roll i glykan-proteininteraktioner .
Förekomst och funktioner inom biokemi
Roll i proteinstruktur och funktion
Aromatiska aminosyror spelar en avgörande roll för att stabilisera de veckade strukturerna hos många proteiner. Aromatiska rester återfinns huvudsakligen sekvestrerade i kärnorna av globulära proteiner, även om de ofta innefattar nyckeldelar av protein-protein- eller protein-ligandinteraktionsgränssnitt på proteinytan.
Biosyntesvägar
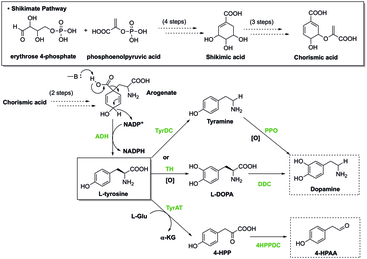
Shikimate väg
I växter leder shikimatvägen först till bildandet av korismat , som är föregångaren till fenylalanin, tyrosin och tryptofan. Dessa aromatiska aminosyror är derivat av många sekundära metaboliter , alla väsentliga för en växts biologiska funktioner, såsom hormonerna salicylat och auxin . Denna väg innehåller enzymer som kan regleras av inhibitorer, som kan upphöra med produktionen av korismat, och i slutändan organismens biologiska funktioner. Herbicider och antibiotika verkar genom att hämma dessa enzymer som är involverade i biosyntesen av aromatiska aminosyror, vilket gör dem giftiga för växter. Glyfosat , en typ av herbicid, används för att kontrollera ansamlingen av överflödigt grönt. Förutom att förstöra grönt, kan glyfosat lätt påverka upprätthållandet av tarmmikrobiotan i värdorganismer genom att specifikt hämma 5-enolpyruvylshikinate-3-fosfatsyntaset som förhindrar biosyntesen av essentiella aromatiska aminosyror. Hämning av detta enzym resulterar i störningar såsom mag-tarmsjukdomar och metabola sjukdomar.
Aromatiska aminosyror som prekursorer
Aromatiska aminosyror fungerar ofta som prekursorer till andra molekyler. Till exempel, vid produktionen av adrenalin, är fenylalanin startmolekylen. Reaktionen anges nedan:
- Fenylalanin → Tyrosin → L-DOPA → Dopamin → Noradrenalin → Epinefrin
Tyrosin är också en prekursor för syntesen av oktopamin och melanin i många organismer. Vid produktionen av tyroxin fungerar fenylalanin också som den första prekursorn:
Vid produktionen av serotonin är tryptofan startmolekylen, som anges nedan:
Dessutom är histidin prekursorn till histamin . Tryptofan är startmolekylen i syntesen av tryptamin, serotonin, auxin, kynureniner och melatonin.
Näringsbehov
Djur får aromatiska aminosyror från sin kost, men alla växter och mikroorganismer måste syntetisera sina aromatiska aminosyror genom den metaboliskt kostsamma shikimatvägen för att kunna tillverka dem. Fenylalanin , tryptofan och histidin är essentiella aminosyror för djur. Eftersom de inte syntetiseras i människokroppen måste de härröra från kosten. Tyrosin är halvessentiellt; därför kan det syntetiseras av djuret, men endast från fenylalanin. Fenylketonuri , en genetisk störning som uppstår som ett resultat av oförmågan att bryta ned fenylalanin, beror på brist på enzymet fenylalaninhydroxylas . En dietbrist på tryptofan kan orsaka hämmad skelettutveckling. Överdrivet intag av aromatiska aminosyror långt över nivåer som erhålls genom normal proteinkonsumtion kan leda till hypertoni , något som kan förbli obemärkt under lång tid hos friska individer. Det kan också orsakas av andra faktorer som användningen av olika örter och livsmedel som choklad som hämmar monoaminoxidasenzymer i varierande grad, och även vissa mediciner. Aromatiska spåraminer som tyramin kan ersätta noradrenalin från perifera monoaminvesiklar och hos personer som tar MAO-hämmare inträffar detta i den utsträckningen att det är livshotande. för Blue diaper syndrome är en autosomal recessiv sjukdom som orsakas av dålig absorption av tryptofan i kroppen.
Se även
- Aromatisk L-aminosyradekarboxylas
- Utökad genetisk kod
- Fenylketonuri
- Tyrosinhydroxylas
- Neurotransmittor
Vidare läsning
- Maeda H, Dudareva N (2012). "Shikimatvägen och aromatisk aminosyrabiosyntes i växter". Årlig översyn av växtbiologi . 63 : 73–105. doi : 10.1146/annurev-arplant-042811-105439 . PMID 22554242 .
- "Tyrosinhydroxylasbrist" . Genetiks hemreferens . US National Library of Medicine. 2020.
externa länkar
-
 Media relaterade till aromatiska aminosyror på Wikimedia Commons
Media relaterade till aromatiska aminosyror på Wikimedia Commons - Aromatiska+aminosyror vid US National Library of Medicine Medical Subject Headings (MeSH)