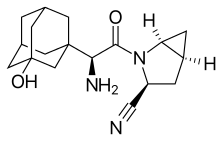
Saxagliptin
 | |
| Kliniska data | |
|---|---|
| Handelsnamn | Onglyza |
| Andra namn | BMS-477118 |
| AHFS / Drugs.com | Professionella drogfakta |
| MedlinePlus | a610003 |
| Licensdata |
|
Graviditetskategori _ |
|
Administreringsvägar _ |
Genom munnen ( tabletter ) |
| Läkemedelsklass | DPP-4-hämmare |
| ATC-kod | |
| Rättslig status | |
| Rättslig status | |
| Farmakokinetiska data | |
| Biotillgänglighet | ~75 % (T max = 2 timmar) |
| Proteinbindning | försumbar |
| Ämnesomsättning | Lever ( CYP3A4 och CYP3A5 ) |
| Eliminationshalveringstid _ | 2,5 h (saxagliptin), 3,1 h (huvudmetabolit) |
| Exkretion | 22 % ( gallgång ), 75 % ( urin ) |
| Identifierare | |
| |
| CAS-nummer |
|
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII |
|
| KEGG | |
| ChEBI | |
| ChEMBL | |
| CompTox Dashboard ( EPA ) | |
| Kemiska och fysikaliska data | |
| Formel | C18H25N3O2 _ _ _ _ _ _ _ |
| Molar massa | 315,417 g·mol -1 |
| 3D-modell ( JSmol ) | |
| |
| |
|
| |
Saxagliptin , som säljs under varumärket Onglyza , är ett oralt hypoglykemiskt medel ( läkemedel mot diabetes ) av klassen dipeptidylpeptidas-4 (DPP-4) hämmare . Tidig utveckling var enbart av Bristol-Myers Squibb ; 2007 AstraZeneca ihop med Bristol-Myers Squibb för att tillsammans utveckla den slutliga substansen och samarbeta kring marknadsföringen av läkemedlet.
I april 2016 lade amerikanska FDA till en varning om ökad risk för hjärtsvikt . Detta baserades på data i en artikel som drog slutsatsen "DPP-4-hämning med saxagliptin ökade eller minskade inte frekvensen av ischemiska händelser, även om antalet sjukhusinläggningar för hjärtsvikt ökade. Även om saxagliptin förbättrar den glykemiska kontrollen, är andra tillvägagångssätt nödvändiga för att minska kardiovaskulär risk hos patienter med diabetes."
Medicinsk användning
Saxagliptin används som monoterapi eller i kombination med andra läkemedel för behandling av typ 2-diabetes . Det verkar inte minska risken för hjärtinfarkt eller stroke . Det ökar risken för sjukhusvistelse för hjärtsvikt med cirka 27 %. Liksom andra DPP-4-hämmare har den relativt måttlig HbA1c-sänkande förmåga, är associerad med en relativt låg risk för hypoglykemi och orsakar inte viktökning.
Saxagliptin förbättrade genomsnittliga HbA1c -nivåer (i förhållande till placebo) i en 24-veckors studie på personer med typ 2-diabetes. Kombinationsbehandling med saxagliptin och metformin var effektivare än saxagliptin eller metformin som monoterapi. När de relativa fördelarna med att öka dosen av en sulfonylurea eller lägga till saxagliptin utvärderades i en studie med 768 patienter, visades kombinationsbehandlingar ha en signifikant större effekt på fastande blodsocker än att enbart öka den testade glibenklamiddosen.
Skadliga effekter
Hos dem som tar sulfonureider finns en ökad risk för lågt blodsocker .
3 biverkningar sågs högre i saxagliptin jämfört med placebo. Tabell 1: Biverkningar (oavsett utredarens bedömning av orsakssamband) i placebokontrollerade prövningar* Rapporterade hos ≥ 5 % av patienterna som behandlats med ONGLYZA (saxagliptintabletter) 5 mg och vanligare än hos patienter behandlade med placebo.
| ONGLYZA 5 mg N=882 | Placebo N=799 | |
|---|---|---|
| Övre luftvägsinfektion | 68 (7,7) | 61 (7,6) |
| Urinvägsinfektion | 60 (6,8) | 49 (6,1) |
| Huvudvärk | 57 (6,5) | 47 (5,9) |
- De 5 placebokontrollerade studierna inkluderar två monoterapistudier och en tilläggsstudie för kombinationsterapi med var och en av följande: metformin, tiazolidindion eller glyburid. Tabell visar 24-veckorsdata oavsett glykemisk räddning.
I februari 2012 distribuerade Bristol-Myers/Astra Zeneca ytterligare säkerhetsinformation om saxagliptinanvändning i Sydafrika. Bipacksedeln ska redigeras för Sydafrika. Kontraindikationer kommer nu att inkludera en historia av känslighet för saxagliptin (eller annan DPP4-hämmare) samt pankreatit. Spontant rapporterade biverkningar i Sydafrika har inkluderat anafylaxi, angioödem och akut pankreatit. [ läkarintyg behövs ]
I en prövning av kardiovaskulära resultat gav saxagliptinbehandling en liten ökning av risken för att bli inlagd på sjukhus för hjärtsvikt. Saxagliptin kan orsaka ledvärk som kan vara allvarlig och invalidiserande. Saxagliptin kan öka risken för hjärtsvikt.
Tolerabilitet
Både monoterapi och kombinationsbehandling med andra medel tolererades i allmänhet väl i kliniska prövningar.
Pankreatit och pankreascancer
En associering av DPP-IV-hämmareklassen med pankreasproblem har föreslagits, huvudsakligen baserat på fallrapporter associerade med DPP-IV-hämmaren sitagliptin och flera inkretinmimetika inklusive exenatid . En studie från 2013 av DPP-4-hämmaren sitagliptin rapporterade fann "oroande förändringar i bukspottkörteln hos råttorna som kan leda till cancer i bukspottkörteln". En andra artikel av samma författare rapporterade en ökning av precancerösa lesioner i bukspottkörteln hos organdonatorer som hade tagit GLP-1-hämmare. Som svar på dessa rapporter genomförde USA:s FDA och European Medicines Agency var och en oberoende granskning av alla kliniska och prekliniska data relaterade till det möjliga sambandet mellan DPP-IV-hämmare och pankreascancer. I ett gemensamt brev till New England Journal of Medicines uppgav byråerna att "Båda byråerna är överens om att påståenden om ett orsakssamband mellan inkretinbaserade läkemedel och pankreatit eller pankreascancer, som nyligen uttryckts i den vetenskapliga litteraturen och i media, är inte överensstämmer med nuvarande data. FDA och EMA har inte kommit till en slutlig slutsats i nuläget angående ett sådant orsakssamband. Även om den samlade data som har granskats ger trygghet, kommer pankreatit att fortsätta att betraktas som en risk förknippad med dessa läkemedel tills mer data finns tillgängliga; båda myndigheterna fortsätter att undersöka denna säkerhetssignal."
Rättegångar har lämnats in där målsägande som utvecklat bukspottkörtelcancer hävdar att DPP-IV-hämmare eller inkretiner hade en orsaksroll i utvecklingen av deras cancer.
Produktion
Syntesen av saxagliptin av Bristol-Myers Squibb genom amidkoppling av N-Boc-3-hydroxiadamantylglycin ( 2 ) och metanoprolinamid ( 3 ) med EDC . Den förra är kommersiellt tillgänglig, medan den senare är tillgänglig som N-Boc-analogen. Prolineamiddelen dehydratiseras därefter med trifluorättiksyraanhydrid för att ge cyaniden som trifluoracetatestern, som hydrolyseras. Avlägsnande av Boc-skyddsgruppen följt av neutralisering ger den önskade produkten ( 1 ):
Farmakologi
Saxagliptin är en del av en klass av diabetesläkemedel som kallas dipeptidylpeptidas-4 (DPP-4)-hämmare. DPP-4 är ett enzym som bryter ner inkretinhormoner . Som en DPP-4-hämmare bromsar saxagliptin nedbrytningen av inkretinhormoner, vilket ökar nivån av dessa hormoner i kroppen. Det är denna ökning av inkretinhormoner som är ansvarig för saxagliptins fördelaktiga verkan, inklusive ökad insulinproduktion som svar på måltider och minskad glukoneogeneshastighet i levern.
Dipeptidylpeptidas-4s roll i blodsockerreglering tros vara genom nedbrytning av GIP och nedbrytning av GLP-1 .
Eftersom inkretinhormoner är mer aktiva som svar på högre blodsockernivåer (och är mindre aktiva som svar på lågt blodsocker), är risken för farligt lågt blodsocker (hypoglykemi) låg vid monoterapi med saxagliptin.
Licensiering
En ny läkemedelsansökan för saxagliptin vid behandling av typ 2-diabetes lämnades in till FDA i juni 2008. Den baserades på ett läkemedelsutvecklingsprogram med 8 randomiserade studier: 1 fas 2-studie med dosintervall (2,5–100 mg/d) ; 6 fas 3, 24-veckors kontrollerade studier med ytterligare kontrollerad uppföljning från 12 till 42 månader, dubbelblindade genomgående; och en 12-veckors verkningsmekanismstudie med en 2-årig uppföljningsperiod. FDA godkände saxagliptin med varumärket Onglyza den 31 juli 2009. Saxagliptin licensierades för användning i hela Europeiska unionen av European Medicines Agency den 1 december 2009. Bristol-Myers Squibb meddelade den 27 december 2006 att Otsuka Pharmaceutical Co. beviljat exklusiva rättigheter att utveckla och kommersialisera föreningen i Japan. Enligt licensavtalet kommer Otsuka att stå för alla utvecklingskostnader, men Bristol-Myers Squibb behåller rättigheterna att sammarknadsföra saxagliptin med Otsuka i Japan. Vidare tillkännagavs den 11 januari 2007 att Bristol-Myers Squibb och AstraZeneca skulle arbeta tillsammans för att slutföra utvecklingen av läkemedlet och i efterföljande marknadsföring.
externa länkar
- "Saxagliptin" . Läkemedelsinformationsportal . US National Library of Medicine.
- Banting och Best Diabetes Center vid UT dpp4
