Cyklisk neutropeni
| Cyklisk neutropeni | |
|---|---|
| Andra namn | Periodisk neutropeni, cyklisk leukopeni, cyklisk hematopoes |
| Specialitet |
Hematologi |
| Symtom | Feber, sjukdomskänsla, inflammation och infektion i munslemhinnan, luftvägarna, mag-tarmkanalen, hud och buksmärtor |
| Vanligt debut | Barndom |
| Orsaker | Mutation i ELANE -genen |
| Diagnostisk metod | Blodprov , genetisk testning |
| Behandling | G-CSF |
| Medicin | Filgrastim |
| Frekvens | 1 på miljon (2018) |
Cyklisk neutropeni ( CyN ) är en sällsynt hematologisk störning och form av medfödd neutropeni som tenderar att inträffa ungefär var tredje vecka och varar i några dagar åt gången på grund av förändrade hastigheter för neutrofilproduktion i benmärgen . Det orsakar ett tillfälligt tillstånd med lågt absolut antal neutrofiler och eftersom neutrofilerna utgör majoriteten av cirkulerande vita blodkroppar utsätter det kroppen för en allvarlig risk för inflammation och infektion . I jämförelse med svår medfödd neutropeni svarar den bra på behandling med granulocytkolonistimulerande faktor ( filgrastim ), vilket ökar antalet neutrofiler, förkortar cykellängden och minskar infektionernas svårighetsgrad och frekvens.
tecken och symtom
De vanligaste symtomen på neutropeni är återkommande feber , sjukdomskänsla , inflammation i vävnaderna som omger tänderna, munsår , inflammation och bakteriell infektion i luftvägarna, mag-tarmkanalen, huden och buksmärtor. Det anses att den största risken för dödsfall är att utveckla nekrotiserande enterokolit (NEC), peritonit , bakteriemi eller Clostridium och Escherichia coli sepsis och septisk chock och lunginflammation .
Orsaker
Cyklisk neutropeni (CyN), liksom allvarlig medfödd neutropeni (SCN), är en sällsynt sjukdom. Det anses att i den allmänna befolkningen har CyN en frekvens på en på en miljon. Det är resultatet av autosomal dominant mutation i ELANE -genen som ligger på den korta armen (p) av kromosom 19 (19p13.3), genen som kodar för neutrofilt elastas , vilket också är den vanligaste orsaken till SCN. Det förekommer sporadiskt som en de novo mutationsvariant eller kan förekomma bland medlemmar av samma familj. När det gäller CyN har mutationsvarianterna visat sig mestadels klunga ihop sig i intron 4 och exon 4 och 5, men var också lokaliserade i intron 3 och exon 2 och 3. Vissa mutationsvarianter har hittats i både Cyn och SCN, vilket indikerar att de är fenotyper av samma sjukdom med olika svårighetsgrad.
Det anses att mutationen orsakar en minskning av "neutrofilproduktionen eller överdriven apoptos (kortare halveringstid)" vilket resulterar i en brist på mogna neutrofiler i blodet. Den exakta patologiska mekanismen undersöks fortfarande, med huvudhypoteserna är fellokalisering av ELANE eller oveckat proteinsvar (UPR) inducerat av mutant ELANE , dock enligt Mehta et al. (2016), "UPR-induktion av mutant ELANE är inte tillräckligt stark för att främja celldöd och att mutant ELANE orsakar SCN genom en alternativ mekanism". Enligt Garg et al. (2020), nya "fynd utmanar den för närvarande rådande modellen som SCN är resultatet av mutant ELANE , som utlöser endoplasmatisk retikulumstress, UPR och apoptos". Uttrycket av ELANE -genen har kopplats till GFI1- genen, och vissa ansåg att interaktion med andra gener orsakar uppkomsten och svårighetsgraden av den ena eller andra fenotypiska störningen. Det är oklart vad som orsakar den cykliska aspekten i CyN. Enligt Donadieu et al. (2011), den "cykliska aspekten ... antyder att det finns en kryptisk biologisk klocka som reglerar granulopoiesis . Denna förmodade klocka kan avslöjas av särskilda mutationer". Michael Mackey "postulerar att produktionen av neutrofiler styrs av långväga stimulerande faktorer i en lång återkopplingsslinga som har en inbyggd tidsfördröjning i mognaden av promyelocyter till helt differentierade neutrofiler". Det är inte heller klart vad som orsakar att nivåerna av sekretorisk leukocytproteashämmare ( SLPI ), som påverkar induktionen av det oveckade proteinsvaret (UPR), inte minskar och som sådan är aktivering av UPR frånvarande i CyN jämfört med SCN, i med andra ord, olika ELANE -mutationer "har olika effekter på UPR-aktivering, och SLPI reglerar omfattningen av ELANE-utlöst UPR".
En studie från 2020 publicerad i Annals of the New York Academy of Sciences om CyNs patomekanism avslöjade att "vissa HSPC:er undkommer UPR-inducerad endoplasmatisk retikulum (ER) stress och förökar sig som svar på granulocytkolonistimulerande faktor (G-CSF) för att en viss tröskel vid vilken UPR återigen påverkar majoriteten av HSPCs. Det finns en cyklisk balans mellan ER-stressinducerad apoptos av HSPCs och kompensatorisk G-CSF-stimulerad HSPC-proliferation följt av granulocytisk differentiering"; med andra ord, CyN "kännetecknas av cyklande UPR-aktiviteter och cyklande UPR-flyktande celler". Den mest sannolika anledningen till att från samma mutationsvariant utvecklar SCN och inte CyN är också på grund av allvarligare skador orsakade av UPR-stress i SCN.
Diagnos
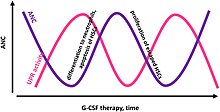
En diagnos bekräftas vanligtvis genom att övervaka antalet absoluta neutrofiler (ANC) tre gånger per vecka i minst sex veckor. Bekräftelsen kan assisteras med Lomb periodogram . Under tillståndet, som varar i tre till sex dagar och tenderar att inträffa ungefär var tredje vecka (men kan variera från 14 till 36 dagar), är det absoluta antalet neutrofiler (ANC) mindre än 200-500 celler/mikroL (<0,2- 0,5x10 9 /L), med ökning av antalet monocyter och milda svängningar av andra celler, inklusive en mild anemi . Mellan cyklerna når neutrofilantalet mestadels toppar vid subnormala eller normala värden.
Genetisk testning rekommenderas för mutationer i ELANE och andra neutropenirelaterade gener (som HAX1 , G6PC3 , GFI1 etc.) för att skilja det från andra sekundära orsaker och former av neutropeni. I vissa fall kan intervaller och oscillationer vara lägre, vilket gör ANC-analysen otillräcklig, och eftersom båda sjukdomarna kan ha samma mutationsvarianter i ELANE är det att föredra att ha både ANC och genetisk analys för att bekräfta i diagnosen om det är allvarligt medfödd eller cyklisk neutropeni.
Behandling
Även om individer mellan cyklerna i allmänhet är friska och symtomen tenderar att förbättras i vuxen ålder, rekommenderas det att undvika aktiviteter som är utsatta för skador, att ha regelbunden mun- och tandvård och att undvika BCG- vaccin . Det rekommenderas att övervaka vita blodkroppar flera gånger om året. Behandlingen efter symtomen bör vara omedelbar för att förhindra infektioner, särskilt under feber när det kräver bredspektrum antibiotikabehandling (se febril neutropeni) . Den viktigaste och ofta livräddande behandlingen är den förebyggande behandlingen av granulocytkolonistimulerande faktor (G-CSF), i form av filgrastim , som reglerar produktionen av neutrofiler i benmärgen, men förkortar den neutropena cykeln till cirka 7 -14 dagar och varaktigheten av det svåra tillståndet. De subkutana injektionerna, med mediandosering på 1,5 μg/kg/dag, kan ges dagligen, intermittent en gång var tredje dag, eller tidsinställda för att bara behandla den neutropena perioden. Behandlingen anses vara "säker och effektiv", utan några signifikanta negativa effekter, förutom risk för utveckling av osteopeni .
Den granulocyt-makrofagkolonistimulerande faktorn (GM-CSF) är mindre effektiv med fler negativa effekter. Ett annat alternativ är hematopoetisk stamcellstransplantation (HSCT), men praktiseras vanligtvis i SCN, och i ett fall mellan två syskondonatorer, varav en genomgick HSCT-behandling för akut myeloid leukemi (AML) medan den andra hade CyN och vars märg var överfördes, överfördes också CyN genom allogen märgtransplantation. Det visar att CyN är en stamcellsstörning . Årliga benmärgsundersökningar rekommenderas inte.
Prognos
Det finns en mycket hög risk för livshotande infektioner och död i tidig ålder. Livskvaliteten och överlevnaden förbättras avsevärt med G-CSF-behandling, som praktiseras sedan slutet av 1980-talet. Till skillnad från svår medfödd neutropeni har individer med cyklisk neutropeni ett bättre svar på G-CSF och har ingen risk att utveckla myelodysplastiskt syndrom (MDS) och akut myeloid leukemi (AML). Men vid långtidsobservationer av över 300 patienter med CyN har det förekommit ett fall av att utveckla kronisk myelogen leukemi (KML) och ett av AML, vilket indikerar att det också är ett preleukemiskt tillstånd, men risken är "mycket låg" (1%), och risken är "korrelerad med sjukdomens svårighetsgrad snarare än med förekomsten av en ELANE-mutation". Enligt Donadieu et al. (2011), "den kumulativa risken för att uppleva minst en allvarlig (potentiellt livshotande) infektion vid 20 års ålder är liknande hos patienter med permanent och cyklisk neutropeni, även om de tidigare patienterna tenderar att ha tidigare manifestationer".
Historia
Först beskrevs 1910, det föreslogs och bekräftades ha ett autosomalt dominant (AD) arv på 1940- och 1960-talen, men skiljdes från medfödda neutropenier fram till 1990-talet då stamtavlor analyserades och genetiska mutationer delades av patienter med allvarlig medfödd neutropeni .