Tallium(I)oxid
|
|
|
|
|
| Namn | |
|---|---|
| Andra namn Tallosoxid
|
|
| Identifierare | |
|
3D-modell ( JSmol )
|
|
| ECHA InfoCard | 100.013.838 |
| EG-nummer |
|
|
PubChem CID
|
|
| UNII | |
|
CompTox Dashboard ( EPA )
|
|
|
|
|
|
| Egenskaper | |
| Tl2O _ _ | |
| Molar massa | 424,77 g/mol |
| Utseende |
svarta ortorombiska kristaller hygroskopiska |
| Densitet | 10,45 g/cm 3 |
| Smältpunkt | 596 °C (1 105 °F; 869 K) |
| Kokpunkt | 1 080 °C (1 980 °F; 1 350 K) (sönderdelas) |
| löslig (reagerar) | |
| Löslighet | löslig i alkohol och syra |
| Strukturera | |
| Rhombohedral , hR18 | |
| R-3m, nr 166 | |
| Besläktade föreningar | |
|
Andra katjoner
|
Tallium(III)oxid |
|
Om inte annat anges ges data för material i standardtillstånd (vid 25 °C [77 °F], 100 kPa).
|
|
Tallium(I)oxid är den oorganiska föreningen av tallium och syre med formeln Tl 2 O där tallium är i sitt +1 oxidationstillstånd . Den är svart och producerar en basisk gul lösning av tallium(I)hydroxid (TlOH) när den löses i vatten. Den bildas genom att värma fast TlOH eller Tl 2 CO 3 i frånvaro av luft. Talliumoxid används för att göra speciellt glas med högt brytningsindex . Talliumoxid är en komponent i flera högtemperatursupraledare . Tallium(I)oxid reagerar med syror och bildar tallium(I)salter.
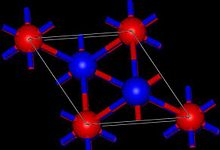
Tl 2 O antar anti- kadmiumjodidstrukturen i fast tillstånd. På detta sätt är Tl(I)-centra pyramidformade och oxidcentra är oktaedriska .
Tallium(I)oxid är, liksom alla talliumföreningar, mycket giftigt.
Förberedelse
Tallium(I)oxid kan framställas genom nedbrytning av tallium(I)hydroxid vid 100 °C eller genom att värma upp tallium(III)oxid i frånvaro av luft till 700 °C.
externa länkar

