Rutenium(IV)oxid
|
|
| Namn | |
|---|---|
|
IUPAC-namn
Rutenium(IV)oxid
|
|
| Andra namn Ruteniumdioxid
|
|
| Identifierare | |
|
3D-modell ( JSmol )
|
|
| ECHA InfoCard | 100.031.660 |
| EG-nummer |
|
|
PubChem CID
|
|
|
CompTox Dashboard ( EPA )
|
|
|
|
|
|
| Egenskaper | |
| RuO 2 | |
| Molar massa | 133,0688 g/mol |
| Utseende | blå-svart fast |
| Densitet | 6,97 g/cm 3 |
| Kokpunkt | 1 200 °C (2 190 °F; 1 470 K) sublimerar |
| olöslig | |
| +162,0·10 -6 cm3 / mol | |
| Strukturera | |
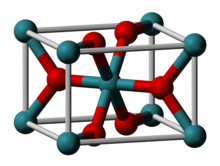
| Rutil (tetragonal), tP6 | |
| P 4 2 / mnm , nr 136 | |
| Octahedral (Ru IV ); trigonal plan (O 2− ) | |
| Faror | |
| Flampunkt | Ej brandfarlig |
| Besläktade föreningar | |
|
Andra anjoner
|
Ruteniumdisulfid |
|
Andra katjoner
|
Osmium(IV)oxid |
|
Relaterade ruteniumoxider _
|
Ruteniumtetroxid |
| Kompletterande datasida | |
| Ruthenium(IV)oxid (datasida) | |
|
Om inte annat anges ges data för material i standardtillstånd (vid 25 °C [77 °F], 100 kPa).
|
|
Ruthenium(IV)oxid är den oorganiska föreningen med formeln Ru O 2 . Denna svarta fasta substans är den vanligaste ruteniumoxiden . Det används i stor utsträckning som en elektrokatalysator för att producera klor, kloroxider och O 2 . Som många andra dioxider antar RuO 2 rutilstrukturen .
Förberedelse
Det framställs vanligtvis genom oxidation av ruteniumtriklorid . Nästan stökiometriska enkristaller av RuO 2 kan erhållas genom kemisk ångtransport med O 2 som transportmedel:
- RuO 2 + O 2 ⇌ RuO 4
Filmer av RuO 2 kan framställas genom kemisk ångavsättning (CVD) från flyktiga ruteniumföreningar. RuO 2 kan också framställas genom elektroplätering från en lösning av ruteniumtriklorid.
Elektrostatiskt stabiliserade hydrosoler av orörd ruteniumdioxidhydrat har framställts genom att utnyttja den autokatalytiska reduktionen av ruteniumtetroxid i vattenlösning. De resulterande partikelpopulationerna kan kontrolleras så att de innefattar väsentligen monodispersa, enhetliga sfärer med diametrar i intervallet 40 nm - 160 nm.
Används
Ruthenium(IV)oxid används som huvudkomponent i katalysatorn i Sumitomo- Deacon-processen som producerar klor genom oxidation av väteklorid .
RuO 2 kan användas som katalysator i många andra situationer. Anmärkningsvärda reaktioner är Fischer-Tropsch-processen , Haber-Bosch-processen och olika manifestationer av bränsleceller .
Potentiella och nischade applikationer
RuO 2 används i stor utsträckning för beläggning av titananoder för elektrolytisk produktion av klor och för beredning av resistorer eller integrerade kretsar . Ruteniumoxidresistorer kan användas som känsliga termometrar i temperaturområdet 0,02 < T < 4 K. Det kan även användas som aktivt material i superkondensatorer eftersom det har mycket hög laddningsöverföringsförmåga. Ruteniumoxid har stor kapacitet att lagra laddning när den används i vattenlösningar. Genomsnittlig kapacitet av rutenium(IV)oxid har nått 650 F/g i H 2 SO 4 -lösning och glödgat vid temperaturer lägre än 200 °C. I försök att optimera dess kapacitiva egenskaper har tidigare arbete tittat på hydratiseringen av ruteniumoxid, dess kristallinitet och partikelstorlek.