Näthinnan
| Retina | |
|---|---|
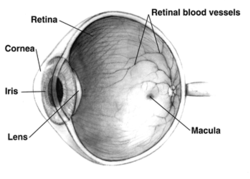 Höger mänskligt öga tvärsnittsvy; ögon varierar avsevärt mellan djur.
| |
| Detaljer | |
| Uttal |
Storbritannien : / ˈ r ɛ t ɪ n ə / , USA : / ˈ r ɛ t ən ə / , pl. retinae /- n i / |
| Del av | Öga |
| Systemet | Visuellt system |
| Artär | Central retinal artär |
| Identifierare | |
| latin | Rēte, tunica interna bulbi |
| Maska | D012160 |
| TA98 | A15.2.04.002 |
| TA2 | 6776 |
| FMA | 58301 |
| Anatomisk terminologi | |
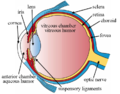
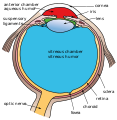
Näthinnan (från latin : rete "nät") är det innersta , ljuskänsliga lagret av vävnad i ögat hos de flesta ryggradsdjur och vissa blötdjur . Ögats optik skapar en fokuserad tvådimensionell bild av den visuella världen på näthinnan, som sedan bearbetar den bilden i näthinnan och skickar nervimpulser längs synnerven till den visuella cortex för att skapa visuell perception . Näthinnan har en funktion som på många sätt är analog med film- eller bildsensorn i en kamera .
Den neurala näthinnan består av flera lager av neuroner sammankopplade av synapser och stöds av ett yttre lager av pigmenterade epitelceller. De primära ljusavkännande cellerna i näthinnan är fotoreceptorcellerna, som är av två typer: stavar och kottar . Stavar fungerar huvudsakligen i svagt ljus och ger monokromatisk syn. Koner fungerar i väl upplysta förhållanden och är ansvariga för uppfattningen av färg genom användning av en rad olika funktioner , såväl som syn med hög skärpa som används för uppgifter som läsning. En tredje typ av ljusavkännande cell, den ljuskänsliga gangliecellen , är viktig för att fånga dygnsrytmer och reflexiva reaktioner som pupillljusreflexen .
Ljus som träffar näthinnan initierar en kaskad av kemiska och elektriska händelser som i slutändan utlöser nervimpulser som skickas till olika syncentra i hjärnan genom fibrerna i synnerven . Neurala signaler från stavarna och konerna genomgår bearbetning av andra neuroner, vars produktion tar formen av aktionspotentialer i retinala ganglieceller vars axoner bildar synnerven. Flera viktiga egenskaper hos visuell perception kan spåras till näthinnans kodning och bearbetning av ljus.
I embryonal utveckling av ryggradsdjur uppstår näthinnan och synnerven som utväxter av den utvecklande hjärnan, särskilt embryonal diencephalon ; således anses näthinnan vara en del av det centrala nervsystemet (CNS) och är egentligen hjärnvävnad. Det är den enda delen av CNS som kan visualiseras icke-invasivt . Ungefär som resten av hjärnan är isolerad från kärlsystemet via blod-hjärnbarriären , skyddas näthinnan på liknande sätt av blod-näthinnan .
Strukturera
Inverterad kontra icke-inverterad näthinna
Ryggradsnäthinnan är inverterad i den meningen att de ljusavkännande cellerna finns på baksidan av näthinnan, så att ljus måste passera genom lager av nervceller och kapillärer innan det når de ljuskänsliga delarna av stavarna och konerna. Ganglioncellerna, vars axoner bildar synnerven, finns längst fram på näthinnan; därför måste synnerven passera genom näthinnan på väg till hjärnan. Inga fotoreceptorer finns i denna region, vilket ger upphov till den blinda fläcken . Däremot i bläckfiskens näthinna är fotoreceptorerna framför, med bearbetande neuroner och kapillärer bakom dem. På grund av detta har bläckfiskar inte en blind fläck.
Även om den överliggande neurala vävnaden är delvis genomskinlig, och de medföljande gliacellerna har visat sig fungera som fiberoptiska kanaler för att transportera fotoner direkt till fotoreceptorerna, sker ljusspridning . Vissa ryggradsdjur, inklusive människor, har ett område på den centrala näthinnan som är anpassat för syn med hög skärpa. Detta område, som kallas fovea centralis , är avaskulärt (har inga blodkärl) och har minimal neural vävnad framför fotoreceptorerna, vilket minimerar ljusspridning.
Bläckfiskarna har en icke-inverterad näthinna, som är jämförbar när det gäller upplösningsförmåga för ögonen hos många ryggradsdjur. Bläckfiskögon har inte en analog av ryggradsdjurets retinala pigmentepitel (RPE). Även om deras fotoreceptorer innehåller ett protein, retinokrom, som återvinner retinal och replikerar en av funktionerna hos ryggradsdjurets RPE, bibehålls sannolikt inte bläckfiskfotoreceptorer lika bra som hos ryggradsdjur, och som ett resultat är den användbara livslängden för fotoreceptorer hos ryggradslösa djur mycket kortare än hos ryggradsdjur. Att lätt byta ut stjälkögon (vissa hummer) eller näthinnan (vissa spindlar, som Deinopis ) förekommer sällan.
Bläckfiskens näthinna har inte sitt ursprung som en utväxt av hjärnan, som ryggradsdjuret gör. Denna skillnad tyder på att ögon på ryggradsdjur och bläckfisk inte är homologa , utan har utvecklats separat. Ur ett evolutionärt perspektiv kan en mer komplex struktur som den inverterade näthinnan i allmänhet uppstå som en konsekvens av två alternerande processer - en fördelaktig "bra" kompromiss mellan konkurrerande funktionella begränsningar, eller som en historisk maladaptiv kvarleva från organevolutionens invecklade väg. och transformation. Syn är en viktig anpassning hos högre ryggradsdjur.
En tredje syn på det "omvända" ryggradsdjursögat är att det kombinerar två fördelar - underhållet av de ovan nämnda fotoreceptorerna och den minskning av ljusintensiteten som krävs för att undvika att förblinda fotoreceptorerna, som är baserade på förfädernas extremt känsliga ögon. modern hagfish (fiskar som lever i mycket djupt, mörkt vatten).
Näthinneskikt

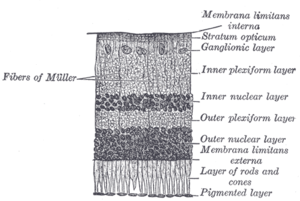
Ryggradsnäthinnan har 10 distinkta lager. Från närmast till längst från glaskroppen:
- Inre begränsande membran – basalmembran framställt av Müller-celler
- Nervfiberlager – axoner i ganglioncellkropparna (observera att ett tunt lager av Müllers cellfotplattor finns mellan detta lager och det inre begränsande membranet)
- Gangliecellskikt – innehåller kärnor av ganglieceller, vars axoner blir synnervsfibrer och några förskjutna amakrinceller
- Inre plexiformskikt – innehåller synapsen mellan de bipolära cellaxonerna och dendriterna i ganglie- och amakrincellerna
- Det inre kärnskiktet – innehåller kärnorna och omgivande cellkroppar (perikarya) av amakrincellerna , bipolära cellerna och horisontella cellerna
- Yttre plexiforma skikt – utsprång av stavar och koner som slutar i stavsfären respektive konpedikeln, dessa gör synapser med dendriter av bipolära celler och horisontella celler. I den makulära regionen är detta känt som Fiberskiktet av Henle .
- Yttre kärnskikt – cellkroppar av stavar och kottar
- Externt begränsande membran – skikt som separerar de inre segmentdelarna av fotoreceptorerna från deras cellkärnor
- Inre segment / yttre segmentlager – inre segment och yttre segment av stavar och koner, de yttre segmenten innehåller en högspecialiserad ljusavkännande apparat.
- Retinalt pigmentepitel – ett enda lager av kubiska epitelceller (med extruderingar som inte visas i diagrammet). Detta lager ligger närmast åderhinnan, och ger näring och stödjande funktioner till neurala näthinnan. Det svarta pigmentet melanin i pigmentlagret förhindrar ljusreflektion över hela ögongloben; detta är oerhört viktigt för klar vision.
Dessa lager kan grupperas i fyra huvudsakliga bearbetningssteg - fotomottagning; överföring till bipolära celler ; överföring till ganglionceller , som också innehåller fotoreceptorer, de ljuskänsliga ganglioncellerna ; och överföring längs synnerven. Vid varje synaptisk stadium horisontella och amakrina celler också lateralt anslutna.
Synnerven är en central del av många axoner av ganglionceller som i första hand ansluter till den laterala geniculate kroppen , en visuell relästation i diencephalon (baksidan av framhjärnan). Den projicerar också till den överlägsna colliculus , den suprachiasmatiska kärnan och kärnan i det optiska området. Den passerar genom de andra lagren och skapar den optiska skivan hos primater.
Ytterligare strukturer, som inte är direkt förknippade med synen, finns som utväxter av näthinnan i vissa grupper av ryggradsdjur. Hos fåglar är pektenen en kärlstruktur med komplex form som skjuter ut från näthinnan in i glaskroppen ; det tillför syre och näringsämnen till ögat och kan också hjälpa till med synen. Reptiler har en liknande, men mycket enklare, struktur.
Hos vuxna människor är hela näthinnan cirka 72 % av en sfär cirka 22 mm i diameter. Hela näthinnan innehåller cirka 7 miljoner kottar och 75 till 150 miljoner stavar. Den optiska skivan, en del av näthinnan som ibland kallas "den blinda fläcken" eftersom den saknar fotoreceptorer, är belägen vid den optiska papillen , där synnervens fibrer lämnar ögat. Det ser ut som ett ovalt vitt område på 3 mm 2 . Temporal (i tinningarnas riktning) till denna skiva är gula fläcken , i vars centrum är fovea , en grop som är ansvarig för skarp central syn, men som faktiskt är mindre känslig för ljus på grund av sin brist på stavar. Mänskliga och icke-mänskliga primater har en fovea, till skillnad från vissa fågelarter, såsom hökar, som är bifoviata, och hundar och katter, som inte har någon fovea, utan ett centralt band som kallas den visuella streaken. [ citat behövs ] Runt fovea sträcker sig den centrala näthinnan i cirka 6 mm och sedan den perifera näthinnan. Den längsta kanten av näthinnan definieras av ora serrata . Avståndet från en ora till den andra (eller gula fläcken), det känsligaste området längs den horisontella meridianen , är cirka 32 mm. [ förtydligande behövs ]
I snitt är näthinnan inte mer än 0,5 mm tjock. Den har tre lager av nervceller och två av synapser , inklusive den unika bandsynapsen . Synnerven bär ganglioncellsaxonerna till hjärnan och blodkärlen som försörjer näthinnan . Ganglioncellerna ligger innerst i ögat medan de fotoreceptiva cellerna ligger bortom. På grund av detta kontraintuitiva arrangemang måste ljus först passera genom och runt ganglioncellerna och genom näthinnan (inklusive dess kapillärkärl, ej visade) innan det når stavarna och konerna. Ljus absorberas av näthinnepigmentepitelet eller åderhinnan (som båda är ogenomskinliga).
De vita blodkropparna i kapillärerna framför fotoreceptorerna kan uppfattas som små ljusa rörliga prickar när man tittar in i blått ljus. Detta är känt som det blåa fältet entoptiska fenomenet (eller Scheerers fenomen).
Mellan ganglioncelllagret och stavarna och konerna finns två lager av neuropiler , där synaptiska kontakter skapas. Neuropillagren är det yttre plexiforma lagret och det inre plexiforma lagret . I det yttre neuropillagret ansluter stavarna och konerna till de vertikalt löpande bipolära cellerna , och de horisontellt orienterade horisontella cellerna ansluter till ganglieceller.
Den centrala näthinnan innehåller övervägande koner, medan den perifera näthinnan övervägande innehåller stavar. Totalt har näthinnan cirka sju miljoner kottar och hundra miljoner stavar. I mitten av gula fläcken är foveal gropen där kottarna är smala och långa, och arrangerade i en sexkantig mosaik , den mest täta, i motsats till de mycket fetare kottarna som ligger mer perifert i näthinnan. Vid foveal gropen förskjuts de andra retinala lagren, innan de byggs upp längs foveal sluttningen tills kanten av fovea, eller parafovea , nås, vilket är den tjockaste delen av näthinnan. Gula fläcken har en gul pigmentering, från screeningpigment, och är känd som gula fläcken. Området som omger fovea har den högsta tätheten av stavar som konvergerar på enkla bipolära celler. Eftersom dess koner har en mycket mindre konvergens av signaler, möjliggör fovea den skarpaste synen ögat kan uppnå.
Även om staven och kottarna är en slags mosaik , är överföringen från receptorer, till bipolära till ganglieceller inte direkt. Eftersom det finns cirka 150 miljoner receptorer och endast 1 miljon synnervfibrer måste konvergens och därmed blandning av signaler ske. Dessutom kan den horisontella verkan av de horisontella och amakrina cellerna tillåta ett område av näthinnan att kontrollera ett annat (t.ex. en stimulans som hämmar en annan). Denna hämning är nyckeln till att minska summan av meddelanden som skickas till de högre delarna av hjärnan. Hos vissa lägre ryggradsdjur (t.ex. duvan ) är kontrollen av meddelanden "centrifugal" - det vill säga ett lager kan kontrollera ett annat, eller högre delar av hjärnan kan driva näthinnans nervceller, men hos primater sker detta inte.
Lager avbildbara med optisk koherenstomografi
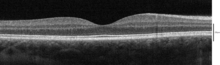
Med hjälp av optisk koherenstomografi (OCT) kan 18 lager identifieras i näthinnan. Skikten och den anatomiska korrelationen är:
Från det innersta till det yttersta är skikten som kan identifieras av ULT enligt följande:
| # | OKT-lager / konventionell etikett | Anatomiskt korrelat | Reflektivitet | Specifik anatomisk gränser? |
Ytterligare referenser |
|---|---|---|---|---|---|
| 1 | Bakre kortikala glaskroppen | Bakre kortikala glaskroppen | Hyperreflekterande | Ja | |
| 2 | Preretinalt utrymme | I ögon där glaskroppen helt eller delvis har lossnat från näthinnan är detta utrymmet som skapas mellan det bakre kortikala glaskroppens ansikte och näthinnans inre begränsande membran. | Hyporeflekterande | ||
| 3 | Internt begränsande membran (ILM) | Formad av Müllers celländfötter (oklart om det kan observeras i oktober) |
Hyperreflekterande | Nej | |
| Nervfiberlager (NFL) | Gangliecellsaxoner som färdas mot synnerven | ||||
| 4 | Ganglioncellslager (GCL) | Gangliecellkroppar (och några förskjutna amakrinceller ) | Hyporeflekterande | ||
| 5 | Inre plexiformskikt (IPL) | Synapser mellan bipolära , amakrina och ganglieceller | Hyperreflekterande | ||
| 6 | Inre kärnlager (INL) | a) Horisontella , bipolära och amakrina cellkroppar b) Müller- cellkärnor |
Hyporeflekterande | ||
| 7 | Yttre plexiformskikt (OPL) | Synapser mellan fotoreceptor , bipolära och horisontella celler | Hyperreflekterande | ||
| 8 | (Inre halvan) Henles nervfiberlager (HL) |
Fotoreceptoraxoner _ (sned orienterade fibrer; finns inte i mitten av perifer eller perifer näthinna) |
Hyporeflekterande | Nej | |
| (Ytre halvan) Yttre kärnlager (ONL) | Fotoreceptorcellkropparna _ _ | ||||
| 9 | Externt begränsande membran (ELM) | Tillverkad av zonulae fäster mellan Müller-celler och fotoreceptorinre segment | Hyperreflekterande | ||
| 10 | Myoid zone (MZ) | Den innersta delen av fotoreceptorns inre segment (IS) som innehåller:
|
Hyporeflekterande | Nej | |
| 11 | Ellipsoidzon (EZ) | Den yttersta delen av fotoreceptorns inre segment (IS) packad med mitokondrier | Mycket hyperreflekterande | Nej | |
| IS/OS-övergång eller fotoreceptorintegritetslinje (PIL) | Fotoreceptorn som förbinder flimmerhåren som överbryggar de inre och yttre segmenten av fotoreceptorcellerna. | ||||
| 12 | Fotoreceptor yttre segment (OS) | Fotoreceptorns yttre segment (OS) som innehåller skivor fyllda med opsin , molekylen som absorberar fotoner. | Hyporeflekterande | ||
| 13 | Interdigitation zone (IZ) | Toppar av RPE -cellerna som omsluter en del av konens OS. Dåligt särskiljbar från RPE. Tidigare: "kon yttre segmentspetslinje" (COST) |
Hyperreflekterande | Nej | |
| 14 | RPE /Bruchs komplex | RPE fagosomzon | Mycket hyperreflekterande | Nej | |
| RPE melanosomzon | Hyporeflekterande | ||||
| RPE mitokondrier zon + Koppling mellan RPE & Bruchs membran | Mycket hyperreflekterande | ||||
| 15 | Choriocapillaris | Tunt lager med måttlig reflektivitet i inre åderhinna | Nej | ||
| 16 | Sattlers lager | Tjockt lager av runda eller ovala hyperreflekterande profiler, med hyporeflekterande kärnor i mitten av koroiden | |||
| 17 | Hallers lager | Tjockt lager av ovala hyperreflekterande profiler, med hyporeflekterande kärnor i yttre åderhinnan | |||
| 18 | Koroidal-skleral juncture | Zon vid den yttre åderhinnan med en markant förändring i strukturen, där stora cirkulära eller äggformade profiler anligger mot en homogent område med variabel reflektivitet |
|||
Utveckling
Retinal utveckling börjar med etableringen av ögonfälten som medieras av SHH- och SIX3 -proteinerna, med efterföljande utveckling av de optiska vesiklerna som regleras av PAX6- och LHX2 -proteinerna. Rollen av Pax6 i ögonutveckling demonstrerades elegant av Walter Gehring och kollegor, som visade att ektopiskt uttryck av Pax6 kan leda till ögonbildning på Drosophila -antenner, vingar och ben. Den optiska vesikeln ger upphov till tre strukturer: den neurala näthinnan, det retinala pigmenterade epitelet och den optiska stjälken. Den neurala näthinnan innehåller retinala progenitorceller (RPC) som ger upphov till de sju celltyperna i näthinnan. Differentiering börjar med retinala ganglionceller och slutar med produktion av Muller glia. Även om varje celltyp skiljer sig från RPC:erna i en sekventiell ordning, finns det avsevärd överlappning i tidpunkten för när individuella celltyper differentierar. Ledtrådarna som bestämmer ett RPC-dottercellsöde kodas av flera transkriptionsfaktorfamiljer inklusive bHLH- och homeodomänfaktorerna .
Förutom att vägleda bestämningen av cellöde, finns det ledtrådar i näthinnan för att bestämma de dorsal-ventrala (DV) och nasal-temporala (NT) axlarna. DV-axeln etableras av en ventral till dorsal gradient av VAX2 , medan NT-axeln koordineras genom uttryck av gaffelhuvudets transkriptionsfaktorer FOXD1 och FOXG1 . Ytterligare gradienter bildas i näthinnan. Denna rumsliga fördelning kan hjälpa till med korrekt inriktning av RGC-axoner som fungerar för att upprätta den retinotopiska kartan.
Blodtillförsel
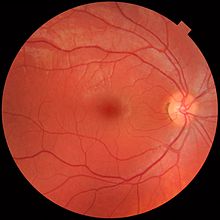
Näthinnan är stratifierad i distinkta lager, som var och en innehåller specifika celltyper eller cellulära avdelningar som har metabolism med olika näringsbehov. För att tillfredsställa dessa krav delar sig den oftalmiska artären och försörjer näthinnan via två distinkta vaskulära nätverk: det koroidala nätverket, som försörjer åderhinnan och den yttre näthinnan, och det retinala nätverket, som försörjer näthinnans inre skikt.
Cirkulationsmekanismer
Även om den inverterade näthinnan hos ryggradsdjur kan verka kontraintuitiv, är den nödvändig för att näthinnan ska fungera korrekt. Fotoreceptorskiktet måste vara inbäddat i retinalt pigmentepitel (RPE), som utför minst sju vitala funktioner, en av de mest uppenbara är att tillföra syre och andra nödvändiga näringsämnen som behövs för att fotoreceptorerna ska fungera. Dessa näringsämnen inkluderar glukos, fettsyror och retinal. Förstärkningsprocessen för däggdjursfotoreceptorer använder stora mängder energi för syn under fotopiska förhållanden (kräver mindre under scotopiska förhållanden) och kräver därför den stora tillförseln av näringsämnen som tillförs av blodkärlen i åderhinnan, som ligger utanför RPE. Åderhinnan tillför cirka 75 % av dessa näringsämnen till näthinnan och näthinnan endast 25 %.
När ljus träffar 11-cis-retinal (i diskarna i stavarna och konerna), ändras 11-cis-retinal till all-trans-retinal vilket sedan utlöser förändringar i opsinerna. Nu regenererar inte de yttre segmenten näthinnan tillbaka till cisformen när den väl har förändrats av ljus. Istället pumpas näthinnan ut till den omgivande RPE där den regenereras och transporteras tillbaka in i de yttre segmenten av fotoreceptorerna. Denna återvinningsfunktion hos RPE skyddar fotoreceptorerna mot fotooxidativ skada och tillåter fotoreceptorcellerna att ha decennier långa användbara liv.
Hos fåglar
Fågelnäthinnan saknar blodkärl, kanske för att ge obehindrat ljuspassage för att bilda bilder och därmed ge bättre upplösning. Det är därför en övervägd uppfattning att fågelnäthinnan för näring och syretillförsel är beroende av ett specialiserat organ, kallat "pecten" eller pecten oculi , beläget på den blinda fläcken eller optiska skivan. Detta organ är extremt rikt på blodkärl och tros tillföra näring och syre till fågelnäthinnan genom diffusion genom glaskroppen. Pektenen är mycket rik på alkaliskt fosfatasaktivitet och polariserade celler i sin bryggdel – båda anstår dess sekretoriska roll. Pektenceller är packade med mörka melaningranuler, som har teoretiserats för att hålla detta organ varmt med absorptionen av ströljus som faller på pektenen. Detta anses öka ämnesomsättningen hos pektenet och därigenom exportera fler näringsmolekyler för att möta näthinnans stränga energikrav under långa perioder av exponering för ljus.
Biometrisk identifiering och diagnos av sjukdom
Bifurkationerna och andra fysiska egenskaper hos det inre retinala vaskulära nätverket är kända för att variera mellan individer, och dessa individuella varianser har använts för biometrisk identifiering och för tidig upptäckt av sjukdomsdebut. Kartläggningen av vaskulära bifurkationer är ett av de grundläggande stegen i biometrisk identifiering. Resultaten av sådana analyser av strukturen av näthinneblodkärl kan utvärderas mot grunddata från vaskulära bifurkationer av näthinnefundusbilder som erhålls från DRIVE-datauppsättningen. Dessutom har klasserna av kärl i DRIVE-datauppsättningen också identifierats, och en automatiserad metod för exakt extraktion av dessa bifurkationer är också tillgänglig. Förändringar i näthinnans blodcirkulation ses med åldrande och exponering för luftföroreningar, och kan tyda på hjärt-kärlsjukdomar som högt blodtryck och åderförkalkning. Att bestämma motsvarande bredd på arterioler och venoler nära den optiska skivan är också en allmänt använd teknik för att identifiera kardiovaskulära risker.
Fungera
Näthinnan översätter en optisk bild till neurala impulser som börjar med den mönstrade exciteringen av de färgkänsliga pigmenten i dess stavar och kottar, näthinnans fotoreceptorceller . Excitationen bearbetas genom att nervsystemet och olika delar av hjärnan arbetar parallellt för att bilda en representation av den yttre miljön i hjärnan.
Konerna svarar på starkt ljus och förmedlar högupplöst färgseende under dagsljusbelysning (även kallat fotopiskt seende) . Spöresponserna är mättade vid dagsljusnivåer och bidrar inte till mönsterseende. Stavar reagerar dock på svagt ljus och förmedlar monokromatisk syn med lägre upplösning under mycket låga belysningsnivåer (kallad scotopisk syn) . Belysningen i de flesta kontorsmiljöer faller mellan dessa två nivåer och kallas mesopisk syn . På mesopiska ljusnivåer bidrar både stavarna och konerna aktivt med mönsterinformation. Vilket bidrag spöinformationen ger till mönsterseendet under dessa omständigheter är oklart.
Konernas svar på olika våglängder av ljus kallas deras spektrala känslighet. I normal mänsklig syn faller den spektrala känsligheten hos en kon in i en av tre undertyper, ofta kallade blå, gröna och röda, men mer exakt kända som korta, medelstora och långa våglängdskänsliga konsubtyper. Det är brist på en eller flera av konsubtyperna som gör att individer har brister i färgseende eller olika typer av färgblindhet . Dessa individer är inte blinda för föremål av en viss färg, men kan inte skilja mellan färger som kan urskiljas av personer med normal syn. Människor har denna trikromatiska syn , medan de flesta andra däggdjur saknar kottar med rött känsligt pigment och därför har sämre dikromatisk färgseende. Vissa djur har dock fyra spektrala undertyper, t.ex. lägger öringen till en ultraviolett undergrupp till korta, medelstora och långa undertyper som liknar människor. Vissa fiskar är också känsliga för polarisering av ljus.
I fotoreceptorerna hyperpolariserar exponering för ljus membranet i en serie av graderade förskjutningar. Det yttre cellsegmentet innehåller ett fotopigment . Inuti cellen håller de normala nivåerna av cykliskt guanosinmonofosfat (cGMP) Na+-kanalen öppen, och därför depolariseras cellen i vilande tillstånd. Fotonen gör att näthinnan som är bunden till receptorproteinet isomeriserar till transretinal . Detta gör att receptorn aktiverar flera G-proteiner . Detta gör i sin tur att Ga-subenheten av proteinet aktiverar ett fosfodiesteras (PDE6), som bryter ned cGMP, vilket resulterar i stängning av Na+ cykliska nukleotidstyrda jonkanaler (CNG). Således är cellen hyperpolariserad. Mängden neurotransmittor som frigörs minskar i starkt ljus och ökar när ljusnivåerna sjunker. Själva fotopigmentet blekas bort i starkt ljus och ersätts endast som en kemisk process, så i en övergång från starkt ljus till mörker kan ögat ta upp till trettio minuter att nå full känslighet.
När den på så sätt exciteras av ljus, skickar fotoceptorn ett proportionellt svar synaptiskt till bipolära celler som i sin tur signalerar retinala ganglieceller . Fotoreceptorerna är också tvärbundna av horisontella celler och amakrinceller , som modifierar den synaptiska signalen innan den når ganglioncellerna, varvid de neurala signalerna blandas och kombineras. Av näthinnans nervceller är det bara de retinala gangliecellerna och få amakrinceller som skapar aktionspotentialer .
I retinala ganglieceller finns det två typer av respons, beroende på cellens mottagliga fält . De receptiva fälten hos retinala ganglieceller omfattar ett centralt, ungefär cirkulärt område, där ljus har en effekt på cellens avfyring, och en ringformig omgivning, där ljus har motsatt effekt. I PÅ-celler gör en ökning av ljusintensiteten i mitten av det mottagliga fältet att avfyrningshastigheten ökar. I OFF-celler gör det att det minskar. I en linjär modell är denna svarsprofil väl beskriven av en skillnad på Gausser och är grunden för kantdetekteringsalgoritmer . Utöver denna enkla skillnad, är ganglionceller också differentierade av kromatisk känslighet och typen av rumslig summering. Celler som visar linjär rumslig summering kallas X-celler (även kallade parvocellulära, P eller midget ganglionceller), och de som visar icke-linjär summering är Y-celler (även kallade magnocellulära, M eller parasol retinala ganglionceller), även om överensstämmelsen mellan X- och Y-celler (i kattens näthinna) och P- och M-celler (i primatnäthinnan) är inte så enkelt som det en gång verkade.
Vid överföringen av visuella signaler till hjärnan, synvägen , är näthinnan vertikalt uppdelad i två, en temporal (närmare tinningen) halva och en nasal (närmare näsan). Axonerna från den nasala halvan korsar hjärnan vid den optiska chiasma för att förenas med axoner från den temporala halvan av det andra ögat innan de passerar in i den laterala genikulära kroppen .
Även om det finns mer än 130 miljoner retinala receptorer, finns det bara cirka 1,2 miljoner fibrer (axoner) i synnerven. Så en stor mängd förbehandling utförs i näthinnan. Fovea producerar den mest exakta informationen . Trots att de upptar cirka 0,01% av synfältet (mindre än 2° av synvinkeln ), är cirka 10% av axonerna i synnerven ägnade åt fovea. Upplösningsgränsen för fovea har bestämts till cirka 10 000 poäng. Informationskapaciteten uppskattas till 500 000 bitar per sekund (för mer information om bitar, se informationsteori ) utan färg eller runt 600 000 bitar per sekund inklusive färg.
Rumslig kodning
När näthinnan skickar nervimpulser som representerar en bild till hjärnan, kodar (komprimerar) den rumsligt dessa impulser för att passa den begränsade kapaciteten hos synnerven. Kompression är nödvändig eftersom det finns 100 gånger fler fotoreceptorceller än ganglionceller . Detta görs genom " dekorrelation ", som utförs av "centrum-surround-strukturerna", som implementeras av de bipolära cellerna och gangliecellerna.
Det finns två typer av center-surroundstrukturer i näthinnan – on-centers och off-centers. On-centers har ett positivt viktat centrum och en negativt viktad surround. Off-center är precis tvärtom. Positiv viktning är mer känd som excitatorisk och negativ viktning som hämmande .
Dessa centrum-surround-strukturer är inte fysiskt uppenbara, i den meningen att man inte kan se dem genom att färga vävnadsprover och undersöka näthinnans anatomi. Centrum-surroundstrukturerna är logiska (dvs. matematiskt abstrakta) i den meningen att de beror på kopplingsstyrkorna mellan bipolära celler och ganglieceller. Man tror att anslutningsstyrkan mellan celler orsakas av antalet och typerna av jonkanaler som är inbäddade i synapserna mellan de bipolära och gangliecellerna.
Centrum-surroundstrukturerna är matematiskt likvärdiga med kantdetekteringsalgoritmerna som används av datorprogrammerare för att extrahera eller förbättra kanterna i ett digitalt fotografi. Således utför näthinnan operationer på de bildrepresenterande impulserna för att förstärka kanterna på föremål inom dess synfält. Till exempel på en bild av en hund, en katt och en bil är det kanterna på dessa föremål som innehåller mest information. För att högre funktioner i hjärnan (eller i en dator för den delen) ska kunna extrahera och klassificera föremål som en hund och en katt, är näthinnan det första steget för att separera de olika föremålen inom scenen.
Som ett exempel är följande matris kärnan i en datoralgoritm som implementerar kantdetektering. Denna matris är datorns ekvivalent med centrum-surround-strukturen. I det här exemplet skulle varje ruta (element) i denna matris vara ansluten till en fotoreceptor. Fotoreceptorn i mitten är den aktuella receptorn som bearbetas. Den centrala fotoreceptorn multipliceras med viktfaktorn +1. De omgivande fotoreceptorerna är de "närmaste grannarna" till centrum och multipliceras med −1/8-värdet. Summan av alla nio av dessa element beräknas slutligen. Denna summering upprepas för varje fotoreceptor i bilden genom att flytta vänster till slutet av en rad och sedan ner till nästa rad.
| -1/8 | -1/8 | -1/8 |
| -1/8 | +1 | -1/8 |
| -1/8 | -1/8 | -1/8 |
Den totala summan av denna matris är noll, om alla insignaler från de nio fotoreceptorerna har samma värde. Nollresultatet indikerar att bilden var enhetlig (icke-föränderlig) inom denna lilla fläck. Negativa eller positiva summor betyder att bilden varierade (förändrades) inom denna lilla del av nio fotoreceptorer.
Ovanstående matris är bara en approximation av vad som verkligen händer inuti näthinnan. Skillnaderna är:
- Ovanstående exempel kallas "balanserad". Termen balanserad betyder att summan av de negativa vikterna är lika med summan av de positiva vikterna så att de tar ut perfekt. Retinala ganglionceller är nästan aldrig perfekt balanserade.
- Bordet är fyrkantigt medan mitt-surroundstrukturerna i näthinnan är cirkulära.
- Neuroner opererar på spiktåg som färdas nerför nervcellsaxoner . Datorer arbetar på ett enda flyttalstal som är i huvudsak konstant från varje ingångspixel . (Datorpixeln är i princip motsvarigheten till en biologisk fotoreceptor.)
- Näthinnan utför alla dessa beräkningar parallellt medan datorn arbetar på varje pixel en i taget. Näthinnan utför inga upprepade summeringar och skiftningar som en dator.
- Slutligen spelar de horisontella och amakrina cellerna en betydande roll i denna process, men det är inte representerat här.
Här är ett exempel på en ingångsbild och hur kantdetektering skulle ändra den.
När bilden är rumsligt kodad av centrum-surround-strukturerna skickas signalen ut längs synnerven (via gangliecellernas axoner) genom den optiska chiasmen till LGN ( lateral geniculate nucleus ). Den exakta funktionen av LGN är okänd för närvarande. Utsignalen från LGN skickas sedan till baksidan av hjärnan. Närmare bestämt "strålar" utsignalen från LGN ut till V1 primära visuella cortex .
Förenklat signalflöde: Fotoreceptorer → Bipolär → Ganglion → Chiasm → LGN → V1 cortex
Klinisk signifikans
Det finns många ärftliga och förvärvade sjukdomar eller störningar som kan påverka näthinnan. Några av dem inkluderar:
- Retinitis pigmentosa är en grupp genetiska sjukdomar som påverkar näthinnan och orsakar förlust av mörkerseende och perifert syn.
- Makuladegeneration beskriver en grupp sjukdomar som kännetecknas av förlust av central syn på grund av död eller försämring av cellerna i gula fläcken .
- Konstångsdystrofi (CORD) beskriver ett antal sjukdomar där synförlust orsakas av försämring av kottarna och /eller stavarna i näthinnan.
- Vid näthinneseparation lossnar näthinnan från baksidan av ögongloben. Tändpunktur är en förlegad behandlingsmetod. Termen näthinneavlossning används för att beskriva en separation av den neurosensoriska näthinnan från näthinnans pigmentepitel . Det finns flera moderna behandlingsmetoder för att fixera en näthinneavlossning: pneumatisk retinopexi , skleralt spänne , kryoterapi , laserfotokoagulation och pars plana vitrektomi .
- Både högt blodtryck och diabetes mellitus kan orsaka skador på de små blodkärlen som försörjer näthinnan, vilket leder till hypertensiv retinopati och diabetisk retinopati .
- Retinoblastom är en cancer i näthinnan.
- Näthinnesjukdomar hos hundar inkluderar retinal dysplasi , progressiv retinal atrofi och plötslig förvärvad retinal degeneration .
- Lipaemia retinalis är ett vitt utseende på näthinnan och kan uppstå genom lipidavlagring vid lipoproteinlipasbrist .
- Näthinneavlossning . Den neurala näthinnan lossnar då och då från pigmentepitelet. I vissa fall är orsaken till sådan lösgöring skada på ögongloben som gör att vätska eller blod kan samlas mellan neurala näthinnan och pigmentepitelet. Avlossning orsakas ibland av sammandragning av fina kollagenfibriller i glaskroppen, som drar områden av näthinnan mot det inre av jordklotet.
- Nattblindhet : Nattblindhet förekommer hos alla personer med allvarlig A-vitaminbrist. Anledningen till detta är att utan vitamin A är mängden retinal och rhodopsin som kan bildas kraftigt deprimerad. Detta tillstånd kallas nattblindhet eftersom mängden ljus tillgängligt på natten är för lite för att tillåta adekvat syn hos personer med vitamin A-brist.
Dessutom har näthinnan beskrivits som ett "fönster" in i hjärnan och kroppen, med tanke på att avvikelser som upptäcks genom en undersökning av näthinnan kan upptäcka både neurologiska och systemiska sjukdomar.
Diagnos
Ett antal olika instrument finns tillgängliga för diagnos av sjukdomar och störningar som påverkar näthinnan. Oftalmoskopi och ögonbottenfotografering har länge använts för att undersöka näthinnan. På senare tid adaptiv optik använts för att avbilda enskilda stavar och kottar i den levande mänskliga näthinnan, och ett företag baserat i Skottland har konstruerat teknik som gör att läkare kan observera hela näthinnan utan något obehag för patienterna.
Elektroretinogrammet används för att icke-invasivt mäta näthinnans elektriska aktivitet, som påverkas av vissa sjukdomar . En relativt ny teknik, som nu blir allmänt tillgänglig, är optisk koherenstomografi (OCT). Denna icke-invasiva teknik gör att man kan erhålla ett 3D- volymetriskt eller högupplöst tvärsnittstomogram av de fina strukturerna i näthinnan, med histologisk kvalitet. Näthinnekärlanalys är en icke-invasiv metod för att undersöka de små artärerna och venerna i näthinnan som gör det möjligt att dra slutsatser om morfologin och funktionen hos små kärl på andra ställen i människokroppen. Det har etablerats som en prediktor för hjärt-kärlsjukdom och verkar ha, enligt en studie publicerad 2019, potential för tidig upptäckt av Alzheimers sjukdom.
Behandling
Behandlingen beror på arten av sjukdomen eller störningen.
Vanliga behandlingsformer
Följande är vanligtvis behandlingsmetoder för näthinnesjukdom:
- Intravitreal medicinering , såsom anti-VEGF eller kortikosteroidmedel
- Vitreoretinal kirurgi
- Användning av kosttillskott
- Modifiering av systemiska riskfaktorer för retinal sjukdom
Mindre vanliga behandlingsmetoder
Retinal genterapi
Genterapi lovar som en potentiell väg för att bota ett brett spektrum av näthinnesjukdomar. Detta innebär att man använder ett icke-infektiöst virus för att överföra en gen till en del av näthinnan. Rekombinanta adenoassocierade virus (rAAV) vektorer har ett antal egenskaper som gör dem idealiska för retinal genterapi, inklusive brist på patogenicitet, minimal immunogenicitet och förmågan att transducera postmitotiska celler på ett stabilt och effektivt sätt. rAAV-vektorer används alltmer för sin förmåga att förmedla effektiv transduktion av retinalt pigmentepitel (RPE), fotoreceptorceller och retinala ganglieceller . Varje celltyp kan målinriktas specifikt genom att välja lämplig kombination av AAV- serotyp , promotor och intraokulärt injektionsställe.
Flera kliniska prövningar har redan rapporterat positiva resultat med användning av rAAV för att behandla Lebers medfödda amauros , vilket visar att behandlingen var både säker och effektiv. Det förekom inga allvarliga biverkningar och patienterna i alla tre studierna visade förbättring av sin synfunktion mätt med ett antal metoder. Metoderna som användes varierade mellan de tre försöken, men omfattade både funktionella metoder som synskärpa och funktionell rörlighet samt objektiva mått som är mindre mottagliga för bias, såsom pupillens förmåga att reagera på ljus och förbättringar av funktionell MR. Förbättringar bibehölls på lång sikt, med patienter som fortsatte att må bra efter mer än 1,5 år.
Den unika arkitekturen hos näthinnan och dess relativt immunprivilegierade miljö hjälper denna process. Tight junctions som bildar blodretinalbarriären separerar det subretinala utrymmet från blodtillförseln, vilket skyddar det från mikrober och de flesta immunförmedlade skador, och förbättrar dess potential att svara på vektormedierade terapier. Den mycket kompartmenterade anatomin i ögat underlättar exakt leverans av terapeutiska vektorsuspensioner till specifika vävnader under direkt visualisering med hjälp av mikrokirurgiska tekniker. I den skyddade miljön av näthinnan kan AAV-vektorer upprätthålla höga nivåer av transgenexpression i retinalt pigmenterat epitel (RPE), fotoreceptorer eller ganglieceller under långa tidsperioder efter en enda behandling. Dessutom kan ögat och synsystemet rutinmässigt och enkelt övervakas för synfunktion och strukturella förändringar i näthinnan efter injektioner med icke-invasiv avancerad teknologi, såsom synskärpa, kontrastkänslighet, fundus autofluorescens ( FAF), mörkeranpassade syntrösklar , vaskulära diametrar, pupillometri, elektroretinografi (ERG), multifokal ERG och optisk koherenstomografi (OCT).
Denna strategi är effektiv mot ett antal retinala sjukdomar som har studerats, inklusive neovaskulära sjukdomar som är kännetecken för åldersrelaterad makuladegeneration , diabetisk retinopati och retinopati av prematuritet . Eftersom regleringen av vaskularisering i den mogna näthinnan involverar en balans mellan endogena positiva tillväxtfaktorer , såsom vaskulär endotelial tillväxtfaktor (VEGF) och hämmare av angiogenes , såsom pigmentepitelhärledd faktor ( PEDF ), rAAV-medierat uttryck av PEDF, angiostatin och den lösliga VEGF-receptorn sFlt-1, som alla är antiangiogena proteiner, har visat sig minska avvikande kärlbildning i djurmodeller. Eftersom specifika genterapier inte lätt kan användas för att behandla en betydande del av patienter med retinal dystrofi, finns det ett stort intresse för att utveckla en mer allmänt användbar överlevnadsfaktorterapi. Neurotrofa faktorer har förmågan att modulera neuronal tillväxt under utveckling för att bibehålla befintliga celler och för att möjliggöra återhämtning av skadade neuronala populationer i ögat. AAV-kodande neurotrofiska faktorer såsom fibroblasttillväxtfaktor (FGF) familjemedlemmar och GDNF skyddade antingen fotoreceptorer från apoptos eller bromsade celldöd.
Organtransplantation Transplantation av näthinnor har försökts, men utan större framgång. Vid MIT , University of Southern California, RWTH Aachen University och University of New South Wales är en "konstgjord näthinna" under utveckling: ett implantat som kommer att kringgå fotoreceptorerna i näthinnan och stimulera de anslutna nervcellerna direkt, med signaler från en digitalkamera.
Historia
Omkring 300 f.Kr. identifierade Herophilos näthinnan från dissektioner av kadaverögon . Han kallade det arachnoidlagret , från dess likhet med ett spindelnät, och retiform , från dess likhet med ett gjutnät. Termen arachnoid kom att hänvisa till ett lager runt hjärnan; termen retiform kom att syfta på näthinnan .
Mellan 1011 och 1021 e.Kr. publicerade Ibn Al-Haytham många experiment som visar att syn uppstår från ljus som reflekteras från föremål in i ögat. Detta överensstämmer med intromissionsteorin och mot emissionsteorin , teorin att syn uppstår från strålar som sänds ut av ögonen. Ibn Al-Haytham bestämde sig dock för att näthinnan inte kunde vara ansvarig för synens början eftersom bilden som bildades på den var inverterad. Istället bestämde han sig för att det måste börja vid linsens yta.
År 1604 utarbetade Johannes Kepler ögats optik och bestämde att näthinnan måste vara där synen börjar. Han lämnade upp till andra forskare att förena den inverterade näthinnebilden med vår uppfattning om världen som upprätt.
År 1894 publicerade Santiago Ramón y Cajal den första stora karaktäriseringen av retinala nervceller i Retina der Wirbelthiere ( Retina of vertebrates) .
George Wald , Haldan Keffer Hartline och Ragnar Granit vann 1967 Nobelpriset i fysiologi eller medicin för sin vetenskapliga forskning om näthinnan.
En nyligen genomförd studie från University of Pennsylvania beräknade att den ungefärliga bandbredden för mänskliga näthinnor är 8,75 megabit per sekund, medan ett marsvins näthinneöverföringshastighet är 875 kilobit per sekund.
MacLaren & Pearson och kollegor vid University College London och Moorfields Eye Hospital i London, 2006, visade att fotoreceptorceller kunde transplanteras framgångsrikt i musens näthinna om donatorceller var i ett kritiskt utvecklingsstadium. Nyligen visade Ader och kollegor i Dublin, med hjälp av elektronmikroskopet, att transplanterade fotoreceptorer bildade synaptiska förbindelser.
2012 lanserade Sebastian Seung och hans laboratorium vid MIT EyeWire , ett Citizen science- spel online där spelare spårar nervceller i näthinnan. Målet med EyeWire-projektet är att identifiera specifika celltyper inom de kända breda klasserna av retinala celler, och att kartlägga sambanden mellan neuroner i näthinnan, vilket kommer att hjälpa till att avgöra hur synen fungerar.
Ytterligare bilder
Se även
- Adenoassocierat virus och genterapi av den mänskliga näthinnan
- Charles Schepens – "fadern till modern näthinnekirurgi"
- Evolution av ögat
- Duplex näthinna
- Retinal scan
- retinal venocklusion
- Lista över xantomvarianter associerade med subtyper av hyperlipoproteinemi
- Rhodopsin
- Uthållighet av vision
Vidare läsning
- S. Ramón y Cajal , Histologie du Système Nerveux de l'Homme et des Vertébrés , Maloine, Paris, 1911.
- Rodieck RW (1965). "Kvantitativ analys av kattens retinala ganglioncellsvar på visuella stimuli". Vision Res . 5 (11): 583–601. doi : 10.1016/0042-6989(65)90033-7 . PMID 5862581 .
- Wandell, Brian A. (1995). Grunder för vision . Sunderland, Mass: Sinauer Associates. ISBN 978-0-87893-853-7 .
- Wässle H, Bojkott BB (1991). "Funktionell arkitektur hos däggdjursnäthinnan". Physiol. Rev. _ 71 (2): 447–480. doi : 10.1152/physrev.1991.71.2.447 . PMID 2006220 .
- Schulz HL, Goetz T, Kaschkoetoe J, Weber BH (2004). "Retinomen - Definierar ett referenstranskriptom av det vuxna däggdjursnäthinnan/retinala pigmentepitelet" . BMC Genomics (om ett transkriptom för ögonfärg). 5 (1): 50. doi : 10.1186/1471-2164-5-50 . PMC 512282 . PMID 15283859 .
- Dowling, John (2007). "Retina" . Scholarpedia . 2 (12): 3487. Bibcode : 2007SchpJ...2.3487D . doi : 10.4249/scholarpedia.3487 .
externa länkar
- Histology of the Eye , redigerad av William Krause, Dept. Pathology and Anatomical science, University of Missouri School of Medicine
- Eye, Brain, and Vision – onlinebok – av David Hubel
- Kolb, H., Fernandez, E., & Nelson, R. (2003). Webvision: Den neurala organisationen av ryggradsnäthinnan . Salt Lake City, Utah: John Moran Eye Center, University of Utah . Hämtad 22 juli 2014.
- Demo: Artificial Retina , MIT Technology Review, september 2004. Rapporter om implantatforskning på Technology Review
- Framgångsrik fotoreceptortransplantation , MIT Technology Review, november 2006. Hur stamceller kan återställa synen Technology Review
- Australian Vision Prosthesis Group Arkiverad 12 augusti 2011 på Wayback Machine , Graduate School of Biomedical Engineering, University of New South Wales
- RetinaCentral , genetik och sjukdomar i den mänskliga näthinnan vid universitetet i Würzburg
- Bild på näthinnelager. NeuroScience 2nd Ed vid United States National Library of Medicine
- Jeremy Nathans seminarier: "The Vertebrate Retina: Structure, Function and Evolution"
- Retina – Cellcentrerad databas
- Histologibild: 07901loa – Histology Learning System vid Boston University
- MedlinePlus Encyclopedia : 002291