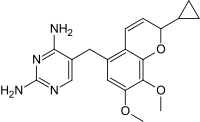
Iclaprim
 | |
| Kliniska data | |
|---|---|
Administreringsvägar _ |
intravenös |
| ATC-kod | |
| Rättslig status | |
| Rättslig status |
|
| Identifierare | |
| |
| CAS-nummer | |
| PubChem CID | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| CompTox Dashboard ( EPA ) | |
| ECHA InfoCard | 100.130.860 |
| Kemiska och fysikaliska data | |
| Formel | C19H22N4O3 _ _ _ _ _ _ _ |
| Molar massa | 354,410 g·mol -1 |
| 3D-modell ( JSmol ) | |
| Chiralitet | Racemisk blandning |
| |
| |
|
| |
Iclaprim är en antibiotisk läkemedelskandidat som är aktiv mot grampositiva organismer . Det administreras intravenöst.
In vitro är iklaprim aktivt mot meticillinresistenta Staphylococcus aureus (MRSA), vankomycinresistenta Staphylococcus aureus (VRSA), stammar av Streptococcus pneumoniae som är resistenta mot flera vanliga antibiotika och vissa gramnegativa bakterier . Det är av typen diaminopyrimidin- dihydrofolatreduktas (DHFR) -hämmande .
Historia
Iclaprim är en optimerad analog av trimetoprim som upptäcktes av forskare vid Roche . Arpida drevs ut från Roche 1998 och förvärvade iclaprim från Roche 2001. Arpida hade ett börsnoterat erbjudande på den schweiziska börsen 2005.
Arpida genomförde två kliniska fas III -studier för komplicerade hud- och hudstrukturinfektioner som avslutades 2008, men som från 2017 inte hade publicerats i den medicinska litteraturen . En ny läkemedelsansökan lämnades in till United States Food and Drug Administration baserat på dessa prövningar, och avslogs på grund av misslyckande med att visa icke-underlägsenhet och på grund av säkerhetsproblem, särskilt läkemedelsinducerad QT-förlängning . FDA:s rådgivande kommitté sa att läkemedlet "inte borde utvecklas vidare" baserat på de resultat som presenterades. En parallell ansökan om marknadsföringsgodkännande till Europeiska läkemedelsmyndigheten drogs tillbaka 2009; i tillkännagivandet av tillbakadragandet sade EMA att det inte fanns tillräckliga data från kliniska studier för att motivera den dosering som föreslagits av företaget och att resistens mot läkemedlet redan hade setts i data från kliniska prövningar.
Arpida kollapsade efter avslaget från FDA och EMA:s tillbakadragande. Arpida och det privatägda schweiziska företaget Evolva började diskutera ett förvärv av Arpida av Evolva, vilket skulle göra det möjligt för Evolva att bli börsnoterad via en omvänd fusion i september 2009. Arpida sålde av iclaprim till Acino Pharma i november 2009, och i december 2009, Arpida och Evolva slutförde sin transaktion.
Acino sålde rättigheterna till iclaprim, dess data och regulatoriska anmälningar och tillverkade läkemedel till en grupp som heter Life Sciences Management Group i Bethesda, Maryland, i september 2013 och det företaget överlät sina rättigheter till ett företag som heter Nuprim, som hade bildats av tidigare verkställande direktör, chief science officer och amerikansk agent för Arpida 2014. I december 2014 undertecknade Motif BioSciences och Nuprim ett avtal som tillåter Motif att förvärva iclaprim-tillgångarna, och transaktionen slutfördes i april 2015. 2015, FDA beviljats kvalificerad infektionssjukdomsproduktstatus för iklaprim.
I september 2017 beviljade FDA särläkemedelsstatus till iclaprim för behandling av Staphylococcus aureus lunginfektioner hos personer med cystisk fibros. Iclaprim var inte sämre än vankomycin när det studerades i två fas III-studier av akuta hud- och hudstrukturinfektioner publicerade 2018. I februari 2019 är det fortfarande inte godkänt.
Kemi
Iclaprim innehåller ett stereocenter och är ett racemat , en 1:1 blandning av ( R )- och ( S ) -enantiomerer :
| Enantiomerer av iklaprim | |
|---|---|
 CAS-nummer: 1208116-65-7 |
 CAS-nummer: 1208116-66-8 |
Namn
Under dess utveckling har andra namn för läkemedlet inkluderat AR-100, MTF-100, RO-48-2622 och varumärket Mersarex. Det fick sitt INN-namn 2003.
externa länkar
Vidare läsning
- Schneider P, Hawser S, Islam K (december 2003). "Iclaprim, en ny diaminopyrimidin med potent aktivitet på trimetoprimkänsliga och resistenta bakterier". Bioorg Med Chem Lett . 13 (23): 4217–21. doi : 10.1016/j.bmcl.2003.07.023 . PMID 14623005 .