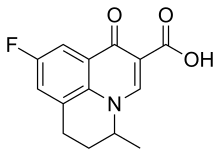
Flumequine
 | |
| Kliniska data | |
|---|---|
| Andra namn | 9-fluor-6,7-dihydro-5-metyl-l-oxo-lH , 5H - benso[ ij ]-kinolizin-2-karboxylsyra |
| AHFS / Drugs.com | Internationella läkemedelsnamn |
| ATC-kod | |
| Rättslig status | |
| Rättslig status |
|
| Farmakokinetiska data | |
| Exkretion | urin och avföring |
| Identifierare | |
| |
| CAS-nummer | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| CompTox Dashboard ( EPA ) | |
| ECHA InfoCard | 100.050.857 |
| Kemiska och fysikaliska data | |
| Formel | C 14 H 12 F N O 3 |
| Molar massa | 261,252 g·mol -1 |
| 3D-modell ( JSmol ) | |
| Smältpunkt | 253 till 255 °C (487 till 491 °F) |
| |
| |
|
| |
Flumequine är ett syntetiskt fluorokinolonantibiotikum som används för att behandla bakterieinfektioner . Det är en första generationens antibakteriell fluorokinolon som har tagits bort från klinisk användning och som inte längre marknadsförs. Godkännandet för försäljning av flumequine har tillfälligt upphävts i hela EU. Det dödar bakterier genom att störa enzymerna som får DNA att varva ner och duplicera. Flumequine användes inom veterinärmedicin för behandling av tarminfektioner (alla infektioner i tarmkanalen), samt för att behandla nötkreatur, svin, kycklingar och fiskar, men endast i ett begränsat antal länder. Det användes ibland i Frankrike (och några andra europeiska länder) för att behandla urinvägsinfektioner under handelsnamnet Apurone. Detta var dock en begränsad indikation eftersom endast minimala serumnivåer uppnåddes.
Historia
Den första kinolonen som användes var nalidixinsyra (marknadsfördes i många länder som Negram) följt av fluorokinolonflumekin. Första generationens fluorokinolonmedel, såsom flumequine, hade dålig distribution i kroppsvävnaderna och begränsad aktivitet. Som sådana användes de främst för behandling av urinvägsinfektioner. Flumequine (bensokinolizin) patenterades första gången 1973 (tyskt patent) av Rikker Labs. Flumequine är en känd antimikrobiell förening som beskrivs och skyddas i US Pat. nr. 3 896 131 (exempel 3), 22 juli 1975. Flumequine är den första kinolonföreningen med en fluoratom i C6-positionen av den relaterade kinolonbasmolekylära strukturen. Även om detta var den första fluorokinolonen, förbises den ofta när man klassificerar läkemedlen inom denna klass efter generationer och utesluts från en sådan lista.
Även om flumequine användes ofta för att behandla husdjur och ibland husdjur, användes flumequine också för att behandla urinvägsinfektioner hos människor. Flumequine, användes tillfälligt för att behandla urinvägsinfektioner tills okulär toxicitet rapporterades. samt leverskador och anafylaktisk chock.
2008 begärde USA:s livsmedels- och läkemedelsmyndighet (FDA) att alla bipacksedlar för kinolon/fluorokinolonläkemedel skulle innehålla en varning i svart ruta om risken för spontana senorrupturer, vilket skulle ha inkluderat flumequin. FDA begärde också att tillverkarna skulle skicka ut Dear Doctor Letters angående denna nya varning. Sådana senproblem har också förknippats med flumequine.
Läkemedelsrester
Användningen av flumequine i matdjur hade väckt stor debatt. Betydande och skadliga rester av kinoloner har hittats hos djur som behandlats med kinoloner och senare slaktats och sålts som livsmedel. Det har funnits en betydande oro angående mängden flumekinrester som finns i livsmedelsdjur som fisk, fjäderfä och nötkreatur. År 2003 drog FAO/WHO:s gemensamma kommitté för livsmedelstillsatser (JECFA) tillbaka de maximala resthalterna (MRL) för flumequine och karbadox baserat på bevis som visar att båda är direktverkande genotoxiska cancerframkallande ämnen, varför kommittén inte kunde fastställa ett acceptabelt dagligt intag (ADI) ) för mänsklig exponering för sådana rester. Därefter, 2006, återupprättade JEFCA ADI efter att ha fått lämpliga bevis och gränsvärden specificerades på nytt. JECFA:s roll är att utvärdera toxikologi, resthaltskemi och relaterad information och ge rekommendationer för acceptabla dagliga intag (ADI) nivåer och maximala resthalter (MRL). Vid sin 16:e session, som hölls i maj 2006, begärde kommittén för rester av veterinärmedicinska läkemedel i livsmedel (CCRVDF) information om registrerad användning av flumequine. Eftersom CCVDF inte fick någon information om de registrerade användningarna av flumequine som de hade begärt, gick kommittéledamöterna med på att avbryta arbetet med gränsvärdena för flumequine i räkor.
Licensierad användning
Urinvägsinfektioner (veterinär och människa)
Tillgänglighet
Veterinär användning:
- Lösning; Oral; 20 % (endast receptbelagda)
- Lösning; Oral; 10% (endast recept)
Mänsklig användning:
- Läsplatta; Oral; Flumequine 400 mg (upphört)
Verkningssätt
Flumequine är en medlem av kinolonantibiotikafamiljen , som är aktiva mot både grampositiva och gramnegativa bakterier. Det fungerar genom att hämma DNA-gyras , ett typ II- topoisomeras , och topoisomeras IV, enzymer som är nödvändiga för att separera bakteriellt DNA, och därigenom hämma celldelningen.
Denna mekanism kan också påverka replikation av däggdjursceller. I synnerhet uppvisar vissa kongener av denna läkemedelsfamilj (till exempel de som innehåller C-8-fluoret), hög aktivitet inte bara mot bakteriella topoisomeraser utan också mot eukaryota topoisomeraser och är toxiska för odlade däggdjursceller och in vivo- tumörmodeller .
Även om kinoloner är mycket toxiska för däggdjursceller i kultur, är dess mekanism för cytotoxisk verkan inte känd. Kinolon-inducerad DNA-skada rapporterades första gången 1986 (Hussy et al.).
Nyligen genomförda studier har visat en korrelation mellan kinolonernas cytotoxicitet hos däggdjursceller och induktionen av mikrokärnor.
Som sådana kan vissa fluorokinoloner orsaka skada på kromosomen i eukaryota celler.
Det fortsätter att finnas avsevärd debatt om huruvida denna DNA-skada ska anses vara en av verkningsmekanismerna för de allvarliga biverkningar som vissa patienter upplever efter fluorokinolonbehandling.
Negativa reaktioner
Flumequine var associerat med allvarlig okulär toxicitet, vilket uteslöt användningen av det hos mänskliga patienter. Läkemedelsinducerad tandsten (njursten) har också associerats med sådan terapi. Anafylaktisk chock inducerad av flumequinterapi har också associerats med dess användning. Anafylaktoida reaktioner som chock, urtikaria och Quinckes ödem har rapporterats i allmänhet uppträda inom två timmar efter att ha tagit den första tabletten. Det fanns arton rapporter listade i WHO-filen 1996. Som med alla läkemedel inom denna klass kan flumequinbehandling resultera i allvarliga reaktioner i det centrala nervsystemet (CNS), fototoxicitet som resulterar i hudreaktioner som erytem, klåda, urtikaria och svåra utslag, gastrointestinala och neurologiska störningar.
Läkemedelsinteraktioner
Flumekin visade sig inte ha någon effekt på teofyllins farmakokinetik.
Kemi
Flumequine är en 9-fluoro-6,7-dihydro-5-metyl-l-oxo-lH,5H-benso[ij]kinolizin-2-karboxylsyra. Molekylformeln är C14H12FNO3 . _ _ _ Det är ett vitt pulver, luktfritt, smaklöst, olösligt i vatten men lösligt i organiskt lösningsmedel.
Farmakokinetik
Flumekin anses vara väl absorberat och utsöndras i urinen och avföringen som glukuronidkonjugaten av moderläkemedlet och 7-hydroxiflumekin. Det elimineras inom 168 timmar efter dosering. Studier rörande kalvlevern visade dock ytterligare oidentifierade rester, av vilka en ny metabolit, ml, representerade den huvudsakliga enskilda metaboliten 24 timmar efter den sista dosen och vid alla efterföljande tidpunkter. Metaboliten ml, som inte uppvisade någon antimikrobiell aktivitet, var närvarande i både fria och proteinbundna fraktioner. Den huvudsakliga återstoden som hittades i ätbara vävnader hos får, grisar och kycklingar var moderläkemedlet tillsammans med mindre mängder av 7-hydroxi-metaboliten. Den enda påvisade restprodukten i öring var moderläkemedlet.