Talimogene laherparepvec
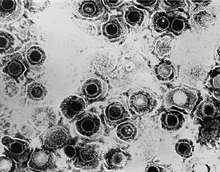 Transmissionselektronmikrofotografi av ett omodifierat herpes simplex-virus
| |
| Genterapi | |
|---|---|
| Målgen | GM-CSF |
| Vektor | Herpes simplex virus 1 |
| Kliniska data | |
| Handelsnamn | T-Vec, Imlygic, Oncovex |
| Andra namn | T-Vec |
| AHFS / Drugs.com | Monografi |
| MedlinePlus | a616006 |
| Licensdata |
|
Graviditetskategori _ |
|
Administreringsvägar _ |
Injektion |
| ATC-kod | |
| Rättslig status | |
| Rättslig status |
|
| Identifierare | |
| CAS-nummer | |
| DrugBank | |
| ChemSpider |
|
| UNII | |
| KEGG | |
Talimogene laherparepvec , som säljs under varumärket Imlygic , är ett biofarmaceutiskt läkemedel som används för att behandla melanom som inte kan opereras; det injiceras direkt i en undergrupp av lesioner som genererar ett systemiskt immunsvar mot mottagarens cancer. Den sista fyraårsanalysen från den pivotala fas 3-studien där TVEC godkändes av FDA visade en svarsfrekvens på 31,5 % med en 16,9 % fullständig respons (CR). Det fanns också en betydande och statistiskt signifikant överlevnadsfördel hos patienter med tidigare metastaserad sjukdom (stadier IIIb-IVM1a) och hos patienter som inte tidigare fått systemisk behandling för melanom. Gruppen i det tidigare stadiet hade en minskning av risken för dödsfall med cirka 50 % med en av fyra patienter som verkade ha uppfyllt, eller vara nära att nå, den medicinska definitionen av botemedel. Verklig användning av talimogene laherparepvec har visat svarsfrekvenser på upp till 88,5 % med CR-frekvenser på upp till 61,5 %.
Ungefär hälften av personer som behandlades med talimogene laherparepvec i kliniska prövningar upplevde trötthet och frossa; cirka 40 % hade feber, cirka 35 % hade illamående och cirka 30 % hade influensaliknande symtom samt smärta vid injektionsstället. Reaktionerna var milda till måttliga i svårighetsgrad; 2% av människorna hade allvarliga reaktioner och dessa var vanligtvis cellulit .
Talimogene laherparepvec är ett genmanipulerat herpesvirus (ett onkolytiskt herpesvirus) . Två gener togs bort – en som stänger av en enskild cells försvar och en annan som hjälper viruset att undvika immunförsvaret – och en gen för humant GM-CSF lades till. Läkemedlet verkar genom att replikera i cancerceller, vilket får dem att spricka; den designades också för att stimulera ett immunsvar mot patientens cancer, vilket har visats av flera data, inklusive regression av tumörer som inte har injicerats med talimogene laherparepvec.
Läkemedlet skapades och utvecklades initialt av BioVex, Inc. och fortsattes av Amgen , som förvärvade BioVex 2011. Det var en av de första onkolytiska immunterapierna som godkändes globalt; den godkändes i USA i oktober 2015 och godkändes i Europa i december 2015.
Medicinsk användning
Talimogene laherparepvec levereras genom att injicera det direkt i tumörer, vilket skapar ett systemiskt antitumörimmunsvar.
I USA är talimogene laherparepvec FDA-godkänd för att behandla melanompatienter i stadium IIIb-IVM1c för vilka kirurgisk ingrepp inte är lämplig och med tumörer som kan injiceras direkt; den EMA-godkända populationen i Europa är för steg IIIb-IVM1a.
Talimogene laherparepvec har visat sig förlänga överlevnaden hos patienter med stadium IIIb-IVM1a melanom och patienter som inte tidigare fått systemisk behandling för melanom.
Skadliga effekter
Ungefär hälften av personer som behandlades med talimogene laherparepvec i kliniska prövningar upplevde trötthet och frossa; cirka 40 % hade feber, cirka 35 % hade illamående och cirka 30 % hade influensaliknande symtom samt smärta vid injektionsstället. Reaktionerna var milda till måttliga i svårighetsgrad; 2% av människorna hade allvarliga reaktioner och dessa var vanligtvis cellulit .
Mer än 10 % av personerna hade ödem , huvudvärk, hosta, kräkningar, diarré, förstoppning, muskelsmärta eller ledvärk. Mellan 1 % och 10 % utvecklade munsår, smärta eller infektion i lesionen, anemi , immunförmedlade händelser (som vaskulit, lunginflammation, förvärrad psoriasis, glomerulonefrit och vitiligo ), uttorkning, förvirring, ångest, depression, yrsel, sömnlöshet, öronvärk , snabb hjärtklappning , djup ventrombos , högt blodtryck, rodnad, andnöd vid träning, halsont, symtom på förkylning, magsmärtor , ryggsmärtor, ljumsksmärta, viktminskning eller sipprar från injektionsstället.
Farmakologi
Talimogene laherparepvec tas upp av normala celler och cancerceller som vildtypsherpes simplex-viruset , det elimineras på samma sätt.
Mekanism
Talimogene laherparepvec förstör direkt de cancerceller som den infekterar, vilket inducerar ett systemiskt immunsvar mot patientens cancer.
Viruset invaderar både cancerceller och friska celler, men det kan inte replikera produktivt i frisk vävnad eftersom det saknar infekterat cellprotein 34.5 (ICP34.5). När celler infekteras med ett virus stängs de av och dör, men ICP34.5 blockerar denna stressreaktion , vilket gör att viruset kan kapa cellens översättningsmaskineri för att replikera sig själv. Ett herpesvirus som saknar genen som kodar för ICP34.5 kan inte replikera i normal vävnad. Men i många cancerceller är stressresponsen redan störd, så ett virus som saknar ICP34.5 kan fortfarande replikera i tumörer. Efter att viruset har replikerats många gånger, sväller cellen och spricker slutligen, dödar cellen och frigör kopiorna av viruset, som sedan kan infektera närliggande celler.
Medan talimogene laherparepvec använder cellens översättningsmaskineri för att replikera, använder den det också för att få cellen att skapa GM-CSF . GM-CSF utsöndras eller frisätts när cancercellen spricker och attraherar dendritiska celler till platsen, som plockar upp tumörantigener, bearbetar dem och sedan presenterar dem på sin yta för cytotoxiska (mördar) T-celler som i sin tur sätter igång en immunsvar.
Sammansättning
Talimogene laherparepvec är ett biofarmaceutiskt läkemedel; det är ett onkolytiskt herpesvirus som skapades genom att genetiskt modifiera en stam av herpes simplex virus 1 (HSV-1) som tagits från en person infekterad med viruset, snarare än en laboratoriestam. Båda kopiorna av den virala genen som kodar för ICP34.5 raderades och ersattes med genen som kodar för humant GM-CSF , och genen som kodar för ICP47 togs bort. I vilda herpesvirus undertrycker ICP47 immunsvaret mot viruset; det togs bort eftersom läkemedlet designades med avsikten att aktivera immunsystemet.
Historia
Det första onkolytiska viruset som godkändes av en tillsynsmyndighet var ett genetiskt modifierat adenovirus vid namn H101 av Shanghai Sunway Biotech. Det fick regulatoriskt godkännande 2005 från Kinas statliga livsmedels- och läkemedelsadministration (SFDA) för behandling av huvud- och halscancer. Talimogene laherparepvec är världens första godkända onkolytiska immunterapi, dvs den designades också för att ge systemiska antitumöreffekter genom induktion av ett antitumörimmunsvar. [ citat behövs ]
Talimogene laherparepvec skapades och utvecklades initialt av BioVex, Inc. under varumärket OncoVEX GM-CSF . Utvecklingen fortsatte av Amgen , som förvärvade BioVex 2011. BioVex grundades 1999, baserat på forskning av Robert Coffin vid University College London , och flyttade sitt huvudkontor till Woburn, Massachusetts 2005, vilket lämnade ungefär hälften av sina anställda i Storbritannien.
Den kliniska fas II-studien vid melanom publicerades 2009 och fas III-studien publicerades 2013.
Talimogene laherparepvec godkändes av US Food and Drug Administration för att behandla melanom i oktober 2015. Det var det första godkännandet av ett onkolytiskt virus och det första godkännandet av en genterapi i väst. Det godkändes av Europeiska läkemedelsmyndigheten i december samma år.
Samhälle och kultur
Ekonomi
Amgen uppskattade att talimogene laherparepvec skulle kosta 65 000 USD per patient vid den tidpunkt då det godkändes.
Internationell press
The Conversation (webbplats) som har flerspråkiga artiklar, publicerade på franska och spanska i oktober 2022 följande artikel av Arthur Battistoni och Françoise Debierre-Grockiego båda från University of Tours
- Immunterapi en parasit hos hundar som hjälper till att bekämpa obotlig hudcancer
Forskning
Från och med 2016 har talimogene laherparepvec studerats i tidiga kliniska prövningar vid pankreascancer , mjukdelssarkom och skivepitelcancer i huvud och hals ; det hade också testats i kombination med checkpoint-hämmarna ipilimumab och pembrolizumab .
externa länkar
- "Talimogene laherparepvec" . Läkemedelsinformationsportal . US National Library of Medicine.