Tvärbindning av DNA
Inom genetik uppstår tvärbindning av DNA när olika exogena eller endogena medel reagerar med två nukleotider av DNA och bildar en kovalent koppling mellan dem . Denna tvärbindning kan ske inom samma sträng (intrasträng) eller mellan motsatta strängar av dubbelsträngat DNA (intersträng). Dessa addukter interfererar med cellulär metabolism, såsom DNA-replikation och transkription , vilket utlöser celldöd . Dessa tvärbindningar kan emellertid repareras genom excision eller rekombinationsvägar.
DNA-tvärbindning har också användbara fördelar vid kemoterapi och inriktning mot cancerceller för apoptos , såväl som för att förstå hur proteiner interagerar med DNA.
Tvärbindningsmedel
Många karakteriserade tvärbindningsmedel har två oberoende reaktiva grupper inom samma molekyl, som var och en kan binda med en nukleotidrest av DNA. Dessa medel separeras baserat på deras ursprungskälla och märks antingen som exogena eller endogena. Exogena tvärbindningsmedel är kemikalier och föreningar, både naturliga och syntetiska, som härrör från miljöexponering såsom läkemedel och cigarettrök eller bilavgaser. Endogena tvärbindningsmedel är föreningar och metaboliter som introduceras från cellulära eller biokemiska vägar inom en cell eller organism.
Exogena medel
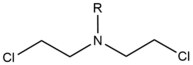
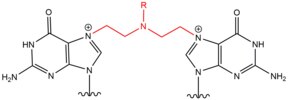
- Kvävesenap är exogena alkyleringsmedel som reagerar med N7 - positionen i guanin. Dessa föreningar har en kärnstruktur av bis-(2-etylklor)amin, med en variabel R -grupp, där de två reaktiva funktionella grupperna tjänar till att alkylera nukleobaser och bilda en tvärbindningsskada. Dessa medel bildar mest föredraget en 1,3 5'-d(GNC) intersträng-tvärbindning. Införandet av detta medel böjer DNA-duplexet något för att ta hänsyn till medlets närvaro i helixen. Dessa medel introduceras ofta som ett läkemedel och används i cytotoxisk kemoterapi .
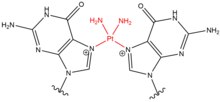
- Cisplatin (cis-diammindiklorplatina(II)) och dess derivat verkar mestadels på intilliggande guaniner vid deras N7 - positioner. Den plana föreningen länkar till nukleobaser genom vattenförskjutning av en eller båda av dess kloridgrupper, vilket tillåter cisplatin att bilda monoaddukter till DNA eller RNA, intrasträng-DNA-tvärbindningar, intersträng-DNA-tvärbindningar och DNA-proteintvärbindningar. När cisplatin genererar DNA-tvärbindningar, bildar det oftare 1,2-intrasträng-tvärbindningar (5'-GG), men bildar också 1,3-intrasträng-tvärbindningar (5-GNG) vid lägre procentandelar. När cisplatin bildar tvärbindningar mellan strängarna (5'-GC) uppstår en allvarlig förvrängning av DNA-spiralen på grund av ett förkortat avstånd mellan guaniner på motsatta strängar och ett cytosin som vänds ut ur helixen som en konsekvens av GG-interaktionen. I likhet med kvävesenap används cisplatin frekvent i kemoterapibehandling - speciellt för testikel- och äggstockscancer.
- Kloroetylnitrosourea (CENU), specifikt karmustin (BCNU), är tvärbindningsmedel som används i stor utsträckning i kemoterapi, särskilt för hjärntumörer. O6 Dessa medel O6 skiljer sig från andra tvärbindare eftersom de alkylerar av guanin för att bilda en -etanoguanin. Denna intermediära förening leder sedan till en intersträng-tvärbindning mellan ett GC-baspar. Dessa tvärbindningsmedel resulterar endast i små förvrängningar av DNA-spiralen på grund av molekylernas mindre storlek.
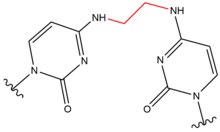
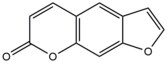
- Psoralener är naturliga föreningar (furokoumariner) som finns i växter. Dessa föreningar interkaleras in i DNA vid 5'-AT-sekvensställen och bildar tymidinaddukter när de aktiveras i närvaro av ultravioletta A (UV-A) strålar . Dessa kovalenta addukter bildas genom att länka 3, 4 ( pyron ) eller 4', 5' ( furan ) kanten av psoralen till 5, 6 dubbelbindningen av tymin . Psoralener kan bilda två typer av monoaddukter och en diaddukt (en tvärbindning mellan strängar) med tymin . Dessa addukter resulterar i lokala förvrängningar av DNA vid interkalationsstället. Psoralener används vid medicinsk behandling av hudsjukdomar, såsom psoriasis och vitiligo .
- Mitomycin C (MMC) är från en klass av antibiotika som används brett i kemoterapi, ofta med mag-tarmrelaterade cancerformer. Mitomycin C kan endast fungera som tvärbindare när en DNA-nukleotid har fått en reduktion till sin kinonring . När två dG har omarrangerats och metylerats på detta sätt, kan en 5'-GC intersträng-tvärbindning bildas med exoaminerna i varje nukleobas. Mitomycin har också förmågan att bilda monoaddukter och intrasträngtvärbindningar med DNA också. Tvärbindningarna mellan strängarna av Mitomycin C bildas i det mindre spåret av DNA, vilket inducerar en måttlig breddning eller sträckning till DNA-spiralen för att ta emot närvaron av molekylen i de två strängarna.
Endogena medel
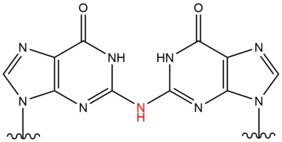
- Salpetersyrlighet bildas som en biprodukt i magen från kostkällor av nitriter och kan leda till tvärbindningsskador i DNA genom omvandling av aminogrupper i DNA till karbonyler. Denna typ av lesion förekommer oftast mellan två guanosiner, varvid 1 av 4 deaminerade guanosiner resulterar i en tvärbindning mellan strängarna. Det inducerar bildning av intersträng-DNA-tvärbindningar vid aminogruppen av exocyklisk N2 av guanin vid 5'-CG-sekvenser. Denna lesion förvränger den dubbla helixen milt.
- Bifunktionella aldehyder är reaktiva kemikalier som bildas endogent via lipidperoxidation och prostoglandinbiosyntes . De skapar etenaddukter som bildas av aldehyd som genomgår omarrangemang för att bilda tvärbindningar på motsatta DNA-strängar. Malondialdehyd är ett prototypiskt exempel som kan tvärbinda DNA via två exocykliska guaninaminogrupper. Andra aldehyder, såsom formaldehyd och acetylaldehyd , kan introducera tvärbindningar mellan strängarna och fungerar ofta som exogena medel eftersom de finns i många bearbetade livsmedel. Ofta finns i bekämpningsmedel, tobaksrök och bilavgaser, α,β-omättade aldehyder, såsom akrolein och krotonaldehyd, är ytterligare exogena medel som kan inducera DNA-tvärbindningar. Till skillnad från andra tvärbindningsmedel är aldehyd-inducerad tvärbindning en i sig själv reversibel process. NMR-struktur av dessa typer av medel som tvärbindningar mellan strängar visar att en 5'-GC-addukt resulterar i mindre förvrängning av DNA, men en 5'-CG-addukt destabiliserar helixen och inducerar en böjning och vridning i DNA:t.
- DNA-tvärbindande lesioner kan också bildas under förhållanden av oxidativ stress, där fria syreradikaler genererar reaktiva intermediärer i DNA, och dessa lesioner har varit inblandade i åldrande och cancer. Tandem-DNA-lesioner bildas med en betydande frekvens genom joniserande strålning och metallkatalyserade H 2 O 2 -reaktioner. Under anoxiska förhållanden är den dominerande dubbelbasskadan en art där C8 av guanin är kopplad till 5-metylgruppen i en intilliggande 3'-tymin (G[8,5-Me]T), vilket bildar intrasträngskada lesioner.
Sammanfattande tabell över tvärbindningsmedel
| Tvärbindningsmedel | Alkyleringsmedel | Tvärlänkningsstruktur | Företrädesrikt målsekvens |
| Kvävesenap | Intrastrand; 5'-GC | ||
| Cisplatin | Intrastrand; 5'-GC Interstrand; 5'-GNG |
||
| Carmustine (BNCU) | Interstand; GC baspar | ||
| Mitomycin C | Interstrand; 5'-GC | ||
| Psoralen | Interstand; 5'-TA | ||
| Malondialdehyd | Interstrand; 5'-GC, 5'-CG | ||
| Oxidativ stress (och strålning) | Intrastrand; d(GpT) | ||
| Salpetersyra | Interstrand; 5'-CG |
Reparation av DNA-tvärbindningar
Tvärbundet DNA repareras i celler genom en kombination av enzymer och andra faktorer från nukleotidexcisionsreparationsvägen (NER), homolog rekombination och basexcisionsreparationsvägen (BER). För att reparera tvärbindningar mellan strängar i eukaryoter, rekryteras ett 3'-fliksendonukleas från NER, XPF-ERCC1, till det tvärbundna DNA:t, där det hjälper till att "haka av" DNA:t genom att klyva 3'-strängen vid tvärbindningsstället. 5'-strängen klyvs sedan, antingen av XPF-ERCC1 eller annat endonukleas , vilket bildar ett dubbelsträngsbrott (DSB), som sedan kan repareras genom den homologa rekombinationsvägen .
DNA-tvärbindningar orsakar i allmänhet förlust av överlappande sekvensinformation från de två DNA-strängarna. Därför beror korrekt reparation av skadan på att man hämtar den förlorade informationen från en oskadad homolog kromosom i samma cell. Hämtning kan ske genom att paras ihop med en systerkromatid som producerats under en föregående replikeringsrunda. I en diploid cell kan återhämtning också ske genom parning med en icke-syster homolog kromosom , vilket sker särskilt under meios . [ citat behövs ] När parning har inträffat kan tvärbindningen tas bort och korrekt information införas i den skadade kromosomen genom homolog rekombination.
Klyvning av bindningen mellan ett deoxiribossocker i DNA:s sockerfosfatryggrad och dess associerade nukleobas lämnar ett abasiskt ställe i dubbelsträngat DNA. Dessa abasiska ställen genereras ofta som en intermediär och återställs sedan i basexcisionsreparation. Men om dessa platser tillåts bestå kan de hämma DNA-replikation och transkription. Abasiska ställen kan reagera med amingrupper på proteiner för att bilda DNA-proteintvärbindningar eller med exocykliska aminer av andra nukleobaser för att bilda tvärbindningar mellan strängar. För att förhindra tvärbindningar mellan strängar eller DNA-protein binder enzymer från BER-vägen tätt det abasiska stället och binder det från närliggande reaktiva grupper, vilket visas i humant alkyladenin-DNA-glykosylas (AAG) och E. coli 3-metyladenin-DNA-glykosylas II ( AlkA ) . in vitro bevis visade att Interstand Cross-Links inducerade av abasic site (DOB-ICL) är en replikationsblockerande och mycket felkodande lesion. Jämfört med flera andra undersökta TLS-poler är pol η sannolikt att bidra till den TLS-medierade reparationen av DOB-ICL in vivo . Genom att använda O 6 -2'-deoxyguanosin-butylen-O 6 -2'-deoxyguanosin (O6-dG-C4-O6-dG) DNA-lesioner som är en kemiskt stabil struktur, hade den kringgående aktiviteten hos flera DNA-polymeraser undersökts och resultaten visade att pol n uppvisade den högsta bypassaktiviteten; emellertid var 70 % av bypass-produkterna mutagena innehållande substitutioner eller deletioner. Ökningen av storleken på ohakade reparationsmellanprodukter ökar frekvensen av deletionsmutationer.
Behandling av E. coli med psoralen -plus-UV-ljus ( PUVA ) producerar tvärbindningar mellan strängarna i cellernas DNA. Cole et al. och Sinden och Cole presenterade bevis för att en homolog rekombinationell reparationsprocess som kräver produkterna av generna uvrA , uvrB och recA kan ta bort dessa tvärbindningar i E. coli . Denna process verkar vara ganska effektiv. Även om en eller två oreparerade tvärbindningar är tillräckliga för att inaktivera en cell, kan en bakteriecell av vildtyp reparera och därför återhämta sig från 53 till 71 psoralentvärbindningar. Eukaryota jästceller inaktiveras också av en kvarvarande tvärbindning, men vildtypsjästceller kan återhämta sig från 120 till 200 tvärbindningar.
Ansökningar
Tvärbindning av DNA och protein
Biokemiska interaktionsmetoder
Tvärbindning av DNA-protein kan orsakas av en mängd olika kemiska och fysikaliska medel, inklusive övergångsmetaller, joniserande strålning och endogena aldehyder, förutom kemoterapeutiska medel . I likhet med DNA-tvärbindning är DNA-proteintvärbindningar lesioner i celler som ofta skadas av UV-strålning. UV-effekten kan leda till reaktiva interaktioner och få DNA och de proteiner som är i kontakt med det att tvärbinda. Dessa tvärbindningar är mycket skrymmande och komplexa lesioner. De förekommer främst i områden av kromosomerna som genomgår DNA-replikation och stör cellulära processer.
Framstegen inom strukturidentifieringsmetoder har gått framåt, och tillägget av förmågan att mäta interaktioner mellan DNA och protein är ett krav för att till fullo förstå de biokemiska processerna. Strukturen av DNA-proteinkomplex kan kartläggas genom fototvärbindning, vilket är den fotoinducerade bildningen av en kovalent bindning mellan två makromolekyler eller mellan två olika delar av en makromolekyl. Metodiken involverar kovalent länkning av ett DNA-bindande motiv av det målsekvensspecifika DNA-bindande proteinet med ett fotoaktiverbart tvärbindningsmedel som kan reagera med DNA-nukleotider när det exponeras för UV. Denna metod ger information om interaktionen mellan DNA:t och proteinet i tvärbindningen.
Kliniska behandlingar
DNA-reparationsvägar kan resultera i bildandet av tumörceller . Cancerbehandlingar har konstruerats med hjälp av DNA-tvärbindningsmedel för att interagera med kvävehaltiga baser av DNA för att blockera DNA-replikation. Dessa tvärbindande medel har förmågan att fungera som terapier med ett medel genom att rikta in sig på och förstöra specifika nukleotider i cancerceller. Detta resultat stoppar cykeln och tillväxten av cancerceller; eftersom det hämmar specifika DNA-reparationsvägar, har detta tillvägagångssätt en potentiell fördel genom att ha färre biverkningar.
Hos människor är den främsta orsaken till cancerdödsfall i världen lungcancer, inklusive icke-småcelligt lungkarcinom (NSCLC) som står för 85 % av alla lungcancerfall i USA. Individer med NSCLC behandlas ofta med terapeutiska platinaföreningar (t.ex. cisplatin, karboplatin eller oxaliplatin) (se Lungcancerkemoterapi) som orsakar tvärbindningar av DNA mellan strängarna. Bland individer med NSLC har lågt uttryck av bröstcancer 1-genen ( BRCA1 ) i primärtumören korrelerat med förbättrad överlevnad efter platinainnehållande kemoterapi. Denna korrelation antyder att låg BRCA1 i cancern, och den därav följande låga nivån av DNA-reparation, orsakar cancerns sårbarhet för behandling av DNA-tvärbindningsmedlen. Hög BRCA1 kan skydda cancerceller genom att verka i den homologa rekombinationella reparationsvägen som tar bort skadorna i DNA som introducerats av platinaläkemedlen. Nivån av BRCA1 -uttryck är potentiellt ett viktigt verktyg för att skräddarsy kemoterapi i lungcancerhantering.
Klinisk kemoterapeutika kan inducera enzymatiska och icke-enzymatiska DNA-proteintvärbindningar. Ett exempel på denna induktion är med platinaderivat, såsom cisplatin och oxaliplatin. De skapar icke-enzymatiska DNA-proteintvärbindningar genom ospecifik tvärbindning av kromatininteragerande proteiner till DNA. Tvärbindning är också möjlig i andra terapeutiska medel genom att antingen stabilisera kovalenta DNA-proteinreaktionsmellanprodukter eller genom att skapa ett pseudosubstrat, som fångar enzymet på DNA. Kamptotecinderivat, såsom irinotekan och topotekan, riktar in sig på och fångar specifikt DNA- topoisomeras 1 (TOP1) genom att interkalera i enzym-DNA-gränssnittet. Eftersom toxiciteten hos dessa läkemedel beror på TOP1-infångning, beror cellulär känslighet för dessa föreningar direkt på TOP1-expressionsnivåer. Som ett resultat är funktionen av dessa läkemedel att tjäna som enzymgifter snarare än hämmare. Detta kan användas för att behandla tumörceller genom att använda TOP 2 enzymgifter.
externa länkar
- – Interaktiv struktur för cisplatin- och DNA-adduktbildning
- – Interaktiv struktur för psoralen och tvärbundet DNA
- Psoralen Ultraviolet En ljusbehandling