Uremi
| Uremi | |
|---|---|
| Andra namn | Uremi |
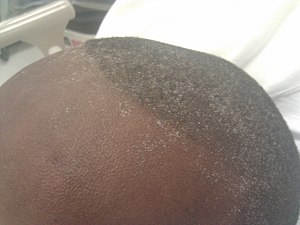 | |
| Uremisk frost i pannan och hårbotten på en ung man som fick klagomål om anorexi och trötthet , med ureakväve i blodet och serumkreatininnivåer på cirka 100 respektive 50 mg/dL. | |
| Specialitet | Nefrologi |
Uremi är termen för höga nivåer av urea i blodet. Urea är en av de primära komponenterna i urin. Det kan definieras som ett överskott i blodet av aminosyra- och proteinmetabolismslutprodukter , såsom urea och kreatinin , som normalt skulle utsöndras i urinen. Uremiskt syndrom kan definieras som den terminala kliniska manifestationen av njursvikt (även kallad njursvikt) . Det är tecknen, symtomen och resultaten från laboratorietester som är resultatet av otillräcklig utsöndring, reglerande och endokrina funktion hos njurarna. Både uremi och uremiskt syndrom har använts omväxlande för att beteckna en mycket hög plasmaureakoncentration som är resultatet av njursvikt. Den tidigare beteckningen kommer att användas för resten av artikeln.
Azotemi är ett liknande, mindre allvarligt tillstånd med höga nivåer av urea, där avvikelsen kan mätas kemiskt men ännu inte är så allvarlig att den ger symtom. Uremi beskriver de patologiska och symtomatiska manifestationerna av svår azotemi.
Det finns ingen specifik tidpunkt för uppkomsten av uremi för personer med progressiv förlust av njurfunktion . Personer med njurfunktion under 50 % (dvs. en glomerulär filtrationshastighet [GFR] mellan 50 och 60 ml/min) och över 30 år kan ha uremi till en viss grad. Detta betyder att uppskattningsvis 8 miljoner människor i USA med en GFR på mindre än 60 ml/min har uremiska symtom. Symtomen, som trötthet, kan vara mycket vaga, vilket gör diagnosen nedsatt njurfunktion svår. Behandling kan vara genom dialys eller en njurtransplantation , även om vissa patienter väljer att fortsätta symtomkontroll och konservativ vård istället.
tecken och symtom
Klassiska tecken på uremi är: progressiv svaghet och lätt trötthet, aptitlöshet på grund av illamående och kräkningar, muskelatrofi , skakningar, onormal mental funktion, frekvent yt andning och metabolisk acidos . Utan intervention via dialys eller njurtransplantation kommer uremi på grund av njursvikt att utvecklas och orsaka stupor, koma och död. Eftersom uremi oftast är en följd av njursvikt, uppträder dess tecken och symtom ofta samtidigt med andra tecken och symtom på njursvikt. [ citat behövs ]
Glomerulär filtrationshastighet (GFR) mäter mängden plasma i milliliter som filtreras genom njurarna varje minut. När GFR minskar försämras prognosen. En del av effekterna kan vändas, om än tillfälligt, med dialys. [ citat behövs ]
| GFR (ml/min) | Effekter |
|---|---|
| 100–120 | Normal GFR |
| <60 | Uremiska symtom kan förekomma, nedsatt välbefinnande |
| 30–60 | Kognitiv försämring |
| 55 | Trötthet och minskad uthållighet |
| <50 | Insulinresistens |
| <30 | Ökar sannolikheten för symtom |
| ≤15 | Njursvikt |
Residualsyndrom
Personer i dialys får det som kallas "restsyndrom". Restsyndrom är en icke-livshotande sjukdom som visas som toxiska effekter som orsakar många av samma tecken och symtom som uremi visar. Det finns flera hypoteser varför kvarvarande syndrom är närvarande. De är: ackumulering av lösta ämnen med stor molekylvikt β2 -mikroglobulin som är dåligt dialyserade (t.ex. ); ackumulering av proteinbundna lösta ämnen med liten molekylvikt som är dåligt dialyserade (t.ex. p-kresylsulfat och indoxylsulfat ); ackumulering av dialyserbara lösta ämnen som avlägsnas ofullständigt (t.ex. sekvestrerade lösta ämnen som fosfat i celler eller otillräcklig eliminering av andra mer toxiska lösta ämnen); indirekta fenomen som karbamylering av proteiner, vävnadsförkalkning eller en toxisk effekt av hormonobalans (t.ex. bisköldkörtelhormon) och; de toxiska effekterna av själva dialysen (t.ex. avlägsnande av okända viktiga vitaminer eller mineraler). Dialys ökar livslängden men patienterna kan ha mer begränsad funktion. De har fysiska begränsningar som inkluderar försämring av balans, gånghastighet och sensoriska funktioner. De har också kognitiva försämringar såsom försämring av uppmärksamhet, minne och prestationsförmåga av högre ordningsuppgifter. Patienter har bibehållits längre än tre decennier på dialys, men den genomsnittliga dödligheten och sjukhusvistelser är höga. Dessutom är patienternas rehabilitering och livskvalitet dålig.
Orsaker
Tillstånd som orsakar ökad blodurea delas in i tre olika kategorier: prerenal, renal och postrenal. [ citat behövs ]
Prerenal azotemi kan orsakas av minskat blodflöde genom njurarna (t.ex. lågt blodtryck , kongestiv hjärtsvikt , chock , blödning , uttorkning ) eller av ökad produktion av urea i levern via en proteinrik kost eller ökad proteinkatabolism (t.ex. stress, feber, allvarlig sjukdom, kortikosteroidbehandling eller gastrointestinal blödning).
Njurorsaker kan hänföras till nedsatt njurfunktion. Dessa inkluderar akut och kronisk njursvikt , akut och kronisk glomerulonefrit , tubulär nekros och andra njursjukdomar .
Postrenala orsaker kan bero på minskad eliminering av urea. Dessa kan bero på obstruktion av urinutflöde såsom stensten, tumörer i urinblåsan eller prostata eller en allvarlig infektion.
Diagnos
En detaljerad och noggrann historia och fysisk undersökning hjälper till att avgöra om uremi är akut eller kronisk. I fall av akut uremi kan orsaker identifieras och elimineras, vilket leder till en högre chans för återhämtning av normal njurfunktion, om den behandlas korrekt.
Blodprov
Primära tester som utförs för diagnos av uremi är en grundläggande metabolisk panel med serumkalcium och fosfor för att utvärdera GFR , blodkarbamidkväve och kreatinin samt serumkalium- , fosfat- , kalcium- och natriumnivåer . Den huvudsakliga abnormiteten är mycket låg GFR (<30 ml/min). Uremi kommer att visa förhöjda både urea och kreatinin, sannolikt förhöjt kalium, högt fosfatvärde och normalt eller något högt natrium, samt sannolikt sänkta kalciumnivåer. Som en grundläggande upparbetning kommer en läkare också att utvärdera för anemi och sköldkörtel- och bisköldkörtelfunktioner. Kronisk anemi kan vara ett olycksbådande tecken på etablerad njursvikt. Sköldkörtel- och bisköldkörtelpanelerna kommer att hjälpa till att arbeta upp eventuella trötthetssymtom, samt fastställa kalciumavvikelser när de relaterar till uremi kontra långvarig eller orelaterade sjukdom av kalciummetabolism. [ citat behövs ]
Urinprov
En 24-timmars urinsamling för bestämning av kreatininclearance kan vara ett alternativ, men inte ett särskilt exakt test på grund av insamlingsproceduren. Ett annat laboratorietest som bör övervägas är urinanalys med mikroskopisk undersökning för förekomst av protein, gips, blod och pH.
Radioisotoptester
Det mest pålitliga testet för att bestämma GFR är iothalamatclearance . Det kan dock vara kostnadskrävande och tidskrävande. Kliniska laboratorier beräknar generellt GFR med modifiering av kosten vid njursjukdom (MDRD) formel eller Cockcroft-Gault formel .
Övrig
Dessutom kan koagulationsstudier indikera förlängd blödningstid med i övrigt normala värden. [ citat behövs ]
Mekanism
Uremi resulterar i att många olika föreningar kvarhålls av kroppen. Med njursvikt kan dessa föreningar byggas upp till farliga nivåer. Det finns mer än 90 olika föreningar som har identifierats. Vissa av dessa föreningar kan vara giftiga för kroppen. [ citat behövs ]
| Solut grupp | Exempel | Källa | Egenskaper |
|---|---|---|---|
| Peptider och små proteiner | p2 - mikroglobulin | skur från större histokompatibilitetskomplex | dåligt dialyserad på grund av stor storlek |
| Guanidiner | guanidinbärnstenssyra | arginin | ökad produktion vid uremi |
| Fenoler | ρ-kresylsulfat | fenylalanin , tyrosin | proteinbundet, producerat av tarmbakterier |
| Indoler | indianska | tryptofan | proteinbundet, producerat av tarmbakterier |
| Alifatiska aminer | dimetylamin | kolin | stor distributionsvolym, producerad av tarmbakterier |
| Polyoler | CMPF | okänd | hårt proteinbundet |
| Ukleosider | pseudouridin | tRNA | mest framträdande av flera förändrade RNA-arter |
| Dikarboxylsyror | oxalat | askorbinsyra | bildning av kristallavlagringar |
| Karbonyler | glyoxal | glykolytiska mellanprodukter | reaktion med proteiner för att bilda avancerade glykeringsslutprodukter |
Uremiska toxiner
Uremiska toxiner är alla biologiskt aktiva föreningar som kvarhålls på grund av nedsatt njurfunktion. Många uremiska salter kan också vara uremiska toxiner. [ citat behövs ]
Urea var en av de första metaboliterna som identifierades. Dess borttagande är direkt relaterat till patientens överlevnad men dess effekt på kroppen är ännu inte klarlagd. Ändå är det inte säkert att de symtom som för närvarande är förknippade med uremi faktiskt orsakas av överskott av urea, eftersom en studie visade att uremiska symtom lindrades genom initiering av dialys, även när urea tillsattes dialysatet för att bibehålla blodets ureakvävenivå vid cirka 90 mg per deciliter (det vill säga cirka 32 mmol per liter). Urea kan vara föregångaren till mer giftiga molekyler, men det är mer troligt att skada på kroppen beror på en kombination av olika föreningar som kan fungera som enzymhämmare eller störa membrantransporten . Indoxylsulfat är ett av de bättre karakteriserade uremiska toxinerna. Indoxylsulfat har visat sig förvärra vaskulär inflammation vid ateroskleros genom att modulera makrofagernas beteende.
| Toxin | Effekt | Referenser |
|---|---|---|
| Urea | Vid höga koncentrationer [>300 mg/dL(>50 mmol/L)]: huvudvärk, kräkningar, trötthet, karbamylering av proteiner | |
| Kreatinin | Påverkar möjligen glukostolerans och erytrocytöverlevnad | |
| Cyanat | Dåsighet och hyperglykemi, karbamylering av proteiner och förändrad proteinfunktion på grund av att det är en nedbrytningsprodukt av urea | |
| Polyoler (t.ex. myoinositol ) | Perifer neuropati | |
| Fenoler | Kan vara mycket giftiga eftersom de är lipidlösliga och därför lätt kan passera cellmembran | |
| "Mellanmolekyler" | Peritonealdialyspatienter rensar mellanmolekyler mer effektivt än hemodialyspatienter. De visar färre tecken på neuropati än hemodialyspatienter | |
| p2 - mikroglobulin | Renal amyloid | |
| Indoxylsulfat | Inducerar njurdysfunktion och kardiovaskulär dysfunktion ; associerade med kronisk njursjukdom och hjärt-kärlsjukdom | |
| ρ-kresylsulfat | Ackumuleras i och förutsäger kronisk njursjukdom |
Biokemiska egenskaper
Många reglerande funktioner i kroppen påverkas. Reglering av kroppsvätskor, saltretention, utsöndring av syra och kvävehaltiga metaboliter är alla försämrade och kan fluktuera kraftigt. Kroppsvätskeregleringen försämras på grund av att vätska inte utsöndras, eller på grund av vätskeförlust från kräkningar eller diarré. Regleringen av salt försämras när saltintaget är lågt eller kärlvolymen är otillräcklig. Syrautsöndring och utsöndring av kvävehaltiga metaboliter försämras med förlust av njurfunktion.
| Bibehållna kvävehaltiga metaboliter | Vätske-, syra-bas- och elektrolytstörningar | Kolhydratintolerans | Onormal lipidmetabolism | Förändrad endokrin funktion |
|---|---|---|---|---|
| Urea | Fast urinosmolalitet | Insulinresistens (hypoglykemi kan också förekomma) | Hypertriglyceridemi | Sekundär hyperparatyreos |
| Cyanat | Metabolisk acidos | Plasmainsulin normalt eller ökat | Minskad högdensitetslipoproteinkolesterol | Förändrad tyroxinmetabolism |
| Kreatinin | Hyponatremi eller hypernatremi eller hyperkalcemi | Försenat svar på kolhydratladdning | Hyperlipoproteinemi | Hyperreninemi och hyperaldosteronism |
| Guanidinföreningar | Hyperkloremi | Hyperglukagonemi | Hyporeninemi | |
| "Mellanmolekyler" | Hypokalcemi | Hypoaldosteronism | ||
| Urinsyra | Hyperfosfatemi | Minskad erytropoietinproduktion | ||
| Hypermagnesemi | Gonadal dysfunktion (ökat prolaktin och luteiniserande hormon , minskat testosteron ) | |||
| Minskad natrium-kalium-ATPas- aktivitet | Ökat serumgastrin och melanocytstimulerande hormon |
Historia
Urea kristalliserades och identifierades mellan 1797 och 1808. Urea antogs vara källan till urinammoniak under denna tid och bekräftades 1817. Det antogs att överskott av urea kan leda till specifika störningar. Senare 1821 bekräftades det att kroppen producerade urea och att det utsöndrades av njurarna. År 1827 syntetiserades urea först i labbet, vilket bekräftade sammansättningen av urea och gjorde det till det första biologiska ämnet som syntetiserades. 1856 producerades urea in vitro via oxidation av proteiner. Det var 1827 som Henri Dutrochet sådde idén om dialys med upptäckten att separera mindre molekyler från större molekyler genom ett semipermeabelt membran. Det var 1829 och 1831 när övertygande bevis erhölls att hos vissa patienter var blodurea förhöjd. De föreslog också att skada kan orsakas av detta. Senare forskning antydde att större neurologiska störningar som koma och kramper inte korrelerade med fysiska fynd som inkluderade generaliserat ödem i hjärnan. Detta antydde att uremi var en form av blodförgiftning. År 1851 beskrev ET Frerich kliniskt uremiskt syndrom och föreslog att en toxicitet var mekanismen för dess orsak. Det var 1856 som J. Picard utvecklade en känslig metod för att reproducerbart mäta blodurea. Han kunde detektera en 40 % minskning av ureakoncentrationen mellan njurartären och njurvenen. Detta arbete befäste det faktum att njursvikt sammanföll med en ökning av blodurea. Det var J. Picard med ET Frerichs arbete som gjorde termen uremi populär.
Muntliga manifestationer
Orala symtom på uremi kan hittas hos upp till 90 % av njurpatienterna. Patienterna kan uppvisa ammoniakliknande smak och lukt i munnen, stomatit , gingivit , minskat salivflöde, xerostomi och parotit.
Ett av de tidiga symtomen på njursvikt är uremisk fetor . Det är en ammoniaklukt i munnen som orsakas av den höga koncentrationen av urea i saliven som sedan bryts ner till ammoniak. När nivån av ureakväve i blodet (BUN) ökar, kan patienten utveckla uremisk stomatit. Uremisk stomatit uppträder som ett pseudomembran eller uppriktiga sår med rodnad och en pultartad päls i munnen. Dessa lesioner kan relateras till hög BUN-nivå >150 mg/dl och försvinner spontant när BUN-nivån reduceras med medicinsk behandling. Det tros vara orsakat av förlust av vävnadsmotstånd och oförmåga att motstå traumatiska influenser. Utöver det kan patienten utveckla en sällsynt manifestation som är uremisk frost . Det är en vit plack som finns på huden eller i munnen, den orsakas av kvarvarande ureakristaller kvar på epitelytan efter svett och salivavdunstning eller som ett resultat av minskat salivflöde. Xerostomi är ett vanligt oralt fynd, det beror på en kombination av direkt inblandning av spottkörtlar, kemisk inflammation, uttorkning och munandning. Det kan bero på begränsat vätskeintag, negativ effekt av läkemedelsbehandling eller låg salivhastighet. Spottsvullnad kan ses ibland.
Hos patienter med njursjukdom kan blekhet i munslemhinnan ibland märkas på grund av anemi orsakad av reduktion av erytropoietin. Uremi kan leda till förändring av trombocytaggregationen. Denna situation, i kombination med användningen av heparin och andra antikoagulantia vid hemodialys, gör att patienterna blir predisponerade för ekkymos , petekier och blödningar i munhålan. Det kan också leda till mukosit och glossit som kan orsaka smärta och inflammation i tungan och munslemhinnan. Dessutom kan patienter också uppleva förändrade smakupplevelser, dysgeusi och vara predisponerade för bakteriella och candidiasisinfektioner. Candidiasis är vanligare hos njurtransplanterade patienter på grund av generaliserad immunsuppression.
Hos barn med njursjukdom har emaljhypoplasi av den primära och permanenta tanden observerats. Avvikelserna i tandutvecklingen korrelerar med den ålder vid vilken metabola störningar uppstår. Till exempel är emaljhypoplasi i form av vit eller brun missfärgning av primärtänder vanligen hos små barn med tidig njursjukdom. Dålig munhygien, en kolhydratrik kost, sjukdomsrelaterad försvagning, hypoplastisk emalj, lågt salivflöde och långvarig medicinering bidrar till ökad risk för kariesbildning . Patienterna har dock vanligtvis låg kariesaktivitet, särskilt hos barn. Detta beror på närvaron av starkt buffrad och alkalisk saliv orsakad av den höga koncentrationen av ureakväve och fosfat i saliv. Salivens pH-värde kommer vanligtvis att ligga över den kritiska pH-nivån för att avmineralisering av emaljen ska ske och detta hjälper till att förhindra bildandet av karies. Utöver det är pulpaförträngning och förkalkning ett vanligt fynd hos patienter med njursjukdom. För patienter som går i dialys illamående och kräkningar till följd av dialysbehandling leda till allvarlig tanderosion .
Tandvårdshänsyn
Vid behandling av patienter med njurinsufficiens bör en tandläkare samla in en fullständig medicinsk historia, med särskild uppmärksamhet på ESRD-relaterade sjukdomar, läkemedel med föreskrivna doser, blodparametrar, tidpunkt och typ av utförd dialys. Dessa aspekter kan diskuteras direkt med nefrologen vid behov. Eventuella förändringar i läkemedel eller andra aspekter av behandlingen måste godkännas i förväg av nefrologen.
Tandundersökning för sådana patienter består av en icke-invasiv fullständig bedömning av dentala, parodontala och mukosala vävnader, med röntgenbilder för att underlätta den diagnostiska processen. Alla potentiella infektionshärdar bör fångas upp; dessa inkluderar periodontala och endodontiska lesioner, kvarvarande rötter, partiellt utbrutna och felplacerade tredje molarer, peri-implantit och mukosala lesioner. Vid misstanke om parodontit ska ett parodontalt diagram registreras. Ortodontiska apparater kan underhållas om de inte stör munhygienen.
Uremi ses ofta hos patienter som genomgår dialys på grund av njurinsufficiens. För hemodialyspatienter är det viktigt att fastställa behandlingsschemat. Tandbehandling bör påbörjas dagen efter hemodialys på grund av flera skäl: det finns ingen ansamling av uremiska toxiner i blodet och cirkulerande heparin saknas. Behandlingen bör inte påbörjas samma dag som hemodialysen eftersom patienterna vanligtvis mår illa och deras blod är hepariniserat, vilket kan orsaka kraftig blödning. För patienter som genomgår peritonealdialys finns det inga kontraindikationer för tandbehandling förutom vid akuta peritoneala infektioner, där ett elektivt ingrepp bör skjutas upp.
Särskild försiktighet bör iakttas när patienten placeras, och undvik komprimering av armen med vaskulär tillgång för hemodialys. Eventuella injektioner eller blodtrycksmätning ska inte utföras på en arm med arteriovenös (AV) fistel. Om AV-platsen är placerad på ett ben, bör patienten undvika att sitta under längre perioder, eftersom venöst dränering kan blockeras. Under långa tandingrepp bör tandläkaren låta patienter med AV-ställen på benen ta en kort promenad eller stå en stund varje timme. [ citat behövs ]
Hemostatiska hjälpmedel bör sättas in i fall av kraftig blödning, vilket vanligtvis ses vid uremi och njursvikt. För att hantera postoperativ blödning bör primära stängningstekniker och lokala hemostatiska medel användas rutinmässigt. För att minska blödningar under och efter ett ingrepp kan tranexamsyra, både som sköljning eller oralt, användas.
Patienter som genomgår dialys utsätts för många transfusioner och njursviktrelaterad immunsuppression; sålunda löper de större risker för infektion med humant immunbristvirus (HIV) och hepatit typ B och C. Det är viktigt att vidta infektionskontrollåtgärder för att undvika korskontaminering i tandkliniken och förhindra risk för exponering för tandvårdspersonal.
En majoritet av medicinerna elimineras från kroppen åtminstone delvis av njurarna. På grund av njursvikt kommer plasmahalveringstiderna för läkemedel som normalt utsöndras i urinen att förlängas, vilket leder till ökad toxicitet. Många läkemedel som normalt administreras säkert kan inte ges till patienter med nedsatt njurfunktion. Dessutom kan vissa läkemedel ges, men dosen måste minskas. Hos patienter som genomgår dialys kommer dock reducerade plasmahalveringstider för läkemedel att observeras. Antibiotika från aminoglykosid- och tetracyklinfamiljerna måste undvikas på grund av deras nefrotoxicitet. De valda antibiotika är penicilliner, klindamycin och cefalosporiner, som kan administreras i normala doser även om det terapeutiska området kommer att utökas. För smärtstillande medel är paracetamol valet för fall av episodisk smärta. Aspirin kännetecknas av en blodplättsdämpande aktivitet och därför bör användningen undvikas hos uremiska patienter. Utmaningen inom farmakoterapi för patienter med njursjukdom är att upprätthålla en medicins terapeutiska nivå inom ett smalt intervall för att undvika subterapeutisk dosering och toxicitet.
Anteckningar
externa länkar
- Uremia , WebMD.com