Synaptisk vesikel
| Synaptisk vesikel | |
|---|---|
 Neuron A (sänder) till neuron B (mottagande). 1 . mitokondrier ; 2 . Synaptisk vesikel med neurotransmittorer ; 3 . Autoreceptor 4 . Synaps med neurotransmittor frisatt ( serotonin ); 5 . Postsynaptiska receptorer aktiverade av neurotransmittor (induktion av en postsynaptisk potential ); 6 . Kalciumkanal ; 7 . Exocytos av en vesikel; 8 . Återfångad signalsubstans. | |
| Detaljer | |
| Systemet | Nervsystem |
| Identifierare | |
| latin | vesicula synaptica |
| Maska | D013572 |
| TH | H2.00.06.2.00004 |
| Anatomiska termer för mikroanatomi | |
I en neuron lagrar synaptiska vesiklar (eller neurotransmittorvesiklar ) olika signalsubstanser som frigörs vid synapsen . Utsläppet regleras av en spänningsberoende kalciumkanal . Vesikler är viktiga för att sprida nervimpulser mellan neuroner och återskapas ständigt av cellen . Området i axonet som innehåller grupper av vesiklar är en axonterminal eller "terminal bouton". Upp till 130 vesiklar kan frigöras per bouton under en tiominutersperiod av stimulering vid 0,2 Hz. I den mänskliga hjärnans visuella cortex har synaptiska vesiklar en genomsnittlig diameter på 39,5 nanometer (nm) med en standardavvikelse på 5,1 nm.
Strukturera
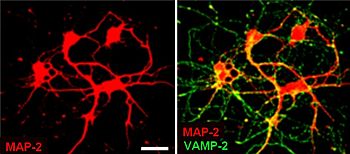
Synaptiska vesiklar är relativt enkla eftersom endast ett begränsat antal proteiner passar in i en sfär med 40 nm diameter. Renade vesiklar har ett protein : fosfolipidförhållande på 1:3 med en lipidkomposition av 40% fosfatidylkolin , 32% fosfatidyletanolamin , 12% fosfatidylserin , 5% fosfatidylinositol och 10% kolesterol .
Synaptiska vesiklar innehåller två klasser av obligatoriska komponenter: transportproteiner involverade i neurotransmittorupptag och trafficking av proteiner som deltar i synaptisk vesikelexocytos, endocytos och återvinning .
- Transportproteiner är sammansatta av protonpumpar som genererar elektrokemiska gradienter , som möjliggör upptag av neurotransmittorer, och neurotransmittortransportörer som reglerar det faktiska upptaget av neurotransmittorer. Den nödvändiga protongradienten skapas av V-ATPase , som bryter ner ATP för energi. Vesikulära transportörer flyttar signalsubstanser från cellernas cytoplasma in i de synaptiska vesiklarna. Vesikulära glutamattransportörer , till exempel, binder glutamat till vesiklar genom denna process.
- Att sälja proteiner är mer komplext. De inkluderar intrinsiska membranproteiner , perifert bundna proteiner och proteiner som SNAREs . Dessa proteiner delar inte en egenskap som skulle göra dem identifierbara som synaptiska vesikelproteiner, och lite är känt om hur dessa proteiner specifikt deponeras i synaptiska vesiklar. Många men inte alla av de kända synaptiska vesikelproteinerna interagerar med icke-vesikulära proteiner och är kopplade till specifika funktioner.
Stökiometrin för förflyttning av olika neurotransmittorer till en vesikel ges i följande tabell .
| Neurotransmittortyp(er) | Inåtgående rörelse | Utåtgående rörelse |
|---|---|---|
| noradrenalin , dopamin , histamin , serotonin och acetylkolin | signalsubstans + | 2H + |
| GABA och glycin | signalsubstans | 1H + |
| glutamat | signalsubstans − + Cl − | 1H + |
Nyligen har det upptäckts att synaptiska vesiklar också innehåller små RNA-molekyler, inklusive överförings-RNA- fragment, Y-RNA- fragment och mirRNA . Denna upptäckt tros ha bred inverkan på att studera kemiska synapser.
Effekter av neurotoxiner
Vissa neurotoxiner , såsom batrachotoxin , är kända för att förstöra synaptiska vesiklar. Stelkrampstoxinet skadar vesikelassocierade membranproteiner (VAMP), en typ av v-SNARE, medan botulinumtoxiner skadar t-SNARES och v-SNARES och därmed hämmar synaptisk överföring . Ett spindeltoxin som kallas alfa-Latrotoxin binder till neurexiner , skadar vesiklar och orsakar massiv frisättning av neurotransmittorer. [ citat behövs ]
Vesikelpooler
Vesikler i nervterminalen är grupperade i tre pooler: den lätt släppbara poolen, återvinningspoolen och reservpoolen. Dessa pooler kännetecknas av sin funktion och position i nervterminalen. Den lätt släppbara poolen är dockad till cellmembranet , vilket gör dessa till den första gruppen av vesiklar som frigörs vid stimulering. Den lätt släppbara poolen är liten och är snabbt uttömd. Återvinningspoolen ligger nära cellmembranet och tenderar att cirkuleras vid måttlig stimulering, så att hastigheten för vesikelfrisättning är samma som eller lägre än hastigheten för vesikelbildning. Denna pool är större än den lätt släppbara poolen, men det tar längre tid att bli mobiliserad. Reservpoolen innehåller vesikler som inte släpps ut under normala förhållanden. Denna reservpool kan vara ganska stor (~50%) i neuroner som odlas på ett glassubstrat, men är mycket liten eller saknas vid mogna synapser i intakt hjärnvävnad.
Fysiologi
Den synaptiska vesikelcykeln
Händelserna i den synaptiska vesikelcykeln kan delas in i några nyckelsteg:
- 1. Trafficking till synapsen
Synaptiska vesikelkomponenter transporteras initialt till synapsen med hjälp av medlemmar av kinesinmotorfamiljen . I C. elegans är huvudmotorn för synaptiska vesiklar UNC-104. Det finns också bevis för att andra proteiner som UNC-16/Sunday Driver reglerar användningen av motorer för transport av synaptiska vesiklar.
- 2. Sändarladdning
Väl framme vid synapsen laddas synaptiska vesiklar med en signalsubstans. Laddning av transmitter är en aktiv process som kräver en neurotransmittortransportör och en protonpump ATPas som ger en elektrokemisk gradient. Dessa transportörer är selektiva för olika klasser av sändare. Karakterisering av unc-17 och unc-47, som kodar för den vesikulära acetylkolintransportören och den vesikulära GABA-transportören har beskrivits hittills.
- 3. Dockning
De laddade synaptiska vesiklarna måste docka nära utsläppsplatser, dock är dockning ett steg i cykeln som vi vet lite om. Många proteiner på synaptiska vesiklar och vid frisättningsställen har identifierats, men ingen av de identifierade proteininteraktionerna mellan vesikelproteinerna och frisättningsställets proteiner kan stå för cykelns dockningsfas. Mutanter i rab-3 och munc-18 förändrar vesikeldockning eller vesikelorganisation vid utsättningsplatser, men de stör inte dockningen helt. SNARE-proteiner verkar nu också vara involverade i dockningssteget i cykeln.
- 4. Grundning
Efter att de synaptiska vesiklarna initialt dockar, måste de förberedas innan de kan börja fusion. Priming förbereder den synaptiska vesikeln så att de kan smälta snabbt som svar på ett kalciuminflöde. Detta primingssteg tros involvera bildningen av delvis sammansatta SNARE-komplex. Proteinerna Munc13 , RIM och RIM-BP deltar i detta evenemang. Munc13 tros stimulera förändringen av t-SNARE-syntaxin från en sluten konformation till en öppen konformation, vilket stimulerar sammansättningen av v-SNARE /t-SNARE-komplex. RIM verkar också reglera priming, men är inte nödvändigt för steget. [ citat behövs ]
- 5. Fusion
Primede vesiklar smälter samman mycket snabbt som svar på kalciumhöjningar i cytoplasman. Denna fusionshändelse tros förmedlas direkt av SNARE och drivs av energin från SNARE-sammansättningen. Den kalciumavkännande triggern för denna händelse är det kalciumbindande synaptiska vesikelproteinet synaptotagmin. Förmågan hos SNAREs att förmedla fusion på ett kalciumberoende sätt har nyligen rekonstituerats in vitro. I överensstämmelse med att SNARE är väsentliga för fusionsprocessen, är v-SNARE- och t-SNARE-mutanter av C. elegans dödliga. På samma sätt indikerar mutanter i Drosophila och knockouts i möss att dessa SNARES spelar en avgörande roll i synaptisk exocytos.
- 6. Endocytos
Detta står för återupptaget av synaptiska vesiklar i fullkontaktfusionsmodellen. Men andra studier har sammanställt bevis som tyder på att denna typ av fusion och endocytos inte alltid är fallet. [ citat behövs ]
Vesikelåtervinning
Två ledande verkningsmekanismer tros vara ansvariga för synaptisk vesikelåtervinning: fullständig kollapsfusion och "kiss-and-run"-metoden. Båda mekanismerna börjar med bildandet av den synaptiska poren som släpper sändaren till det extracellulära utrymmet. Efter frigöring av signalsubstansen kan poren antingen vidgas helt så att vesikeln kollapsar helt in i det synaptiska membranet, eller så kan den stängas snabbt och klämma av membranet för att generera kiss-and-run-fusion.
Full kollaps fusion
Det har visat sig att perioder av intensiv stimulering vid neurala synapser tömmer vesikelantalet samt ökar cellulär kapacitans och ytarea. Detta indikerar att efter att synaptiska vesiklar släpper sin signalsubstans, smälter de samman med och blir en del av cellmembranet. Efter att ha märkt synaptiska vesiklar med HRP ( pepparrotsperoxidas ), fann Heuser och Reese att delar av cellmembranet vid grodans neuromuskulära korsning togs upp av cellen och omvandlades tillbaka till synaptiska vesiklar. Studier tyder på att hela cykeln av exocytos, hämtning och reformering av de synaptiska vesiklarna kräver mindre än 1 minut.
Vid full kollapsfusion smälter den synaptiska vesikeln samman och inkorporeras i cellmembranet. Bildandet av det nya membranet är en proteinmedierad process och kan endast ske under vissa förhållanden. Efter en aktionspotential strömmar Ca 2+ till det presynaptiska membranet. Ca 2+ binder till specifika proteiner i cytoplasman, varav ett är synaptotagmin , som i sin tur utlöser den fullständiga fusionen av den synaptiska vesikeln med cellmembranet. Denna fullständiga sammansmältning av poren assisteras av SNARE- proteiner. Denna stora familj av proteiner förmedlar dockning av synaptiska vesiklar på ett ATP-beroende sätt. Med hjälp av synaptobrevin på den synaptiska vesikeln kan t-SNARE-komplexet på membranet, som består av syntaxin och SNAP-25 , docka, prima och smälta ihop den synaptiska vesikeln i membranet.
Mekanismen bakom fullständig kollapsfusion har visat sig vara målet för botulinum- och stelkrampstoxiner . Botulinumtoxinet har proteasaktivitet som bryter ned SNAP-25- proteinet. SNAP -25- proteinet krävs för vesikelfusion som frigör neurotransmittorer, särskilt acetylkolin. Botulinumtoxin klyver i huvudsak dessa SNARE-proteiner och förhindrar därigenom synaptiska vesiklar från att smälta samman med det cellulära synaptiska membranet och frigöra sina neurotransmittorer. Stelkrampstoxin följer en liknande väg, men angriper istället proteinet synaptobrevin på den synaptiska vesikeln. I sin tur förhindrar dessa neurotoxiner synaptiska vesiklar från att fullborda fullständig kollapsfusion. Utan denna mekanism i kraft kan muskelspasmer, förlamning och död inträffa. [ citat behövs ]
"Kiss-and-spring"
Den andra mekanismen genom vilken synaptiska vesiklar återvinns är känd som kiss-and-run fusion . I det här fallet "kyssar" den synaptiska vesikeln cellmembranet, öppnar en liten por för dess nyttolast av neurotransmittorer att släppas igenom, stänger sedan poren och återanvänds tillbaka in i cellen. Kyss-och-spring-mekanismen har varit ett hett omdebatterat ämne. Dess effekter har observerats och registrerats; men orsaken bakom dess användning i motsats till fullständig kollapsfusion undersöks fortfarande. Det har spekulerats i att kiss-and-run ofta används för att bevara knappa vesikulära resurser samt att de används för att svara på högfrekventa insignaler. Experiment har visat att kiss-and-run-händelser förekommer. Först observerades av Katz och del Castillo, observerades det senare att kiss-and-run-mekanismen skilde sig från full kollapsfusion genom att cellkapacitansen inte ökade i kiss-and-run-händelser. Detta förstärker idén om ett kyss-och-spring-sätt, den synaptiska vesikeln släpper sin nyttolast och separeras sedan från membranet.
Modulation
Celler verkar alltså ha åtminstone två mekanismer att följa för membranåtervinning. Under vissa förhållanden kan celler byta från en mekanism till en annan. Långsam, konventionell, fullständig kollapsfusion dominerar det synaptiska membranet när Ca 2+ -nivåerna är låga, och den snabba kiss-and-run-mekanismen följs när Ca 2+ -nivåerna är höga. [ citat behövs ]
Ales et al. visade att förhöjda koncentrationer av extracellulära kalciumjoner flyttar det föredragna sättet för återvinning och synaptisk vesikelfrisättning till kiss-and-run-mekanismen på ett kalciumkoncentrationsberoende sätt. Det har föreslagits att under utsöndring av neurotransmittorer vid synapser, moduleras exocytossättet av kalcium för att uppnå optimala förhållanden för kopplad exocytos och endocytos enligt synaptisk aktivitet.
Experimentella bevis tyder på att kiss-and-run är det dominerande sättet för synaptisk frisättning i början av stimuluståg. I detta sammanhang reflekterar kiss-and-run en hög sannolikhet för vesikelfrisättning. Förekomsten av kiss-and-run ökar också genom snabb avfyring och stimulering av neuronen, vilket tyder på att kinetiken för denna typ av frisättning är snabbare än andra former av vesikelfrisättning.
Historia
Med tillkomsten av elektronmikroskopet i början av 1950-talet visade sig nervändar innehålla ett stort antal elektrongenomskinliga (transparenta för elektroner) vesiklar. Termen synaptisk vesikel introducerades för första gången av De Robertis och Bennett 1954. Detta var kort efter att transmitterfrisättning vid grodans neuromuskulära korsning visade sig inducera postsynaptiska miniatyrändplattepotentialer som tillskrevs frisättningen av diskreta förpackningar av neurotransmittorer (kvanta) från den presynaptiska nervterminalen. Det var därför rimligt att anta att transmittorsubstansen ( acetylkolin ) fanns i sådana vesiklar, som genom en sekretorisk mekanism skulle släppa ut sitt innehåll i synapspaltan ( vesikelhypotes ).
Den felande länken var demonstrationen att signalsubstansen acetylkolin faktiskt finns i synaptiska vesiklar. Cirka tio år senare möjliggjorde tillämpningen av subcellulära fraktioneringstekniker på hjärnvävnad isolering först av nervändar ( synaptosomer ), och därefter av synaptiska vesiklar från däggdjurshjärnan. Två konkurrerande laboratorier var involverade i detta arbete, det av Victor P. Whittaker vid Institute of Animal Physiology, Agricultural Research Council, Babraham, Cambridge, Storbritannien och det av Eduardo de Robertis vid Instituto de Anatomía General y Embriología, Facultad de Medicina, Universidad de Buenos Aires, Argentina. Whittakers arbete som demonstrerar acetylkolin i vesikelfraktioner från marsvinshjärna publicerades först i abstrakt form 1960 och sedan mer detaljerat 1963 och 1964, och artikeln från de Robertis-gruppen visar en anrikning av bundet acetylkolin i synaptiska vesikelfraktioner från råtta hjärnan dök upp 1963. Båda grupperna släppte synaptiska vesiklar från isolerade synaptosomer genom osmotisk chock . Innehållet av acetylkolin i en vesikel uppskattades ursprungligen till 1000–2000 molekyler. Efterföljande arbete identifierade vesikulär lokalisering av andra neurotransmittorer, såsom aminosyror , katekolaminer , serotonin och ATP . Senare kunde synaptiska vesiklar också isoleras från andra vävnader såsom den övre cervikala ganglien eller bläckfiskhjärnan . Isoleringen av mycket renade fraktioner av kolinerga synaptiska vesiklar från stråltorpedos elektriska organ var ett viktigt steg framåt i studiet av vesikelbiokemi och funktion.
