Schwann cell
| Schwann-cell | |
|---|---|
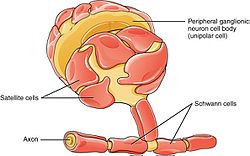 PNS har satellitceller och Schwann-celler.
| |
| Identifierare | |
| Maska | D012583 |
| FMA | 62121 |
| Anatomiska termer för neuroanatomi | |
Schwann-celler eller neurolemmocyter (uppkallade efter den tyska fysiologen Theodor Schwann ) är de huvudsakliga glia i det perifera nervsystemet (PNS). Gliaceller fungerar för att stödja neuroner och i PNS, inkluderar även satellitceller , luktceller , enterisk glia och glia som finns vid sensoriska nervändar, såsom Pacinian corpuscle . De två typerna av Schwann-celler är myeliniserande och icke-myeliniserande. Myeliniserande Schwann-celler omsluter axoner av motoriska och sensoriska neuroner för att bilda myelinskidan . Schwann-cellpromotorn finns i nedströmsregionen av den humana dystrofingenen som ger förkortat transkript som återigen syntetiseras på ett vävnadsspecifikt sätt.
Under utvecklingen av PNS kontrolleras de reglerande mekanismerna för myelinisering av frammatningsinteraktion av specifika gener, vilket påverkar transkriptionskaskader och formar morfologin hos de myeliniserade nervfibrerna.
Schwann-celler är involverade i många viktiga aspekter av perifer nervbiologi - ledning av nervimpulser längs axoner , nervutveckling och -regenerering , trofiskt stöd för neuroner , produktion av nervens extracellulära matris, modulering av neuromuskulär synaptisk aktivitet och presentation av antigener mot T -lymfocyter .
Charcot–Marie–Tooths sjukdom , Guillain–Barrés syndrom (typ akut inflammatorisk demyeliniserande polyradikulopati), schwannomatos , kronisk inflammatorisk demyeliniserande polyneuropati och spetälska är alla neuropatier som involverar Schwann-celler.
Strukturera
| Schwann-celler lindade runt ett axon |
|---|
Schwann-celler är en mängd olika gliaceller som håller perifera nervfibrer (både myeliniserade och omyeliniserade) vid liv. I myeliniserade axoner bildar Schwann-celler myelinskidan . Höljet är inte kontinuerligt. Individuella myeliniserande Schwann-celler täcker cirka 1 mm av ett axon – vilket motsvarar cirka 1000 Schwann-celler längs en 1-meters längd av axonet. Mellanrummen mellan intilliggande Schwann-celler kallas noder av Ranvier .
9-O-Acetyl GD3 gangliosid är en acetylerad glykolipid som finns i cellmembranen hos många typer av ryggradsdjursceller. Under perifer nervregenerering uttrycks 9-O-acetyl GD3 av Schwann-celler.
Fungera
Vertebratens nervsystem förlitar sig på myelinskidan för isolering och som en metod för att minska membrankapacitansen i axonet. Aktionspotentialen hoppar från nod till nod, i en process som kallas saltande ledning , som kan öka ledningshastigheten upp till 10 gånger, utan en ökning av axonal diameter. I denna mening är Schwann-celler PNS:s analoger till centrala nervsystemets oligodendrocyter . Men till skillnad från oligodendrocyter, ger varje myeliniserande Schwann-cell isolering till endast ett axon (se bild). Detta arrangemang tillåter saltande ledning av aktionspotentialer med förökning vid Ranviers noder. På så sätt ökar myeliniseringen kraftigt ledningshastigheten och sparar energi.
Icke-myeliniserande Schwann-celler är involverade i underhåll av axoner och är avgörande för neuronal överlevnad. Vissa grupperar sig kring mindre axoner ( extern bild här ) och bildar Remak-buntar .
Myeliniserande Schwann-celler börjar bilda myelinskidan hos däggdjur under fostrets utveckling och fungerar genom att spiralera runt axonet, ibland med så många som 100 varv. En välutvecklad Schwann-cell är formad som ett ihoprullat pappersark, med lager av myelin mellan varje spole. De inre lagren av omslaget, som huvudsakligen är membranmaterial , bildar myelinskidan, medan det yttersta lagret av kärnförsedd cytoplasma bildar neurilemmat . Endast en liten volym kvarvarande cytoplasma tillåter kommunikation mellan de inre och yttre lagren. Detta ses histologiskt som Schmidt-Lantermann-snittet .
Regeneration
Schwann-celler är kända för sina roller för att stödja nervregenerering . Nerver i PNS består av många axoner myeliniserade av Schwann-celler. Om skada uppstår på en nerv, hjälper Schwann-cellerna till matsmältningen av dess axoner ( fagocytos ). Efter denna process kan Schwann-cellerna styra regenerering genom att bilda en typ av tunnel som leder mot målneuronerna. Denna tunnel är känd som band of Büngner, ett vägledningsspår för de regenererande axonerna, som beter sig som ett endoneuralt rör. Stubben av det skadade axonet kan gro, och de groddar som växer genom Schwann-cells "tunneln" gör det i en hastighet av cirka 1 mm/dag under bra förhållanden. Regenereringshastigheten minskar med tiden. Framgångsrika axoner kan därför återknyta till de muskler eller organ som de tidigare kontrollerat med hjälp av Schwann-celler, men specificiteten upprätthålls inte och fel är frekventa, särskilt när långa avstånd är inblandade. också kopplats till preferentiell motorisk reinnervation . Om Schwann-celler hindras från att associera med axoner, dör axonerna. Regenererande axoner kommer inte att nå något mål om inte Schwann-celler är där för att stödja dem och vägleda dem. De har visat sig vara före tillväxtkottarna .
Schwann-celler är viktiga för upprätthållandet av friska axoner. De producerar en mängd olika faktorer, inklusive neurotrofiner , och överför också viktiga molekyler till axoner.
Genetik
Schwann cellbildning
Sox10
SOX10 är en transkriptionsfaktor som är aktiv under embryonal utveckling och rikligt med bevis tyder på att det är väsentligt för genereringen av glialinjer från stamceller. När SOX10 inaktiveras i möss, misslyckas satellitglia och Schwann-cellprekursorer att utvecklas, även om neuroner genereras normalt utan problem. I frånvaro av SOX10 överlever neurala crest-celler och är fria att generera neuroner, men glialspecifikationen är blockerad. SOX10 kan påverka tidiga gliaprekursorer att svara på neuregulin 1 (se nedan).
Neuregulin 1
Neuregulin 1 (NRG1) verkar på ett antal sätt för att både främja bildningen och säkerställa överlevnaden av omogna Schwann-celler. Under embryonal utveckling hämmar NRG1 bildandet av neuroner från neurala crest-celler, istället bidrar det till att neurala crest-celler leds ner på en väg till gliogenes. NRG1-signalering krävs dock inte för glialdifferentiering från nervkammen.
NRG1 spelar viktiga roller i utvecklingen av neural crest-derivat. Det krävs för neurala kamceller att migrera förbi platsen för dorsala rotganglier för att hitta de ventrala regionerna av sympatisk gangliogenes. Det är också en viktig axon-härledd överlevnadsfaktor och en mitogen för Schwann-cellprekursorer. Det finns i dorsalrotgangliet och motorneuroner vid den tidpunkt då Schwann-cellprekursorer börjar befolka spinalnerver och påverkar därför Schwann-cellöverlevnaden. I embryonala nerver är transmembran III-isoformen troligen den primära varianten av NRG1 som är ansvarig för överlevnadssignaler. Hos möss som saknar transmembran III-isoformen, elimineras Schwann-cellprekursorer så småningom från spinalnerverna.
Bildning av myelinskida
P0
Myelinprotein noll (P0) är en celladhesionsmolekyl som tillhör immunglobulinsuperfamiljen och är huvudkomponenten i perifert myelin, som utgör över 50 % av det totala proteinet i höljet. P0 har visat sig vara väsentligt för bildningen av kompakt myelin, eftersom P0 nollmutant (P0-) möss visade allvarligt avvikande perifer myelinisering. Även om myelinisering av axoner med stor kaliber initierades i P0-möss, var de resulterande myelinskikten mycket tunna och dåligt komprimerade. Oväntat visade P0-möss också degeneration av båda axonerna och deras omgivande myelinskidor, vilket tyder på att P0 spelar en roll för att upprätthålla den strukturella integriteten av både myelinbildning och axonet som det är associerat med. P0-möss utvecklade beteendestörningar runt 2 veckors ålder när möss började visa tecken på lätt darrning. Grov inkoordination uppstod också när djuren utvecklades, samtidigt som darrningen blev allvarligare och några äldre möss utvecklade krampbeteenden. Trots mängden nedsatt motoriskt beteende observerades ingen förlamning hos dessa djur. P0 är också en viktig gen som uttrycks tidigt inom Schwann-celllinjen, uttryckt i Schwann-cellprekursorer efter differentiering från migrerande neurala crest-celler inom det utvecklande embryot.
Krox-20
Flera viktiga transkriptionsfaktorer uttrycks också och involverade i olika utvecklingsstadier, vilket förändrar egenskaperna på Schwann-cellerna från ett omoget till moget tillstånd. En oumbärlig transkriptionsfaktor som uttrycks under myeliniseringsprocessen är Krox-20. Det är en allmän zink-finger transkriptionsfaktor och uttrycks i rombomererna 3 och 5.
Krox-20 anses vara en av huvudregulatorerna för PNS-myelinisering och är viktig för att driva transkription av specifika strukturella proteiner i myelinet. Det har visat sig styra en uppsättning gener som är ansvariga för att störa denna funktion i axonet och ändra den från ett pro-myeliniserande till myeliniserande tillstånd. På detta sätt, i Krox-20 dubbel knock-out möss, har det registrerats att bakhjärnans segmentering påverkas såväl som myelinisering av Schwann-cellassocierade axoner. Faktum är att i dessa möss kan Schwann-cellerna inte utföra sin myelinisering ordentligt eftersom de bara lindar sina cytoplasmatiska processer ett och ett halvt varv runt axonet och trots att de fortfarande uttrycker den tidiga myelinmarkören saknas sena myelin-genprodukter. . Dessutom har nya studier också visat vikten av denna transkriptionsfaktor för att bibehålla myeliniseringsfenotypen (och kräver samuttryck av Sox 10) eftersom dess inaktivering leder till dedifferentiering av Schwann-cellerna.
Klinisk signifikans
Charcot-Marie-Tooths sjukdom (CMT), Guillain-Barrés syndrom (GBS, akut inflammatorisk demyeliniserande polyradikulopati-typ), schwannomatos och kronisk inflammatorisk demyeliniserande polyneuropati (CIDP), spetälska och Zika-virus är alla neuropatier som involverar Schwann-celler.
Transplantation
Ett antal experimentella studier sedan 2001 har implanterat Schwann-celler i ett försök att inducera remyelinisering hos patienter med multipel skleros . Under de senaste två decennierna har många studier visat positiva resultat och potential för Schwann-celltransplantation som en terapi för ryggmärgsskada, både för att underlätta återväxt och myelinisering av skadade CNS-axoner. Schwann-cellstransplantationer i kombination med andra terapier såsom kondroitinas ABC har också visat sig vara effektiva vid funktionell återhämtning från ryggmärgsskada.
Se även
- Elektrofysiologi
- Hodgkin-Huxley modell
- Mesaxon
- Neurotransmission
- Luktskyddande cell
- Schwannoma
- Lista över mänskliga celltyper härledda från bakterielagren
externa länkar
- Diagram på clc.uc.edu
- Histologibild: 21301loa – Histology Learning System vid Boston University — "Ultrastructure of the Cell: myelinated axon and Schwann cell"
- Cellcentrerad databas—Schwann-cell

