Birt–Hogg–Dubé syndrom
 | |
| Birt–Hogg–Dubés syndrom | |
|---|---|
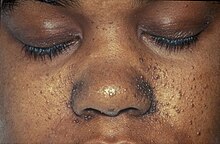
| De karakteristiska fibrofolliculomen för Birt–Hogg–Dubés syndrom ses i en persons ansikte. | |
| Specialitet |
Medicinsk genetik |
Birt–Hogg–Dubé syndrom ( BHD ), även Hornstein–Birt–Hogg–Dubé syndrom , Hornstein–Knickenbergs syndrom och fibrofolliculom med trichodiscomas och acrochordons är en mänsklig autosomal dominant genetisk störning som kan orsaka mottaglighet för njurcancer , njur- och lungcancer . och icke-cancerösa tumörer i hårsäckarna , så kallade fibrofolliculom . Symtomen som ses i varje familj är unika och kan inkludera vilken kombination som helst av de tre symtomen. Fibrofolliculom är den vanligaste manifestationen, som finns i ansiktet och övre bålen hos över 80 % av personer med BHD över 40 år. Lungcystor är lika vanliga (84 %), men endast 24 % av personer med BHD upplever så småningom en kollaps lunga ( spontan pneumothorax ). Njurtumörer, både cancerösa och godartade, förekommer hos 14–34 % av personer med BHD; associerade njurcancer är ofta sällsynta hybridtumörer.
Alla dessa tillstånd som uppstår i en familj kan indikera en diagnos av Birt-Hogg-Dubé-syndrom, även om det endast bekräftas av ett genetiskt test för en mutation i FLCN -genen, som kodar för proteinet folliculin . Även om dess funktion inte är helt klarlagd, verkar det vara en tumörsuppressorgen som begränsar celltillväxt och -delning. Versioner av FLCN har hittats i andra djur, inklusive fruktflugor , schäfer , råttor och möss . Sjukdomen upptäcktes 1977, men sambandet med FLCN klargjordes inte förrän 2002, efter att njurcancer, kollapsade lungor och lungcystor var alla definitivt kopplade till BHD.
Birt–Hogg–Dubés syndrom kan manifestera sig på samma sätt som andra sjukdomar, vilket måste uteslutas vid diagnos. Dessa inkluderar tuberös skleros , som orsakar hudskador som liknar fibrofolliculom, och Von Hippel-Lindaus sjukdom , som orsakar ärftlig njurcancer. När diagnosen väl har diagnostiserats behandlas personer med BHD förebyggande, med övervakning av njurar och lungor med hjälp av medicinsk bildbehandling . Fibrofolliculom kan avlägsnas kirurgiskt och pneumothorax och njurcancer behandlas enligt normal vårdstandard. Dermatologiska undersökningar, halsultraljud och koloskopier bör också övervägas [1] .
tecken och symtom
Hud
Birt–Hogg–Dubés syndrom påverkar huden och ökar risken för tumörer i njurar och lungor. Tillståndet kännetecknas av flera icke-cancerösa, kupolformade tumörer i hårsäckarna ( fibrofolliculomas ) , särskilt i ansiktet, på halsen och mer sällan den övre delen av bröstet. Fibrofolliculomen beskrivs generellt som att de har en ogenomskinlig vit färg eller en gulaktig ton och har en vaxartad, slät konsistens. Tumörerna finns alltid på och runt näsan och på och bakom ytterörat . Vanligtvis uppträder de först i 20- eller 30-årsåldern och finns hos mer än 80 % av personer med syndromet över 40 år. Tumörerna blir större och fler med tiden. Tumörer skiljer sig mellan individer; de kan verka sammanslagna i plack , likna en comedo med en keratinplugg eller inkludera epidermoida cystor . Ett stort antal tumörer i ansiktet kan associeras med hyperseborré (onormalt förhöjd talgproduktion ). Närvaron av fibrofolliculom i en persons ansikte kan orsaka betydande psykisk ångest .
Andra tumörer kan inkludera trichodiscomas (tumörer i hårskivan , som kan vara identiska med fibrofolliculom), angiofibroma och perifollikulära fibromer . Angiofibromer är dock vanligare vid tuberös skleros. Tillsammans med tumörerna ses andra hudåkommor hos personer med Birt–Hogg–Dubés syndrom. Ungefär 40 % av personer eller familjer med sjukdomen har papler i munnen, som kan sitta på kinderna ( munslemhinnan ), tungan, tandköttet eller läpparna. Antingen vita eller slemhinnafärgade, de är diskreta, små och mjuka och består av fibrös vävnad täckt av förtjockat epitel . Kollagenom i huden finns också i vissa familjer. Många personer med BHD har hudskador som verkar vara akrokordon (hudtaggar), men kan istället vara fibrofolliculom. Dessa lesioner finns vanligtvis i armhålan , på ögonlocken och i hudveck. Inte alla individer utvecklar ansiktstumörerna; vissa familjer med mutationen som orsakar BHD utvecklar endast njurtumörer eller spontan pneumothorax.
Njurar

Personer över 20 år med BHD har en ökad risk att utveckla långsamt växande njurtumörer ( kromofobt njurkarcinom respektive njuronkocytom ), njurcystor och möjligen tumörer i andra organ och vävnader. Dessa tumörer förekommer ofta i båda njurarna och på flera platser i varje njure. Det genomsnittliga antalet njurtumörer som hittats hos en person med BHD är 5,3, även om upp till 28 tumörer har hittats. Hybrid onkocytom/kromofob karcinom, som hittas i 50 % av fallen, är den vanligaste cancerformen, följt av kromofob njurkarcinom, klarcellig njurkarcinom, njuronkocytom och papillär njurcellscancer . Personer över 40 år och män är mer benägna att utveckla njurtumörer, som diagnostiseras vid en medianålder av 48. Njurcancer associerad med BHD har diagnostiserats hos personer i åldrarna så unga som 20 år.
I allmänhet löper personer med detta syndrom ungefär sju gånger risken för njurcancer jämfört med den opåverkade befolkningen. Uppskattningar av incidensen bland personer med sjukdomen varierar från 14 till 34 %. I sällsynta fall är det associerat med klarcellig njurcellscancer och papillär njurcellskarcinom . Om det utvecklas hos någon med BHD, uppstår njurcellscancer senare i livet och har en dålig prognos. Även om de typer av tumörer som vanligtvis förknippas med BHD anses vara mindre aggressiva, har fall av avancerad eller metastaserad njurcancer observerats hos personer med syndromet. Både godartade och cancerösa tumörer kan minska njurfunktionen med tiden när de växer sig större.
Lungor
Tillsammans med fibrofolliculom och njurtumörer utvecklar drabbade individer ofta cystor ( blåsor eller bullae ) i den sub pleurala lungbasen eller det intraparenkymala utrymmet som kan brista och orsaka en onormal ansamling av luft i brösthålan ( pneumothorax ), vilket kan resultera i kollapsen av en lunga. Cystorna ger inga andra symtom och lungfunktionen är vanligtvis normal. Mer än 83 % av personer med BHD har cystor, men syndromet orsakar inte tillstånd som progressiv kronisk obstruktiv lungsjukdom eller generaliserad andningssvikt , även om det orsakar emfysem . Spontan, ibland återkommande, pneumothorax förekommer mycket oftare och i en yngre ålder med BHD än hos den opåverkade befolkningen. Omkring 24 % av personer med sjukdomen har minst en spontan pneumothorax, 30 gånger förekomsten hos opåverkade personer. Även om pneumothorax orsakad av BHD ofta inträffar i medelåldern, vid en medianålder av 38, har 17 % av de drabbade personerna en spontan pneumothorax innan de fyller 40. Pneumothorax har setts hos personer så unga som 7 och 16 års ålder. Vissa familjer har en form av BHD som bara påverkar lungorna.
Andra organ
Sköldkörtelknölar har associerats med Birt-Hogg-Dubé-fenotypen, som finns hos 65 % av individerna och 90 % av familjerna med syndromet. Ett samband mellan BHD och sköldkörtelcancer har dock inte styrkts. Andra tillstånd har rapporterats vara associerade, men kanske inte orsakas av mutationen i FLCN eller kanske inte alls är relaterade. Dessa inkluderar multinodulär struma , medullärt sköldkörtelkarcinom , parotidonkocytom , kolonpolypos , bindvävsnevus , lipom , angiolipomas , bisköldkörteladenom, fläckig korioretinopati, neurotekeom , meningiom , angiofibroma i ansiktet, snitt i ansiktet , angiofibroma , slemhinnor , slemhinnor yoma , bröstcancer, tonsillcancer , kolorektal cancer , sarkom i benet, lungcancer, melanom , dermatofibrosarcoma protuberans , basalcellscancer , kutant leiomyosarkom och skivepitelcancer .
Patofysiologi
Genetik

En association med genen för follikulin ( FLCN ) rapporterades första gången 2002. Denna 14- exon -gen är belägen på den korta armen av kromosom 17 (17p11.2) och har en cytosinrik region i exon 11 som är särskilt känslig för mutation. Den vanligaste mutationen i denna region är insättning eller deletion av en cytosinrest, som finns i 53 % av BHD-drabbade familjer. Ingen signifikant skillnad har hittats i symtomen som upplevs av familjer med en insättning på den platsen jämfört med de som har en deletion, men mutationer i FLCN associerade med BHD-syndrom är heterogena och är ofta nonsensmutationer eller ramskiftningsmutationer som orsakar tidig trunkering av proteinprodukten vid karboxiterminalen . Mycket sällan observeras missense-mutationer . De mutationer i FLCN-genen som orsakar Birt–Hogg–Dubés syndrom är könslinjemutationer, vilket innebär att de förekommer i varje cell i kroppen och kan överföras till framtida generationer. Dessa mutationer överförs ofta från en generation till nästa på ett autosomalt dominant sätt, men kan uppstå som en ny mutation hos en individ utan tidigare familjehistoria (en de novo mutation ). Barn till en drabbad förälder har vardera 50 % chans att ha sjukdomen. BHD har mycket hög penetrans . En korrelation mellan olika FLCN- genotyper och fenotyper har inte upptäckts.
Fungera
FLCN skapar ett protein, folliculin, som har två isoformer . Det verkar fungera som en tumörsuppressor och uttrycks starkt i huden, distala nefroner och typ I-pneumocyter . Det har också hittats i öreskärlskörteln , hjärnan, bröstet , bukspottkörteln , prostatan och äggstockarna . Tumörsuppressorer förhindrar normalt celler från att växa och dela sig för snabbt eller på ett okontrollerat sätt. Mutationer i FLCN -genen kan störa follikulins förmåga att begränsa celltillväxt och -delning, vilket leder till bildandet av icke-cancer- och cancertumörer. Nyligen genomförda studier tyder på att folliculin åstadkommer denna funktion genom sin inblandning i cellulär metabolism , möjligen genom modulering av mTOR- vägen (däggdjursmålet för rapamycin ) och/eller oxidativ fosforylering i mitokondrier . Folliculin interagerar med FNIP1 och FNIP2 (FLCN-interagerande protein) för att bilda ett komplex med AMP-aktiverat proteinkinas . Folliculins deltagande i mTOR-vägen kan förklara likheten i fenotyp mellan BHD-syndrom, Cowdens syndrom, tuberös skleros och Peutz-Jeghers syndrom .
De flesta av de cancerframkallande mutationerna gör att proteinet trunkeras vid karboxiterminalen. Den C-terminala änden av follikulin har visat sig vara den domän genom vilken den interagerar med FNIP1, och därmed möjligen mTOR-vägen. FLCN är mycket bevarat hos ryggradsdjur - det är mycket likt mellan många ryggradsdjursarter. Den 508:e aminosyran , normalt lysin , påverkas av en missense-mutation hos vissa personer med BHD. Lysinet vid denna position visar sig vara konserverat mellan ryggradslösa och ryggradsdjur ortologer av follikulin, vilket indikerar att det är viktigt för proteinets funktion.

Personer med BHD föds med en muterad kopia av FLCN -genen i varje cell. Haploinsufficiens - att bara ha en funktionell kopia av FLCN- genen - räcker för att orsaka fibrofolliculom och lungcystor, även om en kopia av genen är tillräckligt för att hålla njurcellerna i schack. Under en persons livstid kan slumpmässiga mutationer inaktivera den normala kopian av genen i en undergrupp av celler. När detta inträffar är resultatet att dessa celler inte har några funktionella kopior av FLCN- genen, vilket gör att cellerna växer utom kontroll. Denna förlust av heterozygositet är en vanlig mekanism vid cancer, och den upptäcks ofta i njurcancer associerade med BHD. De molekylärgenetiska defekterna i njurtumörer hos personer med BHD skiljer sig från två andra liknande njurtumörer, kromofobe njurcellscancer och njuronkocytom . BHD-associerad tumörbildning skiljer sig mellan njuren, där förlust av FLCN- heterozygositet är ansvarig för cancer, och huden, där FLCN är starkt uttryckt i heterozygoter. FLCN har visat sig vara överuttryckt i fibrofolliculomvävnad och ha mycket låga nivåer av uttryck i drabbade njurar. Dessutom har mTOR-vägen visat sig vara aktiverad i tumörvävnad från både människor och möss.
Njurcystogenes och tumörbildning i BHD har visat sig drivas av den konstitutiva aktiveringen av TFEB.
Diagnos
BHD kan föreslås av kliniska fynd men diagnostiseras definitivt genom molekylär genetisk testning för att upptäcka mutationer i FLCN -genen. Den klassiska kliniska triaden inkluderar benigna utväxter av hårsäckar, lungcystor och spontan pneumothorax och bilaterala, multifokala njurtumörer.
Klinisk triad
De kutana manifestationerna av BHD beskrevs ursprungligen som fibrofolliculom (onormala utväxter av en hårsäck), trichodiscomas (hamartomatösa lesioner med en hårsäck i periferin, ofta påträffad i ansiktet) och akrokordon (hudtaggar). Kutana manifestationer bekräftas av histologi . De flesta individer (89%) med BHD visar sig ha flera cystor i båda lungorna, och 24% har haft en eller flera episoder av pneumothorax. Cystorna kan upptäckas genom CT-skanning av bröstet . Njurtumörer kan manifestera sig som flera typer av njurcellscancer, men vissa patologiska subtyper (inklusive kromofober , onkocytom och onkocytiska hybridtumörer) är vanligare. Även om det ursprungliga syndromet upptäcktes på basis av kutana fynd, kan individer med BHD endast manifestera lung- och/eller njurfynd utan några hudskador. Även om dessa tecken indikerar BHD, bekräftas det endast med ett genetiskt test för FLCN- mutationer.
Genetisk testning
FLCN- mutationer detekteras genom sekvensering i 88 % av probanderna med detta syndrom. Det betyder att vissa personer med den kliniska diagnosen har mutationer som inte går att upptäcka med nuvarande teknologi, eller att mutationer i en annan för närvarande okänd gen kan vara ansvarig för en minoritet av fallen. Dessutom testas även amplifieringar och deletioner i exoniska regioner. Genetisk testning kan vara användbar för att bekräfta den kliniska diagnosen och för att ge ett sätt att fastställa andra riskpersoner i en familj även om de ännu inte har utvecklat BHD-symtom.
Differentialdiagnos
BHD kan vara svårt att diagnostisera enbart utifrån symtom, eftersom ärftlig njurcancer, pneumothorax och kutana tumörer förekommer med andra syndrom. Ärftliga bilaterala, multifokala njurtumörer liknande de som ses vid BHD kan förekomma med von Hippel-Lindaus sjukdom (klarcellig njurcellscancer), ärftlig papillär njurcancer (papillär njurcellskarcinom) och ärftlig leiomyomatos och njurcellscancersyndrom . De differentieras med undersökning av tumörernas histologi.
Ärftlig återkommande pneumothorax eller lungcystor är förknippade med Marfans syndrom , Ehlers-Danlos syndrom , tuberös skleroskomplex , alfa1-antitrypsinbrist och cystisk fibros . Icke-ärftlig återkommande pneumothorax och/eller lungcystor kan förekomma med Langerhans cell histiocytos och lymfangioleiomyomatosis . Dessa tillstånd skiljer sig från BHD genom att undersöka patienthistorien och utföra en fysisk undersökning. kan det vara nödvändigt att utesluta pulmonell eller thorax endometrios .
Även om fibrofolliculom är unika för BHD, kan de uppvisa ett tvetydigt utseende och måste bekräftas histologiskt. Andra sjukdomar kan efterlikna de dermatologiska manifestationerna av BHD, inklusive tuberös skleroskomplex, Cowdens syndrom , familjär trichoepitheliom och multipel endokrin neoplasi typ 1 . Tuberös skleros måste särskiljas eftersom båda sjukdomarna kan uppvisa angiofibromer i ansiktet, även om de är vanligare vid tuberös skleros.
Förvaltning
De olika manifestationerna av BHD kontrolleras på olika sätt. Fibrofolliculomen kan avlägsnas kirurgiskt, genom curettage , rakexcision , återuppbyggnad av huden eller laserablation ; Detta är dock inte en permanent lösning, eftersom tumörerna ofta återkommer. Hudundersökning var 6-12:e månad på grund av risk för melanom . Sköldkörtel/parotis ultraljud bör övervägas årligen . Koloskopier bör övervägas . Njur- och lungsymtomen hanteras förebyggande: datortomografi, ultraljud eller MRI av njurarna rekommenderas regelbundet, och familjemedlemmar rekommenderas att inte röka. MRT är den föredragna metoden för övervakning av njurarna hos personer med BHD eftersom de inte medför samma risk för strålningskomplikationer som datortomografi och är känsligare än ultraljud. Rökare med Birt–Hogg–Dubé har svårare lungsymtom än icke-rökare. Även om nefrektomi ibland är indicerat, avlägsnas njurtumörer i fall av BHD ofta utan att ta hela njuren, i en partiell nefrektomi . Knockout-musstudier har visat att administrering av rapamycin kan mildra effekterna av FLCN- mutationer på njurarna och förbättra prognoser för njurcancer på grund av follikulins interaktion med mTOR-vägen.
Epidemiologi
Sjukdomen har rapporterats i mer än 100 familjer över hela världen, även om vissa källor citerar upp till 400 familjer, och den ärvs i ett autosomalt dominant mönster. Det anses vara underdiagnostiserat på grund av variationen i dess uttryck. Mönstret av mutationer och spektrum av symtom är heterogena mellan individer. Mindre allvarliga hudfenotyper ses hos kvinnor och personer av båda könen som har sent inträdande hudsymtom.
Patientregister
Birt-Hogg-Dubé syndrom patienter, familjer och vårdgivare uppmuntras att gå med i NIH Rare Lung Diseases Consortium Contact Registry . Detta är en integritetsskyddad webbplats som tillhandahåller uppdaterad information för individer som är intresserade av de senaste vetenskapliga nyheterna, prövningar och behandlingar relaterade till sällsynta lungsjukdomar.
Historia
Syndromet beskrevs först väl 1977 av tre kanadensiska läkare, Arthur R. Birt, Georgina R. Hogg och William J. Dubé. Det tidigaste fallet av möjlig BHD i den medicinska litteraturen publicerades av Burnier och Rejsek 1927, som beskrev ett fall av perifollikulära fibromer i en 56-årig kvinnas ansikte. Trichodiscomas beskrevs först 1974 av HS Zackheim och H. Pinkus, men associerades inte med BHD förrän Birt, Hogg och Dubé. Det första fallet av BHD med de systemiska symtomen beskrevs av Hornstein och Knickenberg och hittades hos två syskon och deras far, som alla uppvisade kolonpolyper och de karakteristiska fibrofolliculomen. Även om syskonen inte hade njur- eller lungsymtom, hade deras pappa cystor i sina lungor och njurar. Hornstein-Knickenbergs syndrom är ett numera avskaffat namn för de ärftliga fibrofolliculomen som är inneboende till BHD.
Birt, Hogg och Dubé undersökte en familj med ärftlig sköldkörtelcancer och upptäckte att många av medlemmarna hade fibrofolliculom, trichodiscomas och acrochordons, som blev definierade som de klassiska symtomen på sjukdomen med samma namn. Det första fallet av spontan pneumothorax i samband med BHD upptäcktes 1986; det första fallet av njurcancer följde 1993, och förekomsten av lungcystor hos personer med BHD bekräftades 1999. Personer med BHD ansågs en gång ha högre risk för kolorektala polyper och neoplasmer , men detta har motbevisats. BHD Foundation stöder forskning om syndromet och håller regelbundna symposier i BHD och relaterade sjukdomar för forskare, läkare och familjemedlemmar.
Andra djur
Gener relaterade till FLCN och sjukdomar som liknar BHD har hittats hos hundar, fruktflugor, råttor och möss. Hos schäferhundar orsakar missense-mutationer i hundortologen av FLCN en liknande fenotyp som human BHD - njurcancer (i detta fall multifokalt njurcystadenocarcinom) och hudtumörer (nodulär dermatofibros). De hade ett liknande mönster av tumörbildning som human BHD genom att hudskadorna var heterozygota för FLCN- mutationen, och njurtumörerna orsakades sannolikt av förlust av heterozygositet. Tyska schäferhonor med en FLCN- mutation är också benägna att få livmoderleiomyom .
En homolog av FLCN som kallas DBHD har upptäckts i den vanliga fruktflugan, Drosophila melanogaster . Minskad uttryck av DBHD resulterar i förlust av manliga könslinjestamceller (GSC), vilket tyder på att DBHD krävs för manligt GSC-underhåll i flugtestis. Vidare DBHD GSC-underhållet nedströms eller parallellt med JAK/STAT- och Dpp-signaltransduktionsvägarna, vilket tyder på att BHD reglerar tumörbildning genom att kontrollera stamceller i mänskliga {Singh et al. 2006}
En rad råttor med ärftlig njurcancer utvecklades av japanska forskare. De har en mutation i FLCN- homologen som producerar ett trunkerat protein, även om de inte utvecklar de hud- eller lungsymtom som ses hos människor. Heterozygoter har njuravvikelser som ses mycket tidigt i livet som utvecklas till klarcells- och hybridtumörer, vilket avsevärt förkortar djurens livslängd; de är också benägna att få klarcellshyperplasi av endometrie och spottkörtel samt rabdomyolys . Homozygoter överlever inte till födseln. FLCN -gen av vildtyp tillsattes räddades fenotypen.
Knockout-möss har skapats för en njurcancer som orsakar mutation av BHD; heterozygoter utvecklar njurcystor och tumörer som leder till njursvikt inom tre veckor efter födseln. I dessa möss aktiverades mTOR-vägen olämpligt, vilket indikerar att mushomologen av FLCN spelar en reglerande roll i denna väg. Rapamycin räddade delvis fenotypen genom att reglera mTOR. Homozygoter dör i livmodern .
Citat
Bibliografi
- Ayo, Dereje S.; Aughenbaugh, GL; Yi, ES; Hand, JL; Ryu, JH (2007), "Cystic Lung Disease in Birt-Hogg-Dubé Syndrome", Chest , 132 (2): 679–84, doi : 10.1378/chest.07-0042 , PMID 17505035
- Birt, AR; Hogg, GR; , "Hereditary multiple fibrofolliculomas with trichodiscomas and acrochordons", Archives of Dermatology , 113 (12): 1674–7, doi : 10.1001/archderm.113.12.1674 , 896 896 896 .
- BHD Foundation , 2013, arkiverad från originalet 11 juni 2021 , hämtad 17 juli 2013
- Chan-Smutko, Gayun (2012), "Genetic Testing by Cancer Site", The Cancer Journal , 18 (4): 343–9, doi : 10.1097/PPO.0b013e31826246ac , PMID 22846736
- Coleman, Jonathan A; Russo, Paul (2009), "Hereditär och familjär njurcancer", Current Opinion in Urology , 19 (5): 478–85, doi : 10.1097/MOU.0b013e32832f0d40 , PMID 19584731
- Devine, Megan Stuebner; Garcia, Christine Kim (2012 ) , "Genetic Interstitial Lung Disease", Clinics in Chest Medicine , 33 (1): 95–110, doi : 10.1016/j.ccm.2011.11.001 , PMC 3292740 , PM3524292
- Furuya, M.; Nakatani, Y. (2012), "Birt-Hogg-Dube syndrom: Clinicopathological features of the lung", Journal of Clinical Pathology , 66 (3): 178–86, doi : 10.1136/jclinpath-2012-201200 , PMC 35,95,9 PMID 23223565
- "Birt-Hogg-Dubé syndrome" , Genetics Home Reference , US National Library of Medicine, januari 2013 , hämtad 13 juli 2013
- "Birt-Hogg-Dubé syndrome: Educational resources" , Genetics Home Reference , NIH, 22 juli 2013, arkiverad från originalet den 15 mars 2016 , hämtad 25 juli 2013
- Grant, LA; Babar, J.; Griffin, N. (2009), "Cystor, cavities, and honeycombing in multisystem disorders: Differential diagnosis and findings on thin-section CT", Clinical Radiology , 64 (4): 439–48, doi : 10.1016/j.crad. 2008.09.015 , PMID 19264190
- James, William D.; Berger, Timothy; Elston, Dirk (2011), Andrew's Diseases of the Skin: Clinical Dermatology (11:e upplagan), Elsevier Health Sciences, ISBN 978-1-4377-3619-9
- Kniffin, Cassandra L. (22 augusti 2012), "Birt-Hogg-Dube syndrom, BHD" , Online Mendelian Inheritance in Man , Johns Hopkins University, arkiverad från originalet den 10 mars 2017 , hämtad 13 juli 2013
- Liu, Wei; Chen, Zhi; Ma, Yansen; Wu, Xiaochun; Jin, Yaping; Hou, Steven (2013), White-Cooper, Helen (red.), "Genetic Characterization of the Drosophila Birt-Hogg-Dubé Syndrome Gene", PLOS ONE , 8 (6): e65869 , Bibcode : 2013PLoSO ... 865869L , doi : 10.1371/journal.pone.0065869 , PMC 3684598 , PMID 23799055
- ( 2011), "Genetics of Familial Renal Cancers", Nephron Experimental Nephrology , 118 (1): e21–6, doi : 10.1159/000320892 , PMID 21071978 1 , S2464ID
- Menko, Fred H; Van Steensel, Maurice AM; Giraud, Sophie; Friis-Hansen, Lennart; Richard, Stéphane; Ungari, Silvana; Nordenskjöld, Magnus; Hansen, Thomas vO; Solly, John; Maher, Eamonn R; European Bhd, Consortium (2009), "Birt-Hogg-Dubé syndrom: Diagnosis and management", The Lancet Oncology , 10 (12): 1199–206, doi : 10.1016/S1470-2045(09 ) 70188-769 ,
- BHD Foundation , National Organization for Rare Disorders, 2013, arkiverad från originalet den 3 november 2013 , hämtad 25 juli 2013
- Nickerson, Michael L.; Warren, Michelle B.; Toro, Jorge R.; Matrosova, Vera; Glenn, Gladys; Turner, Maria L.; Duray, Paul; Merino, Maria; Choyke, Peter; et al. (2002), "Mutationer i en ny gen leder till njurtumörer, lungväggsdefekter och godartade tumörer i hårsäcken hos patienter med Birt-Hogg-Dubé-syndromet", Cancer Cell , 2 (2 ) : 157–64 , doi : 10.1016/S1535-6108(02)00104-6 , PMID 12204536
- Palmirotta, Raffaele; Savonarola, Annalisa; Ludovici, Giorgia; Donati, Pietro; Cavaliere, Francesco; De Marchis, Maria Laura; Ferroni, Patrizia; Guadagni, Fiorella (mars 2010), "Association between Birt Hogg Dubé syndrome and cancer predisposition", Anticancer Res. , 30 (3): 751–7, PMID 20392993
- Reese, Erin; Sluzevich, Jason; Kluijt, Irma; Teertstra, H. Jelle; De Jong, Daphne; Horenblas, Simon; Ryu, Jay (5 oktober 2009), "Birt-Hogg-Dubé Syndrome" , i Riegert-Johnson, Douglas L; Boardman, Lisa A; Hefferon, Timothy; Roberts, Maegan (red.), Cancer Syndromes , Bethesda, MD: National Center for Biotechnology Information, PMID 21249760
- Riegert-Johnson, DL, "Birt-Hogg-Dube" , Familial Cancer Syndromes , NCBI , hämtad 21 juli 2009
- Sudarshan, Sunil; Karam, Jose A.; Brugarolas, James; Thompson, R. Houston; Uzzo, Robert; Rini, Brian; Margulis, Vitaly; Patard, Jean-Jacques; Escudier, Bernard; Linehan, W. Marston (2013), "Metabolism of Kidney Cancer: From the Lab to Clinical Practice", European Urology , 63 (2): 244–51, doi : 10.1016/j.eururo.2012.09.054 , PMC 3709870 , PMID 23063455
- Toro, Jorge R. (9 september 2008), "Birt-Hogg-Dubé Syndrome" , i Pagon, Roberta A; Adam, Margaret P; Bird, Thomas D; Dolan, Cynthia R; Fong, Chin-To; Smith, Richard JH; Stephens, Karen (red.), GeneReviews , University of Washington, PMID 20301695
- Toro, JR; Wei, MH; Glenn, GM; Weinreich, M; Toure, O; Vocke, C; Turner, M; Choyke, P; Merino, MJ; et al. (2008), "BHD-mutationer, kliniska och molekylärgenetiska undersökningar av Birt-Hogg-Dube syndrom: En ny serie med 50 familjer och en översyn av publicerade rapporter", Journal of Medical Genetics , 45 (6): 321–31, doi : 10.1136/jmg.2007.054304 , PMC 2564862 , PMID 18234728
- Verine, Jérôme; Pluvinage, Amélie; Bousquet, Guilhem; Lehmann-Che, Jacqueline; De Bazelaire, Cédric; Soufir, Nadem; Mongiat-Artus, Pierre (2010), "Hereditary Renal Cancer Syndromes: An Update of a Systematic Review", European Urology , 58 (5): 701–10, doi : 10.1016/j.eururo.2010.08.031 , PMID 250817388
externa länkar

