Svampig degeneration av centrala nervsystemet
| Svampig degeneration av det centrala nervsystemet | |
|---|---|
| Andra namn | Canavans sjukdom, Van Bogaert-Bertrand-typ, Aspartoacylasbrist |
 | |
| Magnetisk resonanstomografi som visar dysmyelinisering, en möjlig indikator på Canavans sjukdom | |
| Specialitet | Neurologi |
| Symtom | Hypotoni, makrocefali, synförlust, motoriska reflexdefekter, svårigheter att andas och svälja |
| Vanligt debut | 3-6 månaders ålder |
| Varaktighet | Terminal |
| Typer | Infantil, medfödd, juvenil |
| Orsaker | Genetisk (autosomal recessiv) |
| Riskfaktorer | Familjehistoria (genetik) |
| Diagnostisk metod | Neuroimaging, urinundersökning |
| Förebyggande | DNA-analys, prenatal analys |
| Behandling | Endast palliativa åtgärder |
| Medicin | N/A |
Svampig degeneration av centrala nervsystemet , även känd som Canavans sjukdom , Van Bogaert-Bertrand-typ eller brist på aspartoacylas (AspA) , är en sällsynt autosomal recessiv neurodegenerativ störning . Det tillhör en grupp genetiska störningar som kallas leukodystrofier , där tillväxten och underhållet av myelinskidan i det centrala nervsystemet ( CNS) försämras. Det finns tre typer av svampig degeneration: infantil, medfödd och juvenil, med juvenil som den allvarligaste typen. Vanliga symtom hos spädbarn inkluderar bristande motorik , svag muskeltonus och makrocefali . Det kan också åtföljas av svårigheter att äta och svälja, kramper och sömnstörningar . Drabbade barn dör vanligtvis före 10 års ålder, men medellivslängden kan variera.
Orsaken till svampig degenerering av CNS är mutationen i en gen som kodar för aspartoacylas (AspA) , ett enzym som hydrolyserar N-acetylasparaginsyra (NAA) . I frånvaro av AspA ackumuleras NAA och resulterar i svampig degeneration. De exakta patofysiologiska orsakerna till sjukdomen är för närvarande oklara, men det finns teorier under utveckling. Svampig degeneration kan diagnostiseras med neuroimaging tekniker och urinundersökning . Det finns ingen aktuell behandling för svampig degeneration, men forskning som använder genterapi för att behandla sjukdomen pågår. Svampig degeneration visar sig vara vanligare bland Ashkenazi-judar , med en förekomst på 1/6000 bland denna etniska grupp.
Kliniska symtom
Svampig degeneration av CNS klassificeras i tre typer: infantil, juvenil och medfödd; baserat på debutåldern och symtomens svårighetsgrad.
Infantil typ
Den infantila typen är den vanligaste typen av svampig degeneration av CNS. Vanligtvis verkar drabbade spädbarn normala under de första månaderna av livet. Debutåldern är cirka 6 månader, då spädbarn börjar utveckla märkbara psykomotoriska defekter . Olika motoriska färdigheter som att vända och stabilisera huvudrörelser påverkas. Hypotoni och makrocefali observeras också under de första månaderna.
Under den senare delen av det första året reagerar de flesta barns ögon inte på visuella stimuli , med episodiska saccadiska ögonrörelser observerade, vilket gör de flesta barn blinda under det andra året.
Symtomen i det terminala stadiet av sjukdomsutveckling är svettning, kräkningar , hypertermi , kramper och hypotoni , vilket vanligtvis leder till att barnet dör. Den förväntade livslängden för drabbade spädbarn varierar, men de flesta spädbarn lever inte över tio års ålder.
Medfödd typ
Debutåldern är vanligtvis några dagar efter födseln i den medfödda typen. Graviditet och förlossning påverkas inte och barnet föds med ett normalt utseende och inga hälsoproblem. Däremot kan drabbade spädbarn bli slöa under de följande dagarna och få rörelser som att suga och svälja svåra. När sjukdomen fortskrider kan patienter ha nedsatt muskeltonus och inaktivering av Moro reflex , även känd som skrämselreflex. Detta kan leda till utvecklingen av Cheyne Stokes andning efter några veckor eller till och med dagar efter förlossningen, vilket kan vara dödligt.
Ungdomstyp
Debutåldern för den unga typen är cirka fem års ålder. De flesta patienter med den unga typen överlever till sen tonåren . Drabbade småbarn utvecklar vanligtvis progressivt cerebellärt syndrom och mental försämring, som följs av synförlust, optisk atrofi och generaliserad spasticitet . Till skillnad från den infantila formen finns det ingen makrocefali uppvisad.
Patofysiologi
Även om de patofysiologiska orsakerna till CD-symtom fortfarande är oklara, utvecklas teorier om orsakerna till myeliniseringsproblem, gelatinös kortikal vit substans och anfall.
Problem med myelinisering
Molecular Water Pump (MWP) och osmolytobalans
Ökat cerebrospinalvätsketryck (CSF) och intramyeliniskt ödem hos CD-patienter tyder på att det finns en effektiv MWP i hjärnan. MWP är ett membranprotein som ansvarar för att pumpa vattenmolekyler, tillsammans med lösta NAA-molekyler, från det intraneuronala utrymmet till det interstitiella utrymmet . Hos friska individer transporteras NAA först ner i koncentrationsgradienten genom MWP från neuroner till det interstitiella utrymmet och hydrolyseras därefter av AspA i angränsande oligodendrocyter .
Hos patienter med CD, är det teorier om att AspA-brist orsakar ackumulering av NAA i det interstitiella utrymmet, vilket inducerar en osmolytobalans och ackumulering av vatten i det interstitiella utrymmet. Detta ökar det hydrostatiska trycket mellan interlamellära utrymmen och extracellulära periaxonala och parenkymatösa utrymmen, vilket lossar de täta förbindelserna mellan dem, vilket orsakar intramyeliniskt ödem. Efterföljande demyelinisering bidrar möjligen till lediga utrymmen i den vita substansen eller svampig degenerering.
Dysmyelinisering
NAA-härledda acetater är involverade i syntesen av fettsyror , som sedan införlivas i myelinlipider . Det antas att hos CD-patienter minskar AspA-brist NAA-härledda acetater och följaktligen minskar syntesen av myelinassocierade lipider. Detta leder till dysmyelinisering , vilket främjar bildandet av vakuoler i interstitiellt utrymme och svampig degenerering. Det har dock visat sig att svampig degeneration inte direkt orsakas av den störda syntesen av myelin. Djurmodeller visar att myelinisering fortfarande kan förekomma hos arter som saknar AspA, möjligen på grund av parallella vägar för myelinisering under de inledande stadierna av myelinogenesen .
Proteinvikning och stabilisering
Brist på AspA sänker uttrycket av acetylkoenzym A (CoA) i celler, vilket kan vara ansvarigt för stabilisering och korrekt veckning av proteiner . Detta leder till proteinnedbrytning, med särskilt stor effekt i oligodendrocyter. I djurstudier av arter med brist på AspA har proteinnedbrytning i oligodendrocyter visat sig orsaka allvarlig förlust av myelinproteiner.
Gelatinös subkortikal vit substans
Bristen på AspA, som är avgörande i oligodendrocyter för att producera NAA-deriverat acetat, leder till bristande reglering av den genetiska strukturen och uttrycket i dessa celler. Detta resulterar i att oligodendrocyter dör, vilket inducerar neuronal skada och bildandet av vakuoler i den subkortikala materien . Dessa vakuoler bidrar till bildandet av subkortikal vit substans med gelatinös textur som finns hos många CD-patienter.
Kramper och neurodegeneration
De patofysiologiska orsakerna till anfall och neurodegeneration hos CD-patienter beror sannolikt på oxidativ stress som genereras av NAA-ackumulering. Det postuleras att NAA främjar oxidativ stress genom att främja reaktiva syrearter , samt minska icke-enzymatiska antioxidantförsvar . NAA påverkar också flera antioxidantenzymer, såsom katalas och glutationperoxidas , vilket försämrar avgiftningen av väteperoxid . Nyligen genomförda djurstudier har visat att kronisk oxidativ stress kan orsaka dysfunktion i mitokondrier , vilket gör hjärnan mer mottaglig för epileptiska anfall .
Diagnos
Canavans sjukdom upptäcks initialt genom uppkomsten av symtom, men ytterligare undersökningar behövs för en definitiv diagnos. Neuroavbildningstekniker som datortomografi (CT) eller magnetisk resonanstomografi (MRT) används vanligtvis för att upptäcka förekomsten av degenerativ subkortikal vit substans . Mikroskopi av cerebrospinalvätskan kan också användas för diagnos, där svullna astrocyter med förvrängda och långsträckta mitokondrier kan ses hos patienter.
Urinundersökningar används för att skilja CD-patienter från andra neurodegenerativa sjukdomar med liknande morfologi , såsom Alexanders sjukdomar och Tay-Sachs sjukdomar (som på liknande sätt uppvisar makrocefali ), eftersom patienter med CD unikt visar ökad utsöndring av NAA.
Förebyggande
DNA-analys används vanligtvis för att avgöra om föräldrarna är bärare av den muterade genen. Prenatal diagnostik genom antingen DNA-analys eller bestämning av NAA i fostervatten (som skulle öka vid en påverkad graviditet) kan också användas när DNA-analys inte kan utföras på föräldrar. Det har observerats att det finns en onormalt hög andel av smittbärare i den judiska befolkningen i Ashkenazi. Risken att deras avkomma får svampig degeneration är en av fyra om båda föräldrarna är bärare av den muterade genen.
Behandlingsmetoder
Det finns för närvarande inga specifika behandlingsformer kända för svampig degeneration av CNS. Vissa behandlingsmoduler är under experimentella prövningar och nuvarande patienter stöds av palliativa åtgärder, som alla beskrivs nedan.
Nuvarande palliativa åtgärder
Nuvarande patienter stöds av vårdriktlinjerna för andra pediatriska neurodegenerativa sjukdomar. För patienter med andningsproblem används sugmaskiner för att rensa bort slemhinnor från de övre luftvägarna i lungorna. Syrekoncentratorer administreras också för luftvägsrensning och kontinuerlig tillförsel av luft för att underlätta andningen. När det gäller spädbarn med hypotoni, åtgärdas det genom att tillhandahålla positioneringsutrustning som specialiserade barnvagnar, badstolar och matarstolar.
Möjliga behandlingsmoduler under utveckling
Intraperitoneala injektioner av liponsyra
Liponsyra (som kan passera blod-hjärnbarriären) har nyligen prövats i prekliniska studier , där den har injicerats i tremorråttor intraperitonealt . Tremorråttor anses vara den naturligt förekommande modellen för svampig degenerering av CNS eftersom NAA inducerar oxidativ stress. Positiva resultat har framkommit från dessa studier, vilket tyder på att liponsyra kan vara ett möjligt tillvägagångssätt för symtomatiska behandlingar .
Intraperitoneal litiumadministrering
En möjlig behandling är att använda neuroprotektiva tekniker för att kompensera för den neurologiska skadan i CNS orsakad av ackumulering av NAA. En potentiell behandling som har identifierats är litium , som har observerats inducera neuroprotektiva effekter hos demenspatienter . Administrering av intraperitonealt litium har testats på både tremor och råttor av vildtyp, vilket orsakar en minskning av NAA-nivåer hos båda arterna. I försök på människor visade sig NAA-nivåerna i patientens hjärna och urin sjunka efter ett års behandling. Detta i kombination med ökad vakenhet och visuell spårning. Dock. CD-symtom inklusive axiell hypotoni och spastisk diplegi kvarstod.
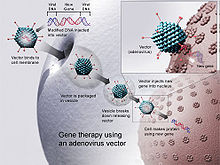
Genterapi
Eftersom CD uppstår från en monogen defekt och är lokaliserad i CNS, är genersättningsterapi en potentiell behandling. Denna terapi innebär att den muterade genen av sjukdomen ersätts med en fullt fungerande gen med hjälp av en vektor, som transporterar terapeutiskt DNA in i celler, vilket gör att cellerna kan producera AspA. Adenoassocierade virus (AAV) används i stor utsträckning som vektorer för genterapi. De är adopterade eftersom de inte replikerar sig själva och är nästan giftfria. Det finns två serotyper som används för behandlingen: AAV2 och AAV9. Skillnaden mellan stereotyperna är att AAV2 begränsas av blod-hjärnbarriären (BBB), medan AAV9 kan passera BBB, vilket möjliggör behandling även i senare stadier av sjukdomen. Men aktuell forskning visar att AAV kan utlösa oönskade immunsvar hos spädbarn och har begränsad geninkapslingskapacitet.
Epidemiologi
Svampig degeneration av CNS är pan-etnisk , på grund av dess förekomst bland ashkenazijudar . Det finns två vanliga mutationer bland dem: missense-mutation (Glu285AIa) och nonsens-mutation (Tyr231X). I missense-mutationen sker en ersättning av glutaminsyra till alanin . När det gäller nonsensmutationen är tyrosinkodonet ersatt av ett termineringskodon . Genetisk screening visar att omkring 1 av 40 friska judar är bärare och förekomsten av denna sjukdom i denna population är så hög som 1 av 6000.
Historia
Det första fallet av svampig degeneration av CNS rapporterades 1928 av Globus och Strauss, som betecknade fallet som Schilders sjukdom, en term för diffus myelinoklastisk skleros . År 1931 rapporterade Canavan om ett fall där megalensfalin av hjärndegeneration skiljer sig från den som orsakas av en tumör . Men hon kunde inte känna igen de svampiga förändringarna som tyder på en unik patologisk orsak som skiljer hennes fall från Schilders sjukdom. Senare 1937 rapporterade Eislebergl sex fall från judiska familjer och upptäckte de familjära egenskaperna hos svampig degeneration, men hon klassificerade dessa fall som Krabbes skleros . Det var inte förrän 1949 när Van Bogaert och Bertrand rapporterade fem fall från judiska familjer, varpå ytterligare patologisk analys bekräftade att svampig degeneration är den nosologiska enheten.