Myelinogenes
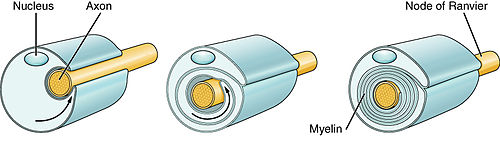
Myelinogenes är bildandet och utvecklingen av myelinskidor i nervsystemet , vanligtvis initierad i sen prenatal neuroutveckling och fortsätter under postnatal utveckling. Myelinogenes fortsätter under hela livslängden för att stödja inlärning och minne via neurala kretsplasticitet samt remyelinisering efter skada. Framgångsrik myelinisering av axoner ökar aktionspotentialens hastighet genom att möjliggöra saltande ledning , vilket är avgörande för snabb signalledning mellan rumsligt åtskilda hjärnregioner, samt ger metaboliskt stöd till neuroner.
Etapper
Myelin bildas av oligodendrocyter i det centrala nervsystemet och Schwann-celler i det perifera nervsystemet . Därför definieras det första stadiet av myelinogenes ofta som differentieringen av oligodendrocyt-progenitorceller eller Schwann-cellsprogenitorer till sina mogna motsvarigheter, följt av myelinbildning runt axoner.
Oligodendrocytlinjen kan ytterligare klassificeras i fyra stadier baserat på deras relation till starten av myelinisering:
- Differentiering: OPC lämnar sitt proliferativa, självförnyande tillstånd och börjar uttrycka gener och proteiner som är associerade med oligodendrocyters ödesengagemang.
- Preoligodendrocyt: Dessa celler uttrycker O4-antigenet och utvecklar flera processer som sträcker sig radiellt utan någon speciell organisation.
- Omogna oligodendrocyter: Ibland hänvisade till som premyeliniserande oligodendrocyter, dessa celler utökar "pionjärprocesser" som kontaktar axoner och förankrar premyeliniserande oligodendrocyter till neuroner så att de är redo att påbörja myelinogenes som svar på axonala signaler. Dessa pionjärprocesser växer longitudinellt längs sina målaxoner.
- Mogna oligodendrocyter: Efter myelinogenes omger mogna oligodendrocyter axoner i organiserade, multilamellära myelinskidor som innehåller myelinbasprotein (MBP) och myelinproteolipidprotein (PLP).
Myelinogenes omfattar således övergångsprocessen mellan fas 3 och 4. Vid initiering av myelinogenes bildar varje pionjärprocess lamellära förlängningar som sträcker sig och utvecklas runt målaxonet. Detta bildar det första varvet av myelinskidan. Skidan fortsätter att expandera längs målaxonets längd medan nytt membran syntetiseras vid framkanten av den inre tungan av det utvecklande myelinskidan, som börjar anta en spiralformad tvärsnittsstruktur.
För att driva en korrekt sammansättning av membranskikten sätts PLP in i membranet för att stabilisera interaktioner mellan utvändiga blad i myelinmembranen; MBP översätts lokalt och sätts in i de cytoplasmatiska membranbladen för att stärka myelinmembranen internt. I samverkan med bildandet av axonala noder av Ranvier bildar myelinskidans kanter paranodala slingor.
Mekanism


Den grundläggande helix-loop-helix- transkriptionsfaktorn OLIG1 spelar en integrerad roll i processen för oligodendrocyt-myelinogenes genom att reglera uttrycket av myelinrelaterade gener. OLIG1 är nödvändigt för att initiera myelinisering av oligodendrocyter i hjärnan, men är något dispenserbar i ryggmärgen.
Axon-härledda signaler reglerar uppkomsten av myelinogenes. Forskare studerade regenererande PNS-axoner i 28 veckor för att undersöka om perifera axoner stimulerar oligodendrocyter att börja myelinisering. Experimentell induktion av myelinisering genom att regenerera perifera axoner visade att Schwann-celler och oligodendrocyter har en gemensam mekanism för att stimulera myelinisering. En liknande studie som arbetar för att ge bevis för neuronal reglering av myelinogenes antydde att myelinbildning berodde på Schwann-celler som kontrollerades av en odefinierad egenskap hos ett associerat axon.
Ny forskning på råttor har föreslagit att apotransferrin och sköldkörtelhormon verkar både separat och synergistiskt för att främja myelinogenes, eftersom apotransferrin främjar uttrycket av sköldkörtelhormonreceptorn alfa .
Perifer myelinogenes
Perifer myelinogenes styrs av syntesen av proteinerna P1, P2 och P0. Genom att använda SDS-PAGE avslöjade forskare distinkta band med bandstorlekar på 27 000 Dalton (P1), 19 000 Dalton (P2) och 14 000 Dalton (P0). Studier har också visat att P1 och P2 är aktiva före P0 eftersom detta protein kommer från det perifera nervsystemet. Under regenereringsprocessen Schwann-celler proteiner associerade med myelinspecifika proteiner när axonal närvaro återupprättas. Syntes av myelinspecifika proteiner sker endast i Schwann-celler associerade med axoner. Dessutom kan membran-membran-interaktioner mellan axoner krävas för att främja syntesen av P1, P2 och P0.
Myelinogenes i synnerven
Processen och den mekanistiska funktionen av myelinogenes har traditionellt studerats med hjälp av ultrastruktur och biokemiska tekniker i synnerver från råtta . Implementeringen av denna studiemetod har länge möjliggjort experimentell observation av myelinogenes i en modellorganismnerv som helt består av omyeliniserade axoner. Dessutom bidrog användningen av råttans synnerv till att ge insikt för tidiga myelinogenesforskare om felaktiga och atypiska förlopp av myelinogenes.
En tidig studie visade att hos de utvecklande synnerverna hos råtta sker bildning av oligodendrocyter och efterföljande myelinisering postnatalt . I synnerven delades oligodendrocytcellerna för sista gången efter fem dagar, med början av myelinbildningen inträffade på eller runt dag 6 eller 7. Den exakta processen genom vilken oligodendrocyterna stimulerades att producera myelin var dock ännu inte helt förstått, men tidig myelinisering i synnerven har kopplats till en ökning av produktionen av olika lipider – kolesterol, cerebrosid och sulfatid.
När forskare började göra postnatal forskning fann de att myelinogenesen i råttans synnerv initialt börjar med axoner med de största diametrarna innan de fortsätter till de återstående mindre axonerna. Under den andra veckan efter födseln avtog oligodendrocytbildningen – vid denna tidpunkt har 15 % av axonerna myeliniserats – men myelinogenesen fortsatte att snabbt öka. Under den fjärde veckan efter födseln hade nästan 85 % av axonerna i råttoptiken myeliniserats. Under den femte veckan och framåt mot vecka sexton, bromsades myelineringen in och de återstående omyeliniserade axonerna var inkapslade i myelin. Genom råttans synnerv gav tidig forskning betydande bidrag till kunskap inom området myelinogenes.
Sulfatiders roll
Studier på den utvecklande synnerven avslöjade att galaktocerebrosid (som bildar sulfatid) uppträdde den 9:e postnatala dagen och nådde en topp den 15:e postnatala dagen. Detta uttryck liknade en period där synnerven visade en maximal myeliniseringsperiod av axonet. Eftersom aktiviteten av axonmyelinisering minskade, och man kunde dra slutsatsen att aktiviteten av enzymet är parallell med inkorporeringen av sulfat ([35S]) i sulfatid in vivo.
Studierna på en synnerv från råtta visade att 15 dagar efter förlossningen observeras en ökning av myeliniseringen. Före denna tidsperiod är de flesta av axonerna, ungefär 70 %, inte myeliniserade. Vid denna tidpunkt inkorporerades [35S]-sulfat i sulfatid och aktiviteten av cerebrosid , sulfotransferas nådde en topp i enzymaktivitet. Denna tidsram visade också en period av maximal myelinisering baserat på biokemiska data.
I CNS verkar sulfatid , sulfaterade glykoproteiner och sulfaterade mukopolysackarider vara associerade med neuroner snarare än myelin. När vi graferar mängden sulfatid gjord av [35S] och aktiviteten av sulfotransferas kommer vi till distinkta toppar. Topparna inträffar den 15:e dagen efter förlossningen. Dessa toppar motsvarade den maximala myeliniseringsperioden för synnerven som har setts under hela experimentet.
Sammanfattningsvis var den tidiga fasen av myelinisering korrelerad med den ökade syntesen av lipider, kolesterol, cerebrosid och sulfatid. Det är troligt att dessa föreningar syntetiseras och förpackas i Golgi-apparaten för oligodendroglia. Även om transporten av dessa lipider är okänd, verkar det som om myeliniseringen är försenad utan deras syntes.
Klinisk signifikans
Eftersom myelin bildar ett elektriskt isolerande lager som omger axonet i vissa nervceller , kan alla demyeliniserande sjukdomar påverka nervsystemets funktion . En sådan sjukdom är multipel skleros (MS), där demyelinisering sker i det centrala nervsystemet (CNS). Även om forskning bedrivs för att skydda oligodendrocyter och främja remyelinisering vid MS, behandlar nuvarande terapier främst immunsystemets roll vid demyelinisering.
Forskningshistoria

En annan forskare, Paul Flechsig, tillbringade större delen av sin karriär med att studera och publicera detaljerna om processen i hjärnbarken hos människor. Detta sker oftast mellan två månader före och efter födseln . Han identifierade 45 separata kortikala områden och kartlade faktiskt hjärnbarken genom myeliniseringsmönstret. Den första kortikala regionen som myelineras är i motorbarken (en del av Brodmanns område 4), den andra är luktbarken och den tredje är en del av den somatosensoriska cortexen (BA 3,1,2).
De sista områdena att myelinisera är den främre cingulate cortex (F#43), den inferior temporala cortex (F#44) och den dorsolaterala prefrontala cortexen (F#45).
I hjärnvikningarna, liksom i alla andra delar av centrala nervsystemet, utvecklas nervfibrerna inte överallt samtidigt, utan steg för steg i bestämd följd, varvid denna ordning av händelserna särskilt upprätthålls med hänsyn till märgens utseende. ämne. I storhjärnans veck har investeringen med märgsubstans (myelinisering) redan börjat på vissa ställen tre månader innan fostrets mognad, medan på andra ställen många fibrer saknar märgsubstans även tre månader efter födseln. Ordningen för succession i vecken styrs av en lag som är identisk med den lag som jag har visat gäller för ryggmärgen, förlängd märgen och mesocephalon, och som kan uttryckas något på detta sätt - att man, ungefär, lika viktiga nervfibrer utvecklas samtidigt, men de av olika betydelse utvecklas efter varandra i en följd som definieras av en imperativ lag (myelogenesens grundlag). Bildandet av märgsubstans är nästan fullbordat i vissa varv vid en tidpunkt då den hos vissa inte ens har börjat och i andra endast gjort små framsteg.

