Organoselenium kemi
Organoseleniumföreningar (eller selenoorganiska) är kemiska föreningar som innehåller kol -till- selen kemiska bindningar . Organoseleniumkemi är motsvarande vetenskap som utforskar deras egenskaper och reaktivitet. Selen tillhör med syre och svavel gruppen 16 grundämnen eller kalkogener, och likheter i kemi är att vänta. Organiska lenföreningar finns i spårhalter i omgivande vatten, jordar och sediment.
Selen kan existera med oxidationstillstånd −2, +2, +4, +6. Se(II) är den dominerande formen i organoseleniumkemi. Nedåt i grupp 16-kolumnen bindningsstyrkan allt svagare (234 kJ / mol för C−Se-bindningen och 272 kJ/mol för C−S-bindningen) och bindningslängderna längre (C−Se 198 pm, C−S 181 pm och C−O 141 pm). Selenföreningar är mer nukleofila än motsvarande svavelföreningar och även surare. p Ka - värdena för XH 2 är 16 för syre, 7 för svavel och 3,8 för selen. I motsats till sulfoxider är motsvarande selenoxider instabila i närvaro av β-protoner och denna egenskap används i många organiska reaktioner av selen, särskilt i selenoxidoxidationer och i selenoxideliminering.
Den första organoseleniumföreningen som isolerades var dietylselenid 1836.
Strukturell klassificering av organoseleniumföreningar
- Selenoler (RSeH) är selenekvivalenter av alkoholer och tioler . Dessa föreningar är relativt instabila och har i allmänhet en obehaglig lukt. Benseneselenol (även kallad selenafenol eller PhSeH) är surare (pK a 5,9) än tiofenol (pK a 6,5) och oxiderar också lättare till diseleniden . Selenafenol framställs genom reduktion av difenyldiselenid.
- Diselenider (R−Se−Se−R) är selenekvivalenter av peroxider och disulfider . De är användbara lagringsstabila prekursorer till mer reaktiva organoseleniumreagenser såsom selenoler och selanylhalider. Mest känd inom organisk kemi är difenyldiselenid , framställd av fenylmagnesiumbromid och selen följt av oxidation av produkten PhSeMgBr.
- Selanylhalogenider (R−Se−Cl, R−Se−Br) framställs genom halogenering av diselenider. Bromering av difenyldiselenid ger fenylselanylbromid (PhSeBr). Dessa föreningar är källor till "PhSe + ".
- Selenider (R−Se−R), även kallade selenoetrar , är selenekvivalenter av etrar och sulfider . Ett exempel är dimetylselenid ((CH3 ) 2Se ) . Dessa är de vanligaste organoseleniumföreningarna. Symmetriska selenider framställs vanligtvis genom alkylering av alkalimetallselenidsalter, t.ex. natriumselenid . Osymmetriska selenider framställs genom alkylering av selenoater. Dessa föreningar reagerar typiskt som nukleofiler , t.ex. med alkylhalider (R'−X) för att ge selenoniumsalter R'RRSe + X− . Tvåvärt selen kan också interagera med mjuka heteroatomer för att bilda hypervalenta selencentra. De reagerar också under vissa omständigheter som elektrofiler, t.ex. med organolitiumreagens (R'Li) på det ata komplexet R'RRSe − Li + .
- Selenoxider (R−Se(O)−R) är selenekvivalenter av sulfoxider . De kan vidare oxideras till selenonerna R−Se(O) 2R , selenanalogerna av sulfoner .
- Selensyra (RSe−OH) är mellanprodukter i oxidationen av selenoler. De förekommer i vissa selenoenzymer, såsom glutationperoxidas .
- Seleninsyror (RSe(O)OH) är analoger till sulfinsyror .
- Selenonsyror (RSe(O) 2OH ) är analoger till sulfonsyror .
- Peroxiseleninsyror (RSe(O)OOH) katalyserar epoxidationsreaktioner och Baeyer–Villiger-oxidationer .
- Selenuraner är hypervalenta organoseleniumföreningar, formellt härledda från tetrahaliderna såsom SeCl 4 . Exempel är av typen ArSeCl3 . Kloriderna erhålls genom klorering av selenenylkloriden .
- Seleniraner är treledade ringar (moder: C 2 H 4 Se) besläktade med tiiraner , men till skillnad från tiiraner är seleniraner kinetiskt instabila och extruderar selen direkt (utan oxidation) för att bilda alkener . Denna egenskap har använts i syntetisk organisk kemi.
- Seloner (R2C = Se) är selenanaloger av ketoner. De är sällsynta på grund av deras tendens att oligomerisera . Diselenobensokinon är stabilt som ett metallkomplex. Selenourea är ett exempel på en stabil förening som innehåller en C=Se-bindning.
- Tioselenider (R−Se−S−R), föreningar med selen(II)–svavel(II)bindningar, analogt med disulfider .
Organiska lenföreningar i naturen
Selen, i form av organoseleniumföreningar, är ett viktigt mikronäringsämne vars frånvaro i kosten orsakar hjärtmuskel- och skelettdysfunktion. Organoseleniumföreningar krävs för cellulärt försvar mot oxidativ skada och för att immunsystemet ska fungera korrekt. De kan också spela en roll för att förebygga för tidigt åldrande och cancer. Källan till Se som används i biosyntes är selenofosfat .
Glutationoxidas är ett enzym med en selenol på dess aktiva plats. Organiska lenföreningar har hittats i högre växter. Till exempel, vid analys av vitlök med tekniken med högpresterande vätskekromatografi kombinerat med induktivt kopplad plasmamasspektrometri (HPLC-ICP-MS), fann man att γ-glutamyl- Se -metylselenocystein var den huvudsakliga Se-innehållande komponenten, tillsammans med mindre mängder Se -metylselenocystein . Spårmängder av dimetylselenid och allylmetylselenid finns i människors andetag efter att ha konsumerat rå vitlök.
Selenocystein och selenometionin
Selenocystein , som kallas den tjugoförsta aminosyran, är avgörande för ribosomriktad proteinsyntes i vissa organismer. Mer än 25 seleninnehållande proteiner (selenoproteiner) är nu kända. De flesta selenberoende enzymer innehåller selenocystein , som är besläktat med cysteinanalog men med selen som ersätter svavel. Denna aminosyra kodas på ett speciellt sätt av DNA . Selenosulfider föreslås också som biokemiska mellanprodukter.
Selenometionin är en selenidinnehållande aminosyra som också förekommer naturligt, men som genereras genom post-transkriptionell modifiering.
Organoseleniumkemi i organisk syntes
Organiska lenföreningar är en specialiserad men användbar samling av reagens användbara i organisk syntes, även om de i allmänhet är uteslutna från processer som är användbara för läkemedel på grund av regulatoriska frågor. Deras användbarhet beror på vissa attribut, inklusive (i) svagheten hos C−Se-bindningen och (ii) den lätta oxidationen av tvåvärda selenföreningar.
Vinyl selenider
Vinylselenider är organoseleniumföreningar som spelar en roll i organisk syntes, särskilt i utvecklingen av bekväma stereoselektiva vägar till funktionaliserade alkener . Även om olika metoder nämns för framställning av vinyliska selenider, har en mer användbar procedur fokuserat på nukleofila eller elektrofila organoseleniumtillsats till terminala eller interna alkyner . Till exempel ger den nukleofila tillsatsen av selenofenol till alkyner, företrädesvis, Z-vinyliska selenider efter längre reaktionstider vid rumstemperatur. Reaktionen är snabbare vid hög temperatur; emellertid erhölls blandningen av Z- och E-vinylselenider i ett nästan 1:1-förhållande. Å andra sidan beror addukterna på arten av substituenterna vid trippelbindningen . Omvänt kan vinyliska selenider framställas genom palladium -katalyserad hydroselenering av alkyner för att ge Markovnikov-addukten i goda utbyten. Det finns vissa begränsningar förknippade med metoderna för att framställa vinyliska selenider som illustreras ovan; de beskrivna förfarandena använder diorganoyldiselenider eller selenofenol som utgångsmaterial, vilka är flyktiga och instabila och har en obehaglig lukt. Framställningen av dessa föreningar är också komplex.
Selenoxidoxidationer
Selendioxid är användbart vid organisk oxidation . Specifikt kommer SeO2 att omvandla en allylisk metylengrupp till motsvarande alkohol . Ett antal andra reagens åstadkommer denna reaktion.
När det gäller reaktionsmekanismen reagerar SeO 2 och det allyliska substratet via pericyklisk process som börjar med en en-reaktion som aktiverar C−H-bindningen. Det andra steget är en [2,3] sigmatropisk reaktion . Oxidationer som involverar selendioxid utförs ofta med katalytiska mängder av selenföreningen och i närvaro av en offerkatalysator eller samoxidant såsom väteperoxid .
SeO 2 -baserade oxidationer ger ibland karbonylföreningar såsom ketoner , β- pinen och cyklohexanonoxidation till 1,2-cyklohexandion. Oxidation av ketoner med a-metylengrupper ger diketoner. Denna typ av oxidation med selenoxid kallas Riley-oxidation .
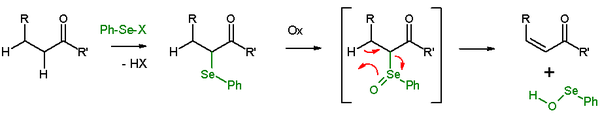
Eliminering av selenoxid
I närvaro av ett β-väte kommer en selenid att ge en elimineringsreaktion efter oxidation, för att lämna kvar en alken och en SeO - selenoperoxol . SeO - selenoperoxolen är mycket reaktiv och är inte isolerad som sådan. I elimineringsreaktionen är alla fem deltagande reaktionscentra koplanära och därför är reaktionsstereokemin syn . Oxidationsmedel som används är väteperoxid , ozon eller MCPBA . Denna reaktionstyp används ofta med ketoner som leder till enoner . Ett exempel är eliminering av acetylcyklohexanon med bensenselenylklorid och natriumhydrid .
Grieco -elimineringen är en liknande selenoxideliminering med o-nitrofenylselenocyanat och tributylfosfin för att orsaka eliminering av H 2 O -elementen.