Kol-syrebindning
En kol-syrebindning är en polär kovalent bindning mellan atomer av kol och syre . Kol-syrebindningar finns i många oorganiska föreningar som koloxider och oxohalider , karbonater och metallkarbonyler , och i organiska föreningar som alkoholer , etrar , karbonylföreningar och oxalater . Syre har 6 egna valenselektroner och tenderar att fylla sitt yttre skal med 8 elektroner genom att dela elektroner med andra atomer för att bilda kovalenta bindningar , acceptera elektroner för att bilda en anjon , eller en kombination av de två. I neutrala föreningar kan en syreatom bilda upp till två enkelbindningar eller en dubbelbindning med kol, medan en kolatom kan bilda upp till fyra enkelbindningar eller två dubbelbindningar med syre.
Limningsmotiv
Bindning vid syre
I etrar bildar syre två kovalenta enkelbindningar med två kolatomer, C–O–C, medan i alkoholer bildar syre en enkelbindning med kol och en med väte, C–O–H. I karbonylföreningar bildar syre en kovalent dubbelbindning med kol, C=O, känd som en karbonylgrupp . I etrar, alkoholer och karbonylföreningar bildar de fyra icke-bindande elektronerna i syrets yttre skal två ensamma par . I alkoxider bildar syre en enkelbindning med kol och tar emot en elektron från en metall för att bilda en alkoxidanjon, R–O − , med tre ensamma par. I oxoniumjoner används ett av syrets två ensamma par för att bilda en tredje kovalent bindning som genererar en katjon , >O + – eller =O + – eller ≡O + , med ett ensamt par kvar.
Bindning vid kol
En kolatom bildar en enkelbindning till syre i alkoholer, etrar och peroxider, två i acetaler , tre i ortoestrar och fyra i ortokarbonater . Kol bildar en dubbelbindning till syre i aldehyder , ketoner och acylhalider . I karboxylsyror , estrar och anhydrider bildar varje karbonylkolatom en dubbelbindning och en enkelbindning till syre. I karbonatestrar och kolsyra bildar karbonylkolet en dubbelbindning och två enkelbindningar till syre. I koldioxid bildar kol två dubbelbindningar till syre.
Elektronegativiteter och bindningslängder
C-O-bindningen är starkt polariserad mot syre ( elektronegativitet av C vs O, 2,55 vs 3,44). Bindningslängder för paraffiniska C–O-bindningar ligger i intervallet 143 pm – mindre än för C–N- eller C–C-bindningar. Förkortade enkelbindningar finns med karboxylsyror (136 pm) på grund av partiell dubbelbindningskaraktär och långsträckta bindningar finns i epoxider (147 pm). C–O -bindningsstyrkan är också större än C–N eller C–C. Till exempel är bindningsstyrkorna 91 kilokalorier (380 kJ)/mol (vid 298 K) i metanol , 87 kilokalorier (360 kJ)/mol i metylamin och 88 kilokalorier (370 kJ)/mol i etan .
Kol och syre bildar terminala dubbelbindningar i funktionella grupper kollektivt kända som karbonylföreningar som tillhör sådana föreningar som ketoner , estrar , karboxylsyror och många fler. Inre C=O-bindningar finns i positivt laddade oxoniumjoner . I furaner bidrar syreatomen till pi-elektrondelokalisering via sin fyllda p-orbital och furaner är därför aromatiska . Bindningslängder för C=O-bindningar är cirka 123 pm i karbonylföreningar. C=O-bindningslängden i koldioxid är 116 pm. C=O-bindningarna i acylhalider har partiell trippelbindningskaraktär och är följaktligen mycket korta: 117 pm. Föreningar med formella C ≡ O-trippelbindningar existerar inte förutom kolmonoxid , som har en mycket kort, stark bindning (112,8 pm), och acyliumjoner , R–C≡O + (typiskt 110-112 pm). Sådana trippelbindningar har en mycket hög bindningsenergi, till och med högre än N–N trippelbindningar. Syre kan också vara trevärt, till exempel i trietyloxoniumtetrafluorborat .
Kemi
Kol-syrebindningsbildande reaktioner är Williamson-etersyntesen , nukleofila acylsubstitutioner och elektrofil addition till alkener. Paternò –Büchi-reaktionen involverar karbonylföreningar.
Syrefunktionella grupper
Kol-syrebindningar finns i dessa funktionella grupper :
| Kemisk klass | Obligationsorder | Formel | Strukturformel | Exempel |
|---|---|---|---|---|
| Alkoholer | 1 | ROH |
|
Etanol |
| Etrar | 1 | ROR′ |
|
Dietyleter |
| Peroxider | 1 | ROOR′ |
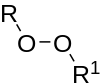
|
Di-tert-butylperoxid |
| Cyanatestrar | 1 | ROCN |

|
Bisfenol A cyanatester |
| Aldehyder | 2 | RCHO |

|
 Akrolein |
| Ketoner | 2 | RCOR′ |

|
Aceton |
| Karboxylsyror | 1 & 2 |
RCOOH (eller RCO 2H ) |
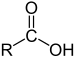
|
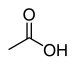 Ättiksyra |
| Estrar | 1 & 2 |
RCOOR (eller RCO 2 R) |

|
Etylakrylat |
| Karbonatestrar | 1 & 2 |
ROCOOR (eller ROCO 2 R) |

|
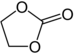 Etenkarbonat |
| Isocyanater | 2 | RNCO |

|
 Fenylisocyanat |
| Nitritestrar | 1 | RONO |
|
Amylnitrit |
| Nitratestrar | 1 | RONO 2 |

|
Isopropylnitrat |
| Karbamatestrar | 1 & 2 | ROCONR 2 |

|
 Carbaryl |
| Furans | 1.5 | R4C4O _ _ _ _ |

|
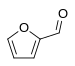 Furfural |
| Pyryliumsalter | 1.5 | R5C5O + X- _ _ _ _ _ |

|
 Antocyaniner |
Se även
- Kolföreningar#Kol-syreföreningar
- Kol-vätebindning
- Kol-kolbindning
- Kol-kvävebindning
- Kol-fluorbindning
- Silikon-syrebindning