Difenyldiselenid

|
|

|
|
| Namn | |
|---|---|
|
IUPAC namn
1,1'-Diselandiyldibensen
|
|
| Andra namn Fenyldiselenid
|
|
| Identifierare | |
|
3D-modell ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard | 100.015.256 |
| EG-nummer |
|
|
PubChem CID
|
|
| RTECS-nummer |
|
| UNII | |
|
CompTox Dashboard ( EPA )
|
|
|
|
|
|
| Egenskaper | |
| C12H10Se 2 _ _ _ _ | |
| Molar massa | 312,154 g·mol -1 |
| Utseende | Gula kristaller |
| Densitet | 1,84 g/cm 3 |
| Smältpunkt | 59 till 61 °C (138 till 142 °F; 332 till 334 K) |
| Olöslig | |
| Löslighet i andra lösningsmedel | Diklormetan , THF , varm hexan |
| Strukturera | |
|
90° vid Se [ citat behövs ] C 2 symmetri [ citat behövs ] |
|
| 0 D | |
| Faror | |
| GHS- märkning : | |
  
|
|
| Fara | |
| H301 , H331 , H373 , H410 | |
| P260 , P261 , P264 , P270 , P271 , P273 , P301+P310 , P304+P340 , P311 , P314 , P321 , P330 , P391 , P403+P405, P403 + P405 , P503 | |
| Besläktade föreningar | |
|
Besläktade föreningar
|
Ph2S2 _ _ _ , C6H5SeH _ _ _ _ |
|
Om inte annat anges ges data för material i standardtillstånd (vid 25 °C [77 °F], 100 kPa).
|
|
Difenyldiselenid är den kemiska föreningen med formeln (C 6 H 5 ) 2 Se 2 , förkortad Ph 2 Se 2 . Detta orangefärgade fasta ämne är det oxiderade derivatet av bensenselenol . Det används som en källa till PhSe-enheten i organisk syntes .
Beredning och egenskaper
Ph 2 Se 2 framställs genom oxidation av bensenselenoat, den konjugerade basen av bensenselenol som genereras via Grignard-reagenset :
Molekylen har idealiserad C 2 -symmetri, som väteperoxid och relaterade molekyler. Se-Se-bindningslängden på 2,29 Å, C-Se-Se-C-diedrisk vinkel är 82° och C-Se-Se-vinklarna är nära 110°.
Antioxidantverkan
"Kosttillskott med Ph 2 Se 2 förhindrade CH 3 HgCl-inducerad rörelsestörning. Denna effekt verkade förmedlas av antioxidantverkan. Ph 2 Se 2 kan vara ett hållbart tillvägagångssätt för att förebygga eller minska CH 3 HgCl-medierade neurotoxiska effekter."
Reaktioner
En reaktion som är karakteristisk för Ph 2 Se 2 är dess reduktion:
- Ph 2 Se 2 + 2 Na → 2 PhSeNa
PhSeNa är en användbar nukleofil som används för att introducera fenylselenylgruppen genom nukleofil substitution av alkylhalider , alkylsulfonater ( mesylater eller tosylater ) och epoxider . Exemplet nedan togs från en syntes av morfin.
En annan karakteristisk reaktion är klorering :
- Ph2Se2 + Cl2 → 2 PhSeCl _
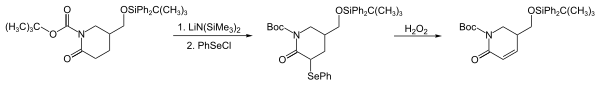
PhSeCl är en kraftfull elektrofil som används för att introducera PhSe-grupper genom reaktion med en mängd olika nukleofiler, inklusive enolater , enolsilyletrar , Grignard-reagenser , organolitiumreagenser , alkener och aminer . I sekvensen nedan (tidiga steg i syntesen av Strychnofoline) introduceras en PhSe-grupp genom reaktion av ett laktamanolat med PhSeCl. Denna sekvens är en kraftfull metod för omvandling av karbonylföreningar till deras α,β-omättade analoger.
Difenyldiselenid i sig är också en källa till en svagt elektrofil PhSe-grupp i reaktioner med relativt kraftfulla nukleofiler som Grignard-reagens, litiumreagens och esterenolater (men inte ketonenolater eller svagare nukleofiler). PhSeCl är både mer reaktivt och mer effektivt, eftersom med Ph 2 Se 2 går hälften av selenet till spillo.
- Ph 2 Se 2 + Nu − → PhSeNu + PhSe −
N -Fenylselenoftalimid (N-PSP) kan användas om PhSeCl är för stark och difenyldiselenid är för svag eller slösaktig.