Plasmodium knowlesi
|
|
| Plasmodium knowlesi | |
|---|---|
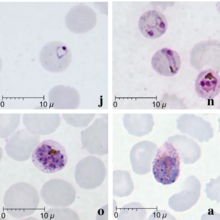
| Giemsa-färgade utstryk av Plasmodium knowlesi som infekterar mänskliga röda blodkroppar | |
| Vetenskaplig klassificering | |
| Rike: | Chromista |
| Underriket: | Harosa |
| Infrakingdom: | Halvaria |
| Superfylum: | Alveolata |
| Provins: | Apicomplexa |
| Klass: | Aconoidasida |
| Beställa: | Haemospororida |
| Familj: | Plasmodiidae |
| Släkte: | Plasmodium |
| Arter: |
P. knowlesi
|
| Binomialt namn | |
|
Plasmodium knowlesi Sinton och Mulligan 1932
|
|
Plasmodium knowlesi är en parasit som orsakar malaria hos människor och andra primater. Det finns i hela Sydostasien och är den vanligaste orsaken till mänsklig malaria i Malaysia . Liksom andra Plasmodium- arter har P. knowlesi en livscykel som kräver infektion av både en mygga och en varmblodig värd. Medan de naturliga varmblodiga värdarna av P. knowlesi sannolikt är olika apor från den gamla världen , kan människor infekteras av P. knowlesi om de matas av infekterade myggor. P. knowlesi är en eukaryot i phylum Apicomplexa , släktet Plasmodium och undersläktet Plasmodium . Den är närmast besläktad med den mänskliga parasiten Plasmodium vivax samt andra Plasmodium- arter som infekterar icke-mänskliga primater.
Människor infekterade med P. knowlesi kan utveckla okomplicerad eller svår malaria liknande den som orsakas av Plasmodium falciparum . Diagnos av P. knowlesi -infektion är utmanande eftersom P. knowlesi mycket liknar andra arter som infekterar människor. Behandlingen liknar andra typer av malaria, med klorokin eller artemisinin kombinationsterapi rekommenderas vanligtvis. P. knowlesi malaria är en framväxande sjukdom som tidigare ansetts vara sällsynt hos människor, men som alltmer erkändes som en stor hälsobörda i Sydostasien.
P. knowlesi beskrevs först som en distinkt art och som en potentiell orsak till mänsklig malaria 1932. Den användes kort i början av 1900-talet för att orsaka feber som en behandling för neurosyfilis . I mitten av 1900-talet P. knowlesi populärt som ett verktyg för att studera Plasmodium- biologi och användes för grundforskning, vaccinforskning och läkemedelsutveckling. P. knowlesi används fortfarande som en laboratoriemodell för malaria, eftersom den lätt infekterar modellprimaten rhesus macaque och kan odlas i cellkultur i humant eller makakblod.
Livscykel
Liksom andra Plasmodium -parasiter har P. knowlesi en livscykel som kräver att den förs fram och tillbaka mellan däggdjursvärdar och insektsvärdar. Primater infekteras genom bett av en infekterad Anopheles- mygga som bär ett parasitstadium som kallas sporozoiten i sina spottkörtlar. Sporozoiter följer blodomloppet till primatlevern där de utvecklas och replikerar under fem till sex dagar innan de spricker, och frigör tusentals dotterceller som kallas merozoiter i blodet (till skillnad från den relaterade P. vivax , gör P. knowlesi inte latenta hypnozoiter i lever). Merozoiterna i blodet fäster vid och invaderar primatens röda blodkroppar . Inuti de röda blodkropparna fortskrider parasiten genom flera morfologiskt urskiljbara stadier, kallade ringstadiet, trofozoiten och schizonten. De schizont-infekterade röda blodkropparna brister så småningom och släpper ut upp till 16 nya merozoiter i blodomloppet som infekterar nya röda blodkroppar och fortsätter cykeln. P. knowlesi slutför denna röda blodkroppscykel var 24:e timme, vilket gör den unikt snabb bland primat-infekterande Plasmodium -arter (som vanligtvis tar 48 eller 72 timmar). Ibland går parasiter som invaderar röda blodkroppar istället in i en sexuell cykel och utvecklas under cirka 48 timmar till distinkta sexuella former som kallas mikrogametocyter eller makrogametocyter. Dessa gametocyter finns kvar i blodet för att intas av myggor.
En mygga får i sig gametocyter när den tar en blodmåltid från en infekterad primatvärd. Väl inne i myggtarmen utvecklas gametocyterna till gameter och smälter sedan ihop till en diploid zygot. Zygoten mognar till en ookinete , som vandrar genom väggen i myggtarmen och utvecklas till en oocysta . Oocystan frigör sedan tusentals sporozoiter, som vandrar genom myggan till spottkörtlarna. Hela denna process i myggan tar 12 till 15 dagar.
Cellbiologi
P. knowlesi liknar till stor del andra Plasmodium -arter i sin cellbiologi. Dess genom består av 23,5 megabaser av DNA separerade i 14 kromosomer . Den innehåller cirka 5200 proteinkodande gener, varav 80% har ortologer närvarande i P. falciparum och P. vivax . Genomet innehåller två stora genfamiljer som är unika för P. knowlesi : familjen SICAvar (schizont-infekterad cellagglutinationsvariant), som är involverad i att visa olika antigener på parasitytan för att undvika immunsystemet, och Kir (knowlesi interspersed) repeat) familj, involverad i att fästa parasiterade röda blodkroppar till blodkärlsväggar.
Som en apicomplexan har P. knowlesi flera distinkta strukturer vid sin apikala ände som är specialiserade för att invadera värdceller. Dessa inkluderar de stora bulbous rhoptries , mindre mikronemes och dispergerade täta granuler , som var och en utsöndrar effektorer för att komma in i och modifiera värdcellen. Liksom andra apicomplexans P. knowlesi också två organeller av endosymbiotiskt ursprung : en enda stor mitokondrie och apikoplasten , som båda är involverade i parasitens metabolism .
Evolution och taxonomi
Trots sin morfologiska likhet med P. malariae är P. knowlesi närmast besläktad med P. vivax såväl som andra Plasmodium- arter som infekterar icke-mänskliga primater. Den sista gemensamma förfadern till alla moderna P. knowlesi -stammar levde för uppskattningsvis 98 000 till 478 000 år sedan. Bland mänskliga parasiter P. knowlesi närmast besläktad med P. vivax , från vilken den avvek mellan 18 miljoner och 34 miljoner år sedan. Ett fylogenetiskt träd som jämför Plasmodium -arterna som infekterar människor visas nedan:
| Subgenus Plasmodium |
|
||||||||||||||||||
Populationen av P. knowlesi -parasiter är mer genetiskt mångfaldig än den hos P. falciparum eller P. vivax . Inom P. knowlesi finns tre genetiskt distinkta subpopulationer. Två finns i samma områden på malaysiska Borneo och kan infektera olika myggor. Den tredje har endast hittats i laboratorieisolat som kommer från andra delar av Sydostasien. Populationer av P. knowlesi isolerade från makaker är genetiskt omöjliga att skilja från de som isolerats från mänskliga infektioner, vilket tyder på att samma parasitpopulationer kan infektera människor och makaker omväxlande.
Tre underarter av P. knowlesi har beskrivits baserat på skillnader i deras utseende i färgade blodfilmer: P. knowlesi edesoni , P. knowlesi sintoni och P. knowlesi arimai , som isolerades från Malaysia, Java respektive Taiwan. Förhållandet mellan dessa beskrivna underarter och de populationer som beskrivs i den moderna litteraturen är inte klart.
Distribution
Plasmodium knowlesi finns i hela Sydostasien , där den främst infekterar den långsvansade makaken , grisstjärtsmakaken och Sumatran surili samt myggvektorerna Anopheles hackeri i halvön Malaysia och Anopheles latens i Sarawak . Långsvansade makaker i det vilda kan infekteras med P. knowlesi utan någon uppenbar sjukdom, även när de samtidigt är infekterade med olika andra Plasmodium -arter. P. knowlesi finns sällan utanför Sydostasien, troligen eftersom myggorna den infekterar är begränsade till den regionen.
Roll i mänskliga sjukdomar
P. knowlesi kan orsaka både okomplicerad och svår malaria hos människor. De som är smittade upplever nästan alltid feber och frossa . Personer med okomplicerad P. knowlesi -malaria upplever ofta också huvudvärk, ledvärk, sjukdomskänsla och aptitlöshet. Mer sällan rapporterar människor hosta, buksmärtor, diarré, illamående och kräkningar. Laboratorietester av infekterade personer visar nästan alltid ett lågt antal blodplättar , även om detta sällan leder till blödningsproblem. Till skillnad från andra mänskliga malaria, tenderar P. knowlesi -malaria att ha feber som ökar var 24:e timme, och kallas därför ofta daglig eller "quotidian" malaria. Okomplicerad P. knowlesi malaria kan behandlas med antimalaria läkemedel .
Minst 10 % av personer som är infekterade med P. knowlesi utvecklar svår malaria. Svår P. knowlesi -malaria liknar svår malaria orsakad av P. falciparum . De med svår sjukdom kan uppleva andnöd, buksmärtor och kräkningar. När sjukdomen fortskrider replikerar parasiter till mycket höga nivåer i blodet, vilket sannolikt orsakar akut njurskada, gulsot , chock och andnöd. Metabolisk acidos är ovanligt, men kan förekomma i särskilt allvarliga fall. Till skillnad från P. falciparum- malaria orsakar svår P. knowlesi- malaria sällan koma eller svår anemi . Cirka 1-2% av fallen är dödliga.
Diagnos
Malaria diagnostiseras traditionellt genom att undersöka Giemsa-färgade blodfilmer under ett mikroskop; dock är det svårt att skilja P. knowlesi från andra Plasmodium -arter på detta sätt på grund av deras liknande utseende. P. knowlesi ringstadieparasiter färgade med Giemsa liknar P. falciparum ringstadier, uppträder som en cirkel med en eller två mörka prickar av kromatin . Äldre trofozoiter verkar mer spridda och bildar en rektangulär form spridd över värdcellen som kallas en "bandform" som liknar det liknande stadiet i P. malariae . Under detta skede uppträder ibland prickar över värdens röda blodkroppar, kallade "Sinton och Mulligans stippling". Schizonter uppträder, på samma sätt som andra Plasmodium- arter, som kluster av lila merozoiter som omger ett centralt mörkfärgat pigment.
På grund av den morfologiska likheten mellan Plasmodium -arter är feldiagnostik av P. knowlesi- infektion som P. falciparum , P. malariae eller P. vivax vanligt. Medan vissa snabba diagnostiska tester kan detektera P. knowlesi , tenderar de att ha dålig känslighet och specificitet och är därför inte alltid tillförlitliga. Detektion av nukleinsyra med PCR eller realtids-PCR är den mest tillförlitliga metoden för att detektera P. knowlesi och skilja den från andra Plasmodium -arter infektion. Men på grund av den relativt långsamma och dyra naturen hos PCR är detta inte tillgängligt i många endemiska områden. Slingförmedlade isotermiska amplifieringsmetoder för P. knowlesi- detektion har också utvecklats, men är ännu inte allmänt använda.
Behandling
Eftersom P. knowlesi bara tar 24 timmar att slutföra sin erytrocytcykel, kan det snabbt resultera i mycket höga nivåer av parasitemi med dödliga konsekvenser. För dem med okomplicerad malaria rekommenderar Världshälsoorganisationen behandling med artemisininbaserad kombinationsterapi ( ACT) eller klorokin . För personer med svår malaria rekommenderar Världshälsoorganisationen administrering av intravenöst artesunat i minst 24 timmar, följt av ACT-behandling. Dessutom har tidiga läkemedelsprövningar föreslagit att kombinationer av klorokin och primakin , artesunat och meflokin , artemeter och lumefantrin , och klorokin enbart kan vara effektiva behandlingar för okomplicerad P. knowlesi -malaria. Det finns inga bevis för att P. knowlesi utvecklar resistens mot nuvarande antimalariamedel.
Epidemiologi
P. knowlesi är den vanligaste orsaken till malaria i Malaysia , och fall av P. knowlesi- malaria har rapporterats i de flesta länder i Sydostasien såväl som resenärer från regionen.
Infektion med P. knowlesi är förknippad med socioekonomiska faktorer och livsstilsfaktorer som för människor in i de täta skogarna där myggvärdarna är vanliga. I synnerhet de som arbetar i skogen eller i dess marginal, såsom bönder, jägare och skogshuggare, löper ökad risk för infektion. Sannolikt av denna anledning smittas män oftare än kvinnor, och vuxna infekteras oftare än barn.
Forskning
P. knowlesi har länge använts som en forskningsmodell för att studera interaktionen mellan parasit och värd, och utveckla antimalariavacciner och läkemedel. Dess användbarhet som forskningsmodell beror delvis på dess förmåga att infektera rhesus makaker, en vanlig laboratoriemodell primat. Rhesus-makaker är mycket mottagliga för P. knowlesi och kan infekteras av myggbett, injektion av sporozoiter eller injektion av parasiter i blodstadiet. Infekterade apor utvecklar vissa kännetecken för mänsklig malaria inklusive anemi och förstoring av mjälten och levern. Infektion är vanligtvis dödlig om den inte behandlas, med dödsorsaken till synes cirkulationssvikt kännetecknad av vidhäftning av infekterade röda blodkroppar till blodkärlsväggarna . Apor kan botas från infektion genom behandling med antimalariamedel; Upprepad infektion följt av botemedel resulterar i att aporna utvecklar viss immunitet mot infektion, ett ämne som också har varit föremål för omfattande forskning.
P. knowlesi används också för in vitro -forskning inom Plasmodium- cellbiologi. Isolerade sporozoiter kan infektera primära rhesus- hepatocyter , vilket möjliggör in vitro- studie av parasitleverstadiet. Dessutom P. knowlesi och P. falciparum de enda Plasmodium -arterna som kan bibehållas kontinuerligt i odlade röda blodkroppar, både rhesus och människor. För att underlätta molekylärbiologisk forskning P. knowlesi -genomet sekvenserats och är tillgängligt på PlasmoDB och andra onlineförråd. P. knowlesi kan genetiskt modifieras i labbet genom transfektion antingen i rhesus macaque-modellsystemet eller i blodcellsodling. Blodsmittande stadier och sporozoiter kan lagras under lång tid genom att frysa med glycerolyt, vilket möjliggör bevarandet av intressanta stammar.
Historia
Den italienska läkaren Giuseppe Franchini beskrev först vad som kan ha varit P. knowlesi 1927 när han noterade en parasit skild från P. cynomolgi och P. inui i blodet på en långsvansmakak. 1931 sågs parasiten igen i en långsvansmakak av HGM Campbell under hans arbete med kala azar ( visceral leishmaniasis) i Calcutta ; Campbells kollega Lionel Everard Napier tog blod från den drabbade apan och inokulerade tre laboratorieapor, varav en var en rhesusmakak som utvecklade en allvarlig infektion. Campbell och Napier gav den infekterade apan till Biraj Mohan Das Gupta som kunde underhålla parasiten genom seriepassage genom apor. 1932 beskrev Das Gupta och hans handledare Robert Knowles parasitens morfologi i makakblod och visade att den kunde infektera tre mänskliga patienter (i varje fall användes den för att framkalla feber med hopp om att behandla en annan infektion). Också 1932 John Sinton och HW Mulligan ytterligare parasitens morfologi i blodkroppar, fastställde att den var en distinkt art från andra beskrivna arter och gav den namnet Plasmodium knowlesi för att hedra Robert Knowles.
Strax därefter, 1935 CE, rapporterade Van Rooyen och George R. Pile att de använde P. knowlesi- infektion för att behandla allmän förlamning hos psykiatriska patienter. P. knowlesi skulle fortsätta att användas som ett allmänt pyretiskt medel för olika sjukdomar, särskilt neurosyfilis för vilka det användes fram till åtminstone 1955. Medan Cyril Garnham hade föreslagit 1957 att P. knowlesi naturligt skulle kunna infektera människor, det första dokumenterade fallet av en människa naturligt infekterad med P. knowlesi var 1965 i en lantmätare från den amerikanska armén som utvecklade frossa och feber efter en fem dagar lång utplacering i Malaysia. Baserat på detta fynd genomförde ett team vid Institutet för medicinsk forskning på halvön Malaysia en undersökning av människor som bor i närheten av makaker, men lyckades inte hitta bevis för att apmalaria överfördes till människor.
Under 1960- och 1970-talen använde vetenskapliga forskargrupper P. knowlesi som en forskningsmodell för att göra avgörande upptäckter i malaria. 1965 och 1972 karakteriserade flera grupper hur P. knowlesi antigenvariation bidrog till immunflykt och kronisk infektion. 1975 visade Louis H. Miller och andra att P. knowlesi krävde Duffy-faktor på ytan av röda blodkroppar för att kunna invadera dem (de skulle fortsätta att visa samma krav för P. vivax ett år senare).
Arbetet med P. knowlesi som en mänsklig malariaparasit återupplivades 2004, när Balbir Singh och andra använde PCR för att visa att över hälften av en grupp människor som diagnostiserats med P. malariae -malaria i malaysiska Borneo faktiskt var infekterade med P. knowlesi . Under det följande decenniet använde flera utredare molekylära detektionsmetoder som kan skilja P. knowlesi från morfologiskt liknande parasiter för att tillskriva en ökande andel malariafall till P. knowlesi i hela Sydostasien. Arbete med arkivprover har visat att infektion med denna parasit har förekommit i Malaysia åtminstone sedan 1990-talet.
externa länkar
- CDC malariasida
- WHO:s malariasida
- P. knowlesi genomdata
- Kortfilm om upptäckten av P. knowlesis roll i mänsklig malaria



