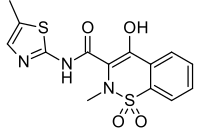
Meloxicam
 | |
 | |
| Kliniska data | |
|---|---|
| Handelsnamn | Mobic, Metacam, Anjeso, andra |
| AHFS / Drugs.com | Monografi |
| MedlinePlus | a601242 |
| Licensdata | |
Graviditetskategori _ |
|
Administreringsvägar _ |
Genom munnen , intravenöst |
| ATC-kod | |
| Rättslig status | |
| Rättslig status | |
| Farmakokinetiska data | |
| Biotillgänglighet | 89 % |
| Proteinbindning | 99,4 % |
| Ämnesomsättning | Lever ( CYP2C9 och 3A4 -medierad) |
| Eliminationshalveringstid _ | 20 timmar |
| Exkretion | Urin och avföring lika |
| Identifierare | |
| |
| CAS-nummer | |
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| PDB-ligand | |
| CompTox Dashboard ( EPA ) | |
| ECHA InfoCard | 100.113.257 |
| Kemiska och fysikaliska data | |
| Formel | C14H13N3O4S2 _ _ _ _ _ _ _ _ _ |
| Molar massa | 351,40 g·mol -1 |
| 3D-modell ( JSmol ) | |
| |
| |
|
| |
Meloxicam , som bland annat säljs under varumärket Mobic , är en icke-steroid antiinflammatorisk medicin (NSAID) som används för att behandla smärta och inflammation vid reumatiska sjukdomar och artros . Det används genom munnen eller genom injektion i en ven . Det rekommenderas att det används under så kort tid som möjligt och i en låg dos.
Vanliga biverkningar inkluderar buksmärtor, yrsel, svullnad, huvudvärk och utslag. Allvarliga biverkningar kan inkludera hjärtsjukdomar , stroke , njurproblem och magsår . Användning rekommenderas inte under tredje trimestern av graviditeten . Det blockerar cyklooxygenas-2 (COX-2) mer än det blockerar cyklooxygenas-1 (COX-1). Det är i oxikamfamiljen av kemikalier och är nära besläktat med piroxikam .
Meloxicam patenterades 1977 och godkändes för medicinsk användning i USA 2000. Det utvecklades av Boehringer Ingelheim ; men det är också tillgängligt som ett generiskt läkemedel . År 2020 var det det 28:e vanligaste läkemedlet i USA, med mer än 19 miljoner recept. En intravenös version av meloxicam (Anjeso) godkändes för medicinsk användning i USA i februari 2020.
Skadliga effekter
Användning av meloxikam kan resultera i gastrointestinal toxicitet och blödning, huvudvärk, utslag och mycket mörk eller svart avföring (ett tecken på tarmblödning). Det har färre gastrointestinala biverkningar än diklofenak , piroxikam , naproxen och kanske alla andra NSAID som inte är COX-2-selektiva.
krävde US Food and Drug Administration (FDA) att läkemedelsetiketten skulle uppdateras för alla icke-steroida antiinflammatoriska läkemedel för att beskriva risken för njurproblem hos ofödda barn som resulterar i lågt fostervatten. De rekommenderar att man undviker NSAID hos gravida kvinnor vid 20 veckor eller senare under graviditeten.
Kardiovaskulär
Liksom andra NSAID är dess användning associerad med en ökad risk för kardiovaskulära händelser som hjärtinfarkt och stroke . Även om meloxikam hämmar bildandet av tromboxan A, verkar det inte göra det vid nivåer som skulle störa trombocytfunktionen . En poolad analys av randomiserade, kontrollerade studier av meloxikambehandling med upp till 60 dagars varaktighet fann att meloxikam var associerat med ett statistiskt signifikant lägre antal tromboemboliska komplikationer än NSAID:t diklofenak (0,2 % respektive 0,8 %) men en liknande incidens av tromboemboliska händelser till naproxen och piroxikam.
Personer med högt blodtryck , högt kolesterol eller diabetes löper risk för kardiovaskulära biverkningar. Personer med familjehistoria av hjärtsjukdom, hjärtinfarkt eller stroke bör berätta för sin behandlande läkare eftersom risken för allvarliga kardiovaskulära biverkningar är betydande.
Gastrointestinala
NSAID orsakar och ökar risken för allvarliga gastrointestinala biverkningar inklusive blödning, sårbildning och perforering av magen eller tarmarna, vilket kan vara dödligt. Äldre patienter löper större risk för allvarliga gastrointestinala händelser.
Mun
Det rekommenderas att avstå från användning av meloxikam i minst fyra till sex halveringstider före kirurgiska eller dentala ingrepp på grund av ökad risk för smakförvrängning, ulcerös stomatit och muntorrhet . [ läkarintyg behövs ]
Handlingsmekanism
Meloxikam blockerar cyklooxygenas (COX), enzymet som ansvarar för att omvandla arakidonsyra till prostaglandin H 2 - det första steget i syntesen av prostaglandiner , som är mediatorer av inflammation. Meloxikam har visat sig, särskilt vid låga terapeutiska doser , selektivt hämma COX-2 framför COX-1 .
Meloxikamkoncentrationerna i ledvätskan varierar från 40 % till 50 % av koncentrationerna i plasma . Den fria fraktionen i ledvätskan är 2,5 gånger högre än i plasma, på grund av det lägre albumininnehållet i ledvätskan jämfört med plasma. Betydelsen av denna penetration är okänd, men det kan förklara det faktum att den presterar exceptionellt bra vid behandling av artrit i djurmodeller.
Farmakokinetik
Absorption
Biotillgängligheten av meloxikam minskar vid oral administrering jämfört med en ekvivalent IV bolusdos. Användning av oralt meloxikam efter en frukost med hög fetthalt ökar de genomsnittliga högsta läkemedelsnivåerna med cirka 22 %; dock ger tillverkaren inga specifika måltidsrekommendationer. Dessutom visar användningen av antacida inte farmakokinetiska interaktioner.
Distribution
Den genomsnittliga distributionsvolymen för meloxikam är cirka 10 L. Det är starkt proteinbundet, främst till albumin .
Ämnesomsättning
Meloxikam metaboliseras i stor utsträckning i levern av enzymerna CYP2C9 och CYP3A4 (minor) till fyra inaktiva metaboliter. Peroxidasaktivitet tros vara ansvarig för de andra två återstående metaboliterna.
Exkretion
Meloxikam utsöndras huvudsakligen i form av metaboliter och förekommer i lika stor utsträckning i urin och avföring. Spår av oförändrat moderläkemedel finns i urin och avföring. Den genomsnittliga halveringstiden för eliminering varierar från 15 till 20 timmar.
Specifika populationer
Geriatri
Användning av meloxikam rekommenderas inte till personer med magsår eller ökad gastrointestinal blödningsrisk, inklusive de över 75 år eller de som tar mediciner associerade med blödningsrisk. Biverkningar har visat sig vara dosberoende och associerade med behandlingens längd.
Veterinär användning
Meloxikam används inom veterinärmedicin för att behandla hundar, men används även på andra djur som nötkreatur och exotiska djur.
De vanligaste biverkningarna inkluderar irritation i mag-tarmkanalen (kräkningar, diarré och sårbildning ).
Hos friska hundar som fått meloxikam har inga perioperativa biverkningar på det kardiovaskulära systemet rapporterats vid rekommenderade doser. Peroperativ administrering av meloxikam till katter påverkade inte postoperativ andningsfrekvens eller hjärtfrekvens.
En peer-reviewed tidskriftsartikel citerar NSAID, inklusive meloxikam, som orsakar gastrointestinala störningar och, vid höga doser, akut njurskada och CNS -tecken som kramper och koma hos katter. Det tillägger att katter har låg tolerans för NSAID.
Ingen nedgång i njurutsöndringsfunktionen observerades när meloxikam administrerades till katter med kronisk njursjukdom. Katter som fick meloxikam hade större proteinuri efter 6 månader än katter som fick placebo. Man drog slutsatsen att meloxikam bör användas med försiktighet till katter med kronisk njursjukdom.
Meloxikam har undersökts som ett alternativ till diklofenak av Royal Society for the Protection of Birds ( RSPB) för att förhindra dödsfall av gamar .
Farmakokinetik
Hos hundar påverkas inte absorptionen av meloxikam från magsäcken av närvaron av foder, med den maximala koncentrationen ( Cmax ) av meloxikam som inträffar i blodet 7–8 timmar efter administrering. Halveringstiden för meloxikam är cirka 24 timmar hos hundar .
I koalan ( Phascolarctos cinereus ) absorberas mycket lite meloxikam i blodet efter oral administrering (det vill säga den har dålig biotillgänglighet ).
Rättslig status
Förenta staterna
År 2003 godkändes meloxikam i USA för användning till hundar för behandling av smärta och inflammation i samband med artros , som en oral ( flytande ) formulering av meloxikam. I januari 2005 lade produktbilagan till en varning i fetstil: "Använd inte till katter." En injicerbar formulering för användning på hundar godkändes av US Food and Drug Administration ( FDA) i november 2003.
I oktober 2004 godkändes en formulering för användning på katter endast för användning före operation. Detta är ett injicerbart meloxikam, indicerat för endast en engångsdos, med specifika och upprepade varningar för att inte administrera en andra dos.
År 2005 skickade FDA ett meddelande om överträdelse till tillverkaren för dess reklammaterial som inkluderade marknadsföring av läkemedlet för off-label användning.
I februari 2020 godkändes meloxikaminjektion för användning i USA. FDA beviljade godkännande av Anjeso till Baudax Bio.
europeiska unionen
I Europa är produkten licensierad för andra antiinflammatoriska fördelar inklusive lindring av både akut och kronisk smärta hos hundar. Meloxicam är också licensierad för användning på hästar, för att lindra smärtan i samband med muskel- och skelettbesvär.
Meloxicam godkändes för användning på nötkreatur i hela Europeiska unionen i januari 1998, genom ett centraliserat marknadsföringstillstånd . Den första generiska meloxikamprodukten godkändes 2006.
Andra länder
Från och med juni 2008 är meloxikam registrerat för långtidsanvändning hos katter i Australien, Nya Zeeland och Kanada.
Se även
externa länkar
- "Meloxicam" . Läkemedelsinformationsportal . US National Library of Medicine.