BRCA2
| BRCA2 | |||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
| Identifierare | |||||||||||||||||||||||||||||||||||||||||||||||
| , BRCC2, BROVCA2, FACD, FAD, FAD1, FANCD, FANCD1, GLM3, PNCA2, XRCC11, bröstcancer 2, DNA-reparationsassocierad, bröstcancer 2, tidig debut, BRCA2 DNA-reparationsassocierad, gener Externa ID: | |||||||||||||||||||||||||||||||||||||||||||||||
| n | |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
| Wikidata | |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
BRCA2 och BRCA2 ( / ˌ b r æ k ə ˈ t uː / ) är en mänsklig gen respektive dess proteinprodukt . Den officiella symbolen (BRCA2, kursiv för genen, icke-kursiv för proteinet) och det officiella namnet (ursprungligen bröstcancer 2 ; för närvarande BRCA2, DNA - reparationsassocierad ) underhålls av HUGO Gennomenklaturkommittén . En alternativ symbol, FANCD1 , känner igen dess association med FANC- proteinkomplexet. Orthologer , utformade Brca2 och Brca2, är vanliga i andra ryggradsdjurarter . BRCA2 är en human tumörsuppressorgen (specifikt en vårdande gen ), som finns i alla människor; dess protein , även kallat av synonymen bröstcancer typ 2-känslighetsprotein , är ansvarigt för att reparera DNA.
BRCA2 och BRCA1 uttrycks normalt i cellerna i bröst och annan vävnad, där de hjälper till att reparera skadat DNA eller förstöra celler om DNA inte kan repareras. De är involverade i reparationen av kromosomskador med en viktig roll i felfri reparation av DNA- dubbelsträngsbrott. Om BRCA1 eller BRCA2 i sig skadas av en BRCA- mutation repareras inte skadat DNA ordentligt, vilket ökar risken för bröstcancer . BRCA1 och BRCA2 har beskrivits som "bröstcancerkänslighetsgener" och "bröstcancermottaglighetsproteiner". Den dominerande allelen har en normal tumörundertryckande funktion medan mutationer med hög penetrans i dessa gener orsakar en förlust av tumörundertryckande funktion, vilket korrelerar med en ökad risk för bröstcancer.
BRCA2 - genen är lokaliserad på den långa (q) armen av kromosom 13 i position 12.3 (13q12.3). Den mänskliga referensgenen BRCA2 innehåller 27 exoner och cDNA har 10 254 baspar som kodar för ett protein med 3418 aminosyror.
Fungera

Även om strukturerna för BRCA1- och BRCA2 -generna är mycket olika, är åtminstone vissa funktioner relaterade till varandra. Proteinerna som tillverkas av båda generna är väsentliga för att reparera skadat DNA (se figur över rekombinationssteg för reparation) . BRCA2 binder enkelsträngat DNA och interagerar direkt med rekombinaset RAD51 för att stimulera och upprätthålla stränginvasion, ett viktigt steg för homolog rekombination . Lokaliseringen av RAD51 till DNA-dubbelsträngbrottet kräver bildandet av BRCA1-PALB2-BRCA2-komplexet. PALB2 (Partner och lokaliserare av BRCA2) kan fungera synergistiskt med en BRCA2-chimär (kallad piccolo eller piBRCA2) för att ytterligare främja stränginvasion. Dessa avbrott kan orsakas av naturlig och medicinsk strålning eller annan miljöexponering, men uppstår också när kromosomerna utbyter genetiskt material under en speciell typ av celldelning som skapar spermier och ägg ( meios ). Dubbelsträngsbrott genereras också under reparation av DNA-tvärlänkar. Genom att reparera DNA spelar dessa proteiner en roll för att upprätthålla stabiliteten hos det mänskliga genomet och förhindrar farliga genomläggningar som kan leda till hematologiska och andra cancerformer.
BRCA2 har visat sig ha en avgörande roll i skyddet från den MRE11 -beroende nukleolytiska nedbrytningen av de omvända gafflarna som bildas under DNA-replikationsgaffelns avstängning (orsakad av hinder som mutationer, interkalerande medel etc.).
Liksom BRCA1 reglerar BRCA2 förmodligen aktiviteten hos andra gener och spelar en avgörande roll i embryonutvecklingen.
Klinisk signifikans
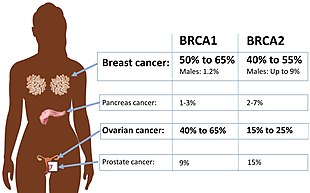
Vissa varianter av BRCA2 -genen ökar risken för bröstcancer som en del av ett ärftligt bröst-äggstockscancersyndrom . Forskare har identifierat hundratals mutationer i BRCA2 -genen, av vilka många orsakar en ökad risk för cancer. BRCA2- mutationer är vanligtvis insättningar eller deletioner av ett litet antal DNA-baspar i genen. Som ett resultat av dessa mutationer är proteinprodukten från BRCA2 -genen onormal och fungerar inte korrekt. Forskare tror att det defekta BRCA2- proteinet inte kan fixa DNA-skador som uppstår i hela genomet. Som ett resultat av detta finns en ökning av mutationer på grund av felbenägen translesionssyntes efter ej reparerad DNA-skada, och vissa av dessa mutationer kan få celler att dela sig på ett okontrollerat sätt och bilda en tumör.
Människor som har två muterade kopior av BRCA2 -genen har en typ av Fanconi-anemi . Detta tillstånd orsakas av extremt reducerade nivåer av BRCA2-proteinet i celler, vilket möjliggör ackumulering av skadat DNA. Patienter med Fanconi-anemi är benägna att få flera typer av leukemi (en typ av blodcellscancer); solida tumörer, särskilt i huvudet, halsen, huden och reproduktionsorganen; och benmärgsdämpning (minskad blodcellsproduktion som leder till anemi ). Kvinnor som har ärvt en defekt BRCA1- eller BRCA2 -gen har risker för bröst- och äggstockscancer som är så höga och verkar så selektiva att många mutationsbärare väljer att genomgå profylaktisk kirurgi . Det har förekommit många gissningar som förklarar en sådan till synes slående vävnadsspecificitet. Viktiga bestämningsfaktorer för var BRCA1- och BRCA2 -associerade ärftliga cancerformer uppstår är relaterade till cancerpatogenens vävnadsspecificitet, medlet som orsakar kronisk inflammation eller cancerframkallande ämne. Målvävnaden kan ha receptorer för patogenen, bli selektivt exponerad för cancerframkallande ämnen och en infektiös process. Ett medfött genomiskt underskott försämrar normala svar och förvärrar känsligheten för sjukdomar i organmål. Denna teori passar även data för flera tumörsuppressorer utöver BRCA1 eller BRCA2 . En stor fördel med denna modell är att den antyder att det finns några alternativ utöver profylaktisk kirurgi.
Utöver bröstcancer hos män och kvinnor leder mutationer i BRCA2 också till en ökad risk för äggstockscancer , livmoderrörs- , prostatacancer och pankreascancer . I vissa studier har mutationer i den centrala delen av genen förknippats med högre risk för äggstockscancer och lägre risk för prostatacancer än mutationer i andra delar av genen. Flera andra typer av cancer har också setts i vissa familjer med BRCA2- mutationer.
I allmänhet står starkt nedärvda genmutationer (inklusive mutationer i BRCA2 ) endast för 5-10 % av fallen av bröstcancer; den specifika risken att få bröstcancer eller annan cancer för alla som bär på en BRCA2 -mutation beror på många faktorer.
Historia
| BRCA2-genen upptäcktes 1994. 1996 identifierade Kenneth Offit och hans forskargrupp vid Memorial Sloan Kettering Cancer Center framgångsrikt den vanligaste mutationen på genen associerad med bröst- och äggstockscancer bland individer av Ashkenazi-judiska härkomst. Genen klonades först av forskare vid Myriad Genetics , Endo Recherche, Inc., HSC Research & Development Limited Partnership och University of Pennsylvania . Metoder för att diagnostisera sannolikheten för att en patient med mutationer i BRCA1 och BRCA2 ska få cancer täcktes av patent som ägs eller kontrolleras av Myriad Genetics . Myriads affärsmodell att uteslutande erbjuda det diagnostiska testet ledde från Myriads början som ett startup 1994 till att det var ett börsnoterat företag med 1200 anställda och cirka 500 miljoner USD i årlig omsättning 2012; det ledde också till kontroverser över höga testpriser och otillgängligheten av andra åsikter från andra diagnostiska laboratorier, vilket i sin tur ledde till stämningsansökan för landmärke Association for Molecular Pathology v. Myriad Genetics . Könslinjemutationer och grundareffektAlla könslinje BRCA2-mutationer som hittills identifierats har ärvts, vilket tyder på möjligheten av en stor "grundare"-effekt där en viss mutation är gemensam för en väldefinierad befolkningsgrupp och teoretiskt kan spåras tillbaka till en gemensam förfader. Med tanke på komplexiteten i mutationsscreening för BRCA2, kan dessa vanliga mutationer förenkla metoderna som krävs för mutationsscreening i vissa populationer. Analys av mutationer som uppträder med hög frekvens tillåter också studier av deras kliniska uttryck. Ett slående exempel på en grundarmutation finns på Island, där en enda BRCA2 (999del5) mutation står för praktiskt taget alla bröst-/äggstockscancerfamiljer. Denna ramförskjutningsmutation leder till en starkt trunkerad proteinprodukt. I en stor studie som undersökte hundratals cancer- och kontrollindivider hittades denna 999del5-mutation hos 0,6 % av den allmänna befolkningen. Observera att medan 72 % av patienterna som visade sig vara bärare hade en måttlig eller stark familjehistoria av bröstcancer, hade 28 % liten eller ingen familjehistoria av sjukdomen. Detta tyder starkt på närvaron av modifierande gener som påverkar det fenotypiska uttrycket av denna mutation, eller möjligen interaktionen av BRCA2-mutationen med miljöfaktorer. Ytterligare exempel på grundarmutationer i BRCA2 ges i tabellen nedan.
MeiosHos växten Arabidopsis thaliana orsakar förlust av BRCA2 -homologen AtBRCA2 allvarliga defekter i både manlig meios och i utvecklingen av den kvinnliga gametocyten . AtBRCA2-protein krävs för korrekt lokalisering av det synaptonemala komplexproteinet AtZYP1 och rekombinaserna AtRAD51 och AtDMC1. Dessutom krävs AtBRCA2 för korrekt meiotisk synapsis. Således är AtBRCA2 sannolikt viktigt för meiotisk rekombination. Det verkar som att AtBRCA2 verkar under meios för att kontrollera de enkelsträngade invasionsstegen som medieras av AtRAD51 och AtDMC1 som inträffar under meiotisk homolog rekombinationell reparation av DNA-skador. Homologer av BRCA2 är också väsentliga för meios i svampen Ustilago maydis , masken Caenorhabditis elegans och fruktflugan Drosophila melanogaster . Möss som producerar trunkerade versioner av BRCA2 är livskraftiga men sterila. BRCA2-muterade råttor har en fenotyp av tillväxthämning och sterilitet hos båda könen. Aspermatogenes hos dessa muterade råttor beror på ett misslyckande i homolog kromosomsynaps under meios. BRC upprepade sekvenserDMC1 (DNA meiotisk rekombinas 1) är en meiosspecifik homolog av RAD51 som förmedlar strängbyte under homolog rekombinationell reparation. DMC1 främjar bildningen av DNA-strängsinvasionsprodukter (ledmolekyler) mellan homologa DNA-molekyler. Human DMC1 interagerar direkt med var och en av en serie upprepade sekvenser i BRCA2-proteinet (kallade BRC-repetitioner) som stimulerar bildning av ledmolekyler av DMC1. BRC-repetitioner överensstämmer med ett motiv som består av en sekvens av cirka 35 högkonserverade aminosyror som finns närvarande minst en gång i alla BRCA2-liknande proteiner. BRCA2 BRC-repetitioner stimulerar bildning av ledmolekyler genom att främja interaktionen av enkelsträngat DNA (ssDNA) med DMC1. Det ssDNA som är komplexbundet med DMC1 kan paras med homologt ssDNA från en annan kromosom under synopsisstadiet av meios för att bilda en ledmolekyl, ett centralt steg i homolog rekombination . Således verkar BRC-repetitionssekvenserna av BRCA2 spela en nyckelroll i rekombinationell reparation av DNA-skador under meiotisk rekombination. Sammantaget verkar det som att homolog rekombination under meios fungerar för att reparera DNA-skador, [ citat behövs ] och att BRCA2 spelar en nyckelroll för att utföra denna funktion. NeurogenesBRCA2 krävs i musen för neurogenes och undertryckande av medulloblastom . ''BRCA2''-förlust påverkar djupt neurogenes, särskilt under embryonal och postnatal neural utveckling. Dessa neurologiska defekter uppstår från DNA-skador. Epigenetisk kontrollEpigenetiska förändringar i uttrycket av BRCA2 (som orsakar överuttryck eller underuttryck) är mycket vanliga i sporadiska cancerformer (se tabell nedan) medan mutationer i BRCA2 sällan hittas. Vid icke-småcellig lungcancer undertrycks BRCA2 epigenetiskt genom hypermetylering av promotorn. I detta fall är promotorhypermetylering signifikant associerad med lågt mRNA- uttryck och lågt proteinuttryck men inte med förlust av heterozygositet hos genen. Vid sporadisk äggstockscancer finner man en motsatt effekt. BRCA2-promotor- och 5'-UTR-regioner har relativt få eller inga metylerade CpG-dinukleotider i tumör-DNA jämfört med icke-tumör-DNA, och en signifikant korrelation finns mellan hypometylering och ett >3-faldigt överuttryck av BRCA2. Detta indikerar att hypometylering av BRCA2-promotorn och 5'-UTR-regionerna leder till överuttryck av BRCA2-mRNA. En rapport indikerade viss epigenetisk kontroll av BRCA2-uttryck av mikroRNA miR-146a och miR-148a. BRCA2 uttryck i cancerI eukaryoter har BRCA2-protein en viktig roll i homolog rekombinationell reparation. Hos möss och människor förmedlar BRCA2 primärt ordnad sammansättning av RAD51 på enkelsträngat (ss) DNA, den form som är aktiv för homolog parning och stränginvasion. BRCA2 omdirigerar också RAD51 från dubbelsträngat DNA och förhindrar dissociation från ssDNA. Dessutom bildar de fyra paralogerna av RAD51 , bestående av RAD51B ( RAD51L1 ), RAD51C (RAD51L2), RAD51D ( RAD51L3 ), XRCC2 ett komplex som kallas BCDX2-komplexet (se figur: Rekombinationell reparation av DNA). Detta komplex deltar i RAD51-rekrytering eller stabilisering på skadeplatser. BCDX2-komplexet verkar verka genom att underlätta sammansättningen eller stabiliteten av nukleoproteinfilamentet RAD51 . RAD51 katalyserar strängöverföring mellan en bruten sekvens och dess oskadade homolog för att möjliggöra återsyntes av den skadade regionen (se homologa rekombinationsmodeller) . Vissa studier av cancer rapporterar överuttryckt BRCA2 medan andra studier rapporterar underuttryck av BRCA2 . Minst två rapporter fann överuttryck i vissa sporadiska brösttumörer och underuttryck i andra sporadiska brösttumörer. (se bordet). Många cancerformer har epigenetiska brister i olika DNA-reparationsgener (se Frekvenser av epimutationer i DNA-reparationsgener i cancer) . Dessa reparationsbrister orsakar sannolikt ökade oreparerade DNA-skador. Överuttrycket av BRCA2 som ses i många cancerformer kan återspegla kompenserande BRCA2 -överuttryck och ökad homolog rekombinationell reparation för att åtminstone delvis hantera sådana överskott av DNA-skador. Egawa et al. tyder på att ökat uttryck av BRCA2 kan förklaras av den genomiska instabilitet som ofta ses i cancer, vilket inducerar BRCA2-mRNA-uttryck på grund av ett ökat behov av BRCA2 för DNA-reparation. Underuttryck av BRCA2 skulle i sig leda till ökade oreparerade DNA-skador. Replikationsfel efter dessa skador (se translesionssyntes ) skulle leda till ökade mutationer och cancer.
InteraktionerBRCA2 har visat sig interagera med Domänarkitektur
BRCA2 innehåller ett antal 39 aminosyraupprepningar som är avgörande för bindning till RAD51 (ett nyckelprotein i DNA-rekombinationell reparation) och resistens mot behandling med metylmetansulfonat . Den spiralformade BRCA2-domänen antar en spiralformad struktur, bestående av en fyra-helix-klusterkärna (alfa 1, alfa 8, alfa 9, alfa 10) och två på varandra följande beta-hårnålar (beta 1 till beta 4). Ett segment på cirka 50 aminosyror som innehåller fyra korta helixar (alfa 2 till alfa 4), slingrar sig runt ytan av kärnstrukturen . I BRCA2 packas alfa 9- och alfa-10-spiralerna med BRCA2 OB1-domänen genom van der Waals- kontakter som involverar hydrofoba och aromatiska rester, och även genom vätebindningar i sidokedjor och ryggrad . Denna domän binder proteinet med 70 aminosyror DSS1 (deleted i split-hand/split foot syndrome), som ursprungligen identifierades som en av tre gener som kartläggs till ett 1,5-Mb locus borttaget i ett ärftligt utvecklingsmissbildningssyndrom. BRCA OB1-domänen antar en OB-vikning, som består av ett kraftigt krökt femsträngat beta-ark som sluter sig själv för att bilda en beta-fat . OB1 har ett grunt spår som bildas av en sida av det krökta arket och avgränsas av två slingor, en mellan beta 1 och beta 2 och en annan mellan beta 4 och beta 5, vilket möjliggör svag enkelsträngad DNA- bindning . Domänen binder också proteinet med 70 aminosyror DSS1 (deleted i split-hand/split foot syndrome). BRCA OB3-domänen antar en OB-vikning, som består av ett mycket krökt femsträngat beta-ark som sluter sig för att bilda en beta-fat . OB3 har ett uttalat spår som bildas av en sida av det böjda arket och avgränsas av två slingor, en mellan beta 1 och beta 2 och en annan mellan beta 4 och beta 5, vilket möjliggör stark ssDNA - bindning . Tower-domänen antar en sekundär struktur som består av ett par långa, antiparallella alfa-helixar (stammen) som stödjer en tre-helixbunt (3HB) vid sin ände. 3HB innehåller ett helix-turn-helix- motiv och liknar de DNA- bindande domänerna för de bakteriella platsspecifika rekombinaserna och för eukaryota Myb och homeodomän transkriptionsfaktorer . Tower-domänen har en viktig roll i BRCA2-tumörsuppressorfunktionen och är väsentlig för lämplig bindning av BRCA2 till DNA . Patent, verkställighet, rättstvister och kontroverserEn patentansökan för den isolerade genen BRCA1 och cancer-cancerfrämjande mutationer, samt metoder för att diagnostisera sannolikheten för att få bröstcancer, lämnades in av University of Utah, National Institute of Environmental Health Sciences (NIEHS) och Myriad Genetics 1994 ; under nästa år isolerade och sekvenserade Myriad i samarbete med andra utredare BRCA2-genen och identifierade relevanta mutationer, och det första BRCA2-patentet lämnades in i USA av Myriad och de andra institutionerna 1995. Myriad är exklusiv licenstagare för dessa patent och har verkställt dem i USA mot kliniska diagnostiska laboratorier. Denna affärsmodell ledde från att Myriad var en startup 1994 till att vara ett börsnoterat företag med 1200 anställda och cirka 500 miljoner USD i årlig omsättning 2012; det ledde också till kontroverser över höga priser och oförmågan att få andra åsikter från andra diagnostiska laboratorier, vilket i sin tur ledde till stämningen Association for Molecular Pathology v. Myriad Genetics . Patenten börjar löpa ut 2014. Peter Meldrum, VD för Myriad Genetics, har erkänt att Myriad har "andra konkurrensfördelar som kan göra sådan [patent]tillämpning onödig" i Europa. Rättsliga beslut kring BRCA1- och BRCA2-patenten kommer att påverka området för genetisk testning i allmänhet. I juni 2013, i Association for Molecular Pathology v. Myriad Genetics (nr 12-398), beslutade USA:s högsta domstol enhälligt att "Ett naturligt förekommande DNA-segment är en naturprodukt och inte patentberättigat bara för att det har isolerats ," ogiltigförklarar Myriads patent på generna BRCA1 och BRCA2. Men domstolen ansåg också att manipulation av en gen för att skapa något som inte finns i naturen fortfarande kan vara berättigat till patentskydd. Den federala domstolen i Australien kom till motsatt slutsats och bekräftade giltigheten av ett australiensiskt Myriad Genetics-patent över BRCA1-genen i februari 2013, men detta beslut överklagas och överklagandet kommer att omfatta övervägande av USA:s högsta domstols beslut. Vidare läsning
externa länkar
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||