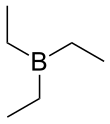
Trietylboran
|
|
|||
| Namn | |||
|---|---|---|---|
|
Föredraget IUPAC-namn
Trietylboran |
|||
| Andra namn Trietylbor, trietylbor
|
|||
| Identifierare | |||
|
3D-modell ( JSmol )
|
|||
| ChemSpider | |||
| ECHA InfoCard | 100.002.383 | ||
| EG-nummer |
|
||
|
PubChem CID
|
|||
| UNII | |||
|
CompTox Dashboard ( EPA )
|
|||
|
|||
|
|||
| Egenskaper | |||
| (CH 3 CH 2 ) 3 B | |||
| Molar massa | 98,00 g/mol | ||
| Utseende | Färglös vätska | ||
| Densitet | 0,677 g/cm 3 | ||
| Smältpunkt | −93 °C (−135 °F; 180 K) | ||
| Kokpunkt | 95 °C (203 °F; 368 K) | ||
| Inte tillämpbar; mycket reaktiv | |||
| Faror | |||
| Arbetsmiljö och hälsa (OHS/OSH): | |||
|
Huvudsakliga faror
|
Spontant brandfarligt i luft; orsakar brännskador | ||
| GHS- märkning : | |||
   
|
|||
| Fara | |||
| H225 , H250 , H301 , H314 , H330 , H360 | |||
| P201 , P202 , P210 , P222 , P233 , P240 , P241 , P242 , P243 , P260 , P264 , P270 , P271 , P280 , P281 , P2081 , P3014 +, P3014+, P3014+ , P3014+, P3014+ , P3014 +, , P302+P334 , P303 + P361+ P353 , P304+P340 , P305+P351+P338 , P308+P313 , P310 , P320 , P321 , P330 , P363 , P370+P378 , P403 + P233 3+ 4 P 5 P 20 , P5 1 | |||
| NFPA 704 (branddiamant) | |||
| Flampunkt | < −20 °C (−4 °F; 253 K) | ||
| −20 °C (−4 °F; 253 K) | |||
| Säkerhetsdatablad (SDS) | Externt säkerhetsdatablad | ||
| Besläktade föreningar | |||
|
Besläktade föreningar
|
|
||
|
Om inte annat anges ges data för material i standardtillstånd (vid 25 °C [77 °F], 100 kPa).
|
|||
Trietylboran ( TEB ), även kallad trietylbor , är en organoboran (en förening med en B-C-bindning). Det är en färglös pyrofor vätska. Dess kemiska formel är (CH 3 CH 2 ) 3 B eller (C 2 H 5 ) 3 B , förkortat Et 3 B . Det är lösligt i organiska lösningsmedel tetrahydrofuran och hexan .
Förberedelse och struktur
Trietylboran framställs genom reaktion av trimetylborat med trietylaluminium :
- Et3Al + (MeO) 3B → Et3B + (MeO ) 3Al
Molekylen är monomer, till skillnad från H 3 B och Et 3 Al, som tenderar att dimerisera. Den har en plan BC 3 -kärna.
Ansökningar
Turbojetmotor
Trietylboran användes för att antända JP-7 -bränslet i Pratt & Whitney J58 turbojet / ramjetmotorer som driver Lockheed SR-71 Blackbird och dess föregångare, A-12 OXCART . Trietylboran är lämpligt eftersom det lätt antänds vid exponering för syre. Den valdes som tändmetod av tillförlitlighetsskäl, och i fallet Blackbird, eftersom JP-7-bränsle har mycket låg flyktighet och är svårt att tända. Konventionella tändstift utgjorde en hög risk för felfunktion. Trietylboran användes för att starta varje motor och för att tända efterbrännarna .
Raket
Blandat med 10–15 % trietylaluminium , användes det före lyftet för att tända F-1-motorerna på Saturn V- raketen.
Merlin -motorerna som driver SpaceX Falcon 9 -raketen använder en trietylaluminium- trietylboranblandning (TEA-TEB) som en första och andra stegs tändare .
Firefly Aerospace Alpha- rakettens Reaver-motorer antänds också av en trietylaluminium-trietylboranblandning.
Organisk kemi
Industriellt används trietylboran som initiator i radikalreaktioner , där det är effektivt även vid låga temperaturer. Som initiator kan den ersätta vissa tennorganiska föreningar.
Det reagerar med metallenolater , vilket ger enoxitrietylborater som kan alkyleras vid a-kolatomen i ketonen mer selektivt än i dess frånvaro. Till exempel producerar enolatet från behandling av cyklohexanon med kaliumhydrid 2-allylcyklohexanon i 90 % utbyte när trietylboran är närvarande. Utan den innehåller produktblandningen 43 % av den monoallylerade produkten, 31 % diallylerade cyklohexanoner och 28 % oreagerat utgångsmaterial. Valet av bas och temperatur påverkar om det mer eller mindre stabila enolatet produceras, vilket tillåter kontroll över substituenternas position. Utgående från 2-metylcyklohexanon leder reaktion med kaliumhydrid och trietylboran i THF vid rumstemperatur till det mer substituerade (och mer stabila) enolatet, medan reaktion vid -78 °C med kaliumhexametyldisilazid , KN[ Si ( CH
3 )
3 ]
2 och trietylboran genererar det mindre substituerade (och mindre stabila) enolatet. Efter reaktion med metyljodid ger den förra blandningen 2,2-dimetylcyklohexanon i 90 % utbyte medan den senare ger 2,6-dimetylcyklohexanon i 93 % utbyte.
Det används i Barton–McCombie-deoxygeneringsreaktionen för deoxygenering av alkoholer. I kombination med litiumtri- tert -butoxialuminiumhydrid spjälkar den etrar. Till exempel omvandlas THF, efter hydrolys, till 1-butanol . Det främjar också vissa varianter av Reformatskii-reaktionen .
Trietylboran är prekursorn till reduktionsmedlen litiumtrietylborhydrid (" superhydrid ") och natriumtrietylborhydrid .
- MH + Et3B → MBHEt3 ( M = Li, Na)
Trietylboran reagerar med metanol för att bilda dietyl(metoxi)boran, som används som kelatbildare i Narasaka-Prasad-reduktionen för den stereoselektiva genereringen av syn -1,3- dioler från β-hydroxiketoner.
Säkerhet
Trietylboran är starkt pyrofor , med en självantändningstemperatur på −20 °C (−4 °F), brinner med en äppelgrön låga som är karakteristisk för borföreningar. Således hanteras och lagras den vanligtvis med luftfria tekniker . Trietylboran är också akut giftigt vid förtäring, med en LD50 på 235 mg/kg hos försökspersoner på råtta.