Silverperklorat
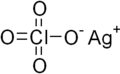
|
|
| Namn | |
|---|---|
|
IUPAC-namn
Silver(I)perklorat
|
|
|
Systematiskt IUPAC-namn
Silver(I)klorat(VII) |
|
| Andra namn Perklorsyra, silver(1+) salt argt perklorat |
|
| Identifierare | |
|
|
|
3D-modell ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard | 100.029.123 |
| EG-nummer |
|
|
PubChem CID
|
|
| UNII | |
|
CompTox Dashboard ( EPA )
|
|
|
|
|
|
| Egenskaper | |
| AgClO 4 | |
| Molar massa | 207,319 g/mol |
| Utseende | Färglösa hygroskopiska kristaller |
| Densitet | 2,806 g/cm 3 |
| Smältpunkt | 486 °C (907 °F; 759 K) (sönderdelas) |
|
557 g/100 ml (25 °C) 792,8 g/100 ml (99 °C) |
|
| Löslighet | löslig i organiska lösningsmedel |
| Strukturera | |
| kubisk | |
| Faror | |
| GHS- märkning : | |
 
|
|
| Fara | |
| H272 , H314 | |
| P210 , P220 , P221 , P260 , P264 , P280 , P301+P330+P331 , P303 + P361 +P353 , P304+ P340 , P305+P351 + P338 , P301 + P338 , P301 + , P321+ , P405 , P501 | |
| NFPA 704 (branddiamant) | |
|
Om inte annat anges ges data för material i standardtillstånd (vid 25 °C [77 °F], 100 kPa).
|
|
Silverperklorat är den kemiska föreningen med formeln AgClO 4 . Denna vita fasta substans bildar ett monohydrat och är milt utflytande . Det är en användbar källa till Ag + -jonen, även om närvaron av perklorat innebär risker. Det används som en katalysator i organisk kemi.
Produktion
Silverperklorat skapas genom att värma upp en blandning av perklorsyra med silvernitrat .
Alternativt kan den framställas genom reaktionen mellan bariumperklorat och silversulfat , eller från reaktionen av perklorsyra med silveroxid .
Löslighet
Silverperklorat är anmärkningsvärt för sin löslighet i aromatiska lösningsmedel som bensen (52,8 g/L) och toluen (1010 g/L). I dessa lösningsmedel binder silverkatjonen till arenen, vilket har visats genom omfattande kristallografiska studier på kristaller erhållna från sådana lösningar. Dess löslighet i vatten är extremt hög, upp till 500 g per 100 ml vatten.
Relaterade reagenser
I likhet med silvernitrat är silverperklorat ett effektivt reagens för att ersätta halogenidligander med perklorat, som är en svagt eller icke-koordinerande anjon . Användningen av silverperklorat i kemisk syntes har minskat på grund av farhågor om explosiviteten hos perkloratsalter. Andra silverreagens är silvertetrafluoroborat och det relaterade silvertrifluormetansulfonatet och silverhexafluorfosfatet .
| HClO4 _ | han | |||||||||||||||||
| LiClO 4 | Be(ClO4)2 |
B(ClO4 ) - 4 B (ClO4)3 |
ROClO 3 |
NH4ClO4NOClO4 N ( ) ClO4 3 |
H 3 OClO 4 | FClO 4 | Ne | |||||||||||
| NaClO4 _ | Mg( ClO4 ) 2 |
Al(ClO4)3 Al(ClO4 ) − 4 Al (ClO4)2−5 3−6 Al (ClO 4 ) |
Si | P | S |
ClO − 4 ClOClO 3 Cl 2 O 7 |
Ar | |||||||||||
| KClO 4 | Ca( ClO4 ) 2 | Sc( ClO4 ) 3 | Ti( ClO4 ) 4 |
VO(ClO 4 ) 3 VO 2 (ClO 4 ) |
Cr( ClO4 ) 3 | Mn(ClO4)2 |
Fe(ClO4 ) 2 Fe (ClO4)3 |
Co(ClO4)2, Co(ClO4)3 |
Ni( ClO4 ) 2 | Cu( ClO4 ) 2 | Zn(ClO4)2 | Ga(ClO4)3 | Ge | Som | Se | Br | Kr | |
| RbClO4 _ | Sr( ClO4 ) 2 | Y(ClO4)3 | Zr( ClO4 ) 4 | Nb(ClO4)5 | Mo | Tc | Ru | Rh( ClO4 ) 3 | Pd(ClO4)2 | AgClO 4 | Cd(ClO4)2 | I (ClO4)3 | Sn(ClO4)4 | Sb | TeO(ClO4)2 | jag | Xe | |
| CsClO4 _ | Ba( ClO4 ) 2 | Lu(ClO4)3 | Hf(ClO4)4 | Ta(ClO4)5 | W | Re | Os | Ir | Pt | Au |
Hg2(ClO4)2, Hg(ClO4)2 |
Tl(ClO4), Tl(ClO4)3 |
Pb( ClO4 ) 2 | Bi(ClO4)3 | Po | På | Rn | |
| FrClO4 | Ra | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
| ↓ | ||||||||||||||||||
| La | Ce(ClO4)x | Pr( ClO4 ) 3 | Nd( ClO4 ) 3 | Pm | Sm(ClO4)3 | Eu(ClO4)3 | Gd(ClO4)3 | Tb(ClO4)3 | Dy(ClO4)3 | Ho(ClO4)3 | Er(ClO4)3 | Tm(ClO4)3 | Yb(ClO4)3 | |||||
| Ac | Th(ClO4)4 | Pa | UO2(ClO4)2 | Np | Pu | Am | Centimeter | Bk | Jfr | Es | Fm | Md | Nej | |||||
