Natriumtrifluoracetat
|
|
|
|
| Namn | |
|---|---|
|
IUPAC-namn
Natriumtrifluoracetat
|
|
| Andra namn Natriumperfluoracetat Natrium 2,2,2-trifluoracetat |
|
| Identifierare | |
|
3D-modell ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard | 100.018.982 |
| EG-nummer |
|
|
PubChem CID
|
|
| UNII | |
|
CompTox Dashboard ( EPA )
|
|
|
|
|
|
| Egenskaper | |
| C 2 F 3 Na O 2 | |
| Molar massa | 136,005 g·mol -1 |
| Utseende | Vitt kristallint pulver |
| Densitet | 1,49 g ml -1 |
| Smältpunkt | 207 °C (405 °F; 480 K) |
| Kokpunkt | Bryts ner |
| 625 g/L | |
| Löslighet | löslig i alkohol , acetonitril , dimetylformamid och de flesta polära organiska lösningsmedel |
| Surhet (p K a ) | 0,23 (konjugerad syra) |
| Faror | |
| Arbetsmiljö och hälsa (OHS/OSH): | |
|
Huvudsakliga faror
|
Giftig, Irriterande, Miljöskadlig |
| GHS- märkning : | |
  
|
|
| Fara | |
| H300 , H315 , H319 , H335 , H410 | |
| P261 , P264 , P270 , P271 , P273 , P280 , P301+P310 , P302+P352 , P304+P340 , P305+P351+P338, P312, P3201, P3201, P3201 , P3201 , P3201 , P3201 , P3201 3 , P362 , P391 , P403 + P233 , P405 , P501 | |
| NFPA 704 (branddiamant) | |
| Flampunkt | Ej brandfarlig |
| Ej brandfarlig | |
| Besläktade föreningar | |
|
Andra anjoner
|
Natriumtrikloracetat |
|
Besläktade föreningar
|
Natriumformiat |
|
Om inte annat anges ges data för material i standardtillstånd (vid 25 °C [77 °F], 100 kPa).
|
|
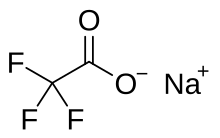
Natriumtrifluoracetat är en kemisk förening med formeln CF 3 CO 2 Na. Det är natriumsaltet av trifluorättiksyra . Det används som en källa till trifluormetyleringar .
Grundläggande
Med ett pKa på 0,23 för trifluorättiksyra är trifluoracetatjonen en extremt svag bas jämfört med ättiksyra som har ett pKa på 4,76. Detta beror på den elektronbortdragande effekten av de tre fluoratomerna intill karboxylatgruppen . Starka syror som saltsyra eller svavelsyra kan protonera trifluoracetatjonen till trifluorättiksyra :
I allmänhet reagerar trifluoracetat i jämvikt med hydroniumkatjoner för att bilda trifluorättiksyra:
Den allmänna reaktionen med hydronium är i jämvikt på grund av likheten i pKa mellan trifluorättiksyra och hydroniumjonen.
Förberedelse
En lämplig metod är att lösa en ekvivalent mängd natriumkarbonat i 50 % vattenlösning av trifluorättiksyra. Lösningen filtreras och indunstas genom vakuumindunstning (med särskild försiktighet för att undvika nedbrytning av saltet genom överhettning). Den erhållna fasta substansen torkas under vakuum vid 100°C.
Används
Natriumtrifluoracetat är ett användbart reagens för trifluormetylering .
Se även
- ^ "Trifluormetylering av karbonylföreningar med natriumtrifluoracetat". Journal of Fluorine Chemistry . 126 (6): 937–940. Juni 2005. doi : 10.1016/j.jfluchem.2005.04.012 .
- ^ Prakash, GK Surya; Mathew, Thomas (2010), "Sodium Trifluoroacetate", Encyclopedia of Reagents for Organic Synthesis , doi : 10.1002/047084289x.rn01136 , ISBN 9780470842898




