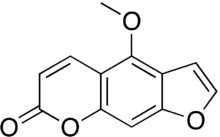
Bergapten
|
|

|
|

|
|
| Namn | |
|---|---|
|
Föredraget IUPAC-namn
4-metoxi-7H - furo[3,2- g ][1]bensopyran-7-on |
|
Andra namn
|
|
| Identifierare | |
|
3D-modell ( JSmol )
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| ECHA InfoCard | 100.006.913 |
| EG-nummer |
|
| KEGG | |
|
PubChem CID
|
|
| UNII | |
| FN-nummer | 1759 |
|
CompTox Dashboard ( EPA )
|
|
|
|
|
|
| Egenskaper | |
| C12H8O4 _ _ _ _ _ | |
| Molar massa | 216,192 g/mol |
| Farmakologi | |
| D05BA03 ( WHO ) | |
|
Om inte annat anges ges data för material i standardtillstånd (vid 25 °C [77 °F], 100 kPa).
|
|
Bergapten ( 5-methoxypsoralen) är en naturligt förekommande organisk kemisk förening som produceras av många växtarter, särskilt från morotsfamiljen Apiaceae och citrusfamiljen Rutaceae . Till exempel har bergapten extraherats från 24 arter av släktet Heracleum i familjen Apiaceae. I familjen Rutaceae innehåller olika citrusarter betydande mängder bergapten, speciellt bergamottapelsinen , micranthaen och vissa varianter av limefrukt och bitter apelsin .
Bergapten tillhör en klass av kemiska föreningar som kallas furanokumarinerna . År 1834 isolerade Kalbrunner 5-methoxypsoralen från bergamott eterisk olja , därav det vanliga namnet "bergapten". Det var det första furanokumarinet som isolerades och identifierades.
Giftighet
Bergapten är ett derivat av psoralen , moderföreningen till en familj av naturligt förekommande organiska föreningar som kallas linjära furanokumariner (så kallade eftersom de uppvisar en linjär kemisk struktur). Några av de linjära furanokumarinerna, inklusive bergapten, fungerar som starka fotosensibilisatorer när de appliceras topiskt på huden.
Bergapten finns ofta i växter associerade med fytofotodermatit , en potentiellt allvarlig hudinflammation. Kontakt med växtdelar som innehåller bergapten (och andra linjära furanokumariner) följt av exponering för ultraviolett ljus kan leda till fytofotodermatit. I synnerhet verkar bergapten vara den primära fototoxiska föreningen som är ansvarig för Citrus -inducerad fytofotodermatit.
Bergapten och andra linjära furanokumariner inducerar en förlust av mallaktivitet för RNA-syntes. 5-metoxipsoralen har också noterats för dess mutagena effekter såväl som dess förmåga att vara ett mycket potent medel för att inducera kromosomavvikelser. Med en tillräckligt hög koncentration observerades fullständig mitotisk hämning.
Det finns tillräckliga bevis för att bergapten främjar cancer hos djur, men sådana bevis för cancerogenicitet hos människor saknas. Enligt International Agency for Research on Cancer är bergapten troligen cancerframkallande för människor.
Medicinsk användning
Bergapten tjänar till att få huden att absorbera mer ljus, och pigmentsjukdomar som vitiligo (leukodermi) och psoriasis har behandlingar som involverar furanokumariner ofta i samband med solexponering eller solstrålning. Hos personer som lätt blir solbrända kan furanokumariner också öka hudens tolerans mot solstrålning. Bergapten visades framkalla vissa hudreaktioner för att jämna ut pigmentering för vitiligopatienter beroende på olika faktorer som patientens mottaglighet, doseringen och luftfuktigheten, men effekterna kan vara inkonsekventa.
Med psoriasis har bergapten värderats som en oral fotokemoterapibehandling för dess effekt och avsaknad av fototoxiska och läkemedelsokänsliga reaktioner. Det fungerar som ett fotosensibiliserande läkemedel som är lika effektivt eller, med tillräckligt hög dosering, mer effektivt än 8-metoxipsoralen för att eliminera psoriasisskador. Det har visat sig vara ett värdefullt alternativ till 8-metoxipsoralen på grund av den relativa bristen på biverkningar under behandling som erytma, klåda och illamående.
Bergapten har också varit inblandad som en potentiell förebyggande metod för solljusrelaterad hudcancer. En studie fann att en solbränna med bergapten hade mindre DNA-skador hos människor. Bergapten har visat sig ha antitumöreffekter, som dess förmåga att inducera den autofagiska processen i bröstcancerceller. En studie föreslog att detta var möjligt genom uppreglering av PTEN-genuttryck i dessa bröstcancerceller.
Bergapten, tillsammans med andra furanokumariner, har också varit inblandad i Cytokrom P450- hämning.
Syntes
Bergapten är en naturlig förening som kommer från växter som det vanliga fikonet, men det kan också syntetiseras. De flesta synteser av linjära furanokumariner innebär att man börjar med en central aromatisk enhet och lägger till två heterocykliska ringar. Alternativa syntesvägar är önskvärda för att undvika regiokemiska problem och måttliga utbyten. Syntesen som beskrivs här involverar jod som en borttagbar grupp för att säkerställa regiokemisk integritet och konvergens. Såsom visas i diagrammet var floroglucinol (förening 1) utgångsmaterialet. Monometylering utfördes följt av en reaktion med etylpropiolat i närvaro av ZnCl2 för att ge 7-hydroxi-5-metoxikumarin (produkt 3, ej visad) med 68 % utbyte. 8-positionen av 7-hydroxi-5-metoxikumarin skyddades sedan av jod för att undvika bildningen av ett kantigt furanokumarin. Produkt 4 i diagrammet är resultatet av det jodskyddet. Produkt 5 var resultatet av allyleringen av produkt 4. Osmiumtetraoxid och natriummetaperjodat användes för att oxidativt klyva O-allylderivatet på aldehydprodukten 7 via en diolmellanprodukt (produkt 6, ej visad). Cyklisering av aldehydprodukten 7 med användning av BF3 - Et20 i tetra- n -butylammoniumbromid utfördes sedan för att konstruera furanringen. Det sista steget var att avlägsna jodskyddsgruppen via Pd(OAc) 2 för att slutligen producera bergapten (produkt 9) med 90 % utbyte. Syntetisk bergapten isolerades som en färglös förening med egenskaper spektroskopiskt identiska med den naturliga produkten.
En känd användning av bergapten är i syntesen av Fraxinol. Nyckelreaktionen i denna syntes är oxidationen av furanringen av visnagin och bergapten med kromsyra.
