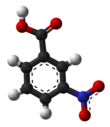
3-nitrobensoesyra
|
|
|||
| Namn | |||
|---|---|---|---|
|
Föredraget IUPAC-namn
3-nitrobensoesyra |
|||
| Andra namn
m -Nitrobensoesyra
|
|||
| Identifierare | |||
|
3D-modell ( JSmol )
|
|||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard | 100.004.099 | ||
|
PubChem CID
|
|||
| UNII | |||
|
CompTox Dashboard ( EPA )
|
|||
|
|||
|
|||
| Egenskaper | |||
| C 7 H 5 N O 4 | |||
| Molar massa | 167,12 g/mol | ||
| Utseende | krämfärgad fast | ||
| Densitet | 1,494 g/cm 3 | ||
| Smältpunkt | 139 till 141 °C (282 till 286 °F; 412 till 414 K) | ||
| 0,24 g/100 ml (15 °C) | |||
| Surhet (p K a ) | 3,47 (i vatten) | ||
| -80,22·10 −6 cm3 / mol | |||
| Besläktade föreningar | |||
|
Besläktade föreningar
|
Bensoesyra Nitrobensen Antranilsyra 3,5-Dinitrobensoesyra 2-Nitrobensoesyra 4-Nitrobensoesyra |
||
|
Om inte annat anges ges data för material i standardtillstånd (vid 25 °C [77 °F], 100 kPa).
|
|||
3-Nitrobensoesyra är en organisk förening med formeln C 6 H 4 (NO 2 )CO 2 H. Det är en aromatisk förening och under standardförhållanden är det ett benvitt fast ämne. De två substituenterna är i en metaposition i förhållande till varandra, vilket ger det alternativa namnet m -nitrobensoesyra. Denna förening kan vara användbar eftersom den är en föregångare till 3-aminobensoesyra, som används för att framställa vissa färgämnen.
Förberedelse
Den framställs genom nitrering av bensoesyra vid låga temperaturer. Både 2-Nitrobensoesyra och 4-Nitrobensoesyra produceras som biprodukter, med utbyten på cirka 20 % respektive 1,5 %. Eftersom karboxylsyrafunktionella grupper är elektronavdragande , under en elektrofil aromatisk substitutionsreaktion av nitrering, riktas substituenter till en metaposition som förklarar denna regiokemi.
En mindre effektiv väg involverar nitrering av metylbensoat , följt av hydrolys. Alternativt har oxidativ CC-bindningsklyvning av 3-nitroacetofenon till motsvarande arylkarboxylsyra visats. En ytterligare syntes involverar oxidation av 3-nitrobensaldehyd.
Egenskaper
Med ap Ka på 3,47 är 3-nitrobensoesyra ungefär tio gånger surare än bensoesyra . Den konjugerade basen av bensoesyra stabiliseras av närvaron av den elektronavdragande nitrogruppen, vilket förklarar dess ökade surhet jämfört med osubstituerad bensoesyra. Det är vanligtvis lösligt i syresatta och klorerade lösningsmedel.
Reaktivitet
Närvaron av både karboxylsyra- och nitrofunktionella grupper deaktiverar ringen med avseende på elektrofila aromatiska substitutionsreaktioner .
Säkerhet
Föreningen har sannolikt måttlig toxicitet, med LD 50 (iv, mus) på 640 mg/kg. Denna förening kan orsaka hud- och ögonirritation med exponeringssymtom inklusive methemoglobin, sensibilisering, irritation och skada på hornhinnan.
- ^ a b "Dissociationskonstanter av organiska syror och baser" . Hämtad 11 april 2010 .
- ^ a b Takao Maki, Kazuo Takeda (2002). "Bensoesyra och derivat". Ullmanns Encyclopedia of Industrial Chemistry . Weinheim: Wiley-VCH. doi : 10.1002/14356007.a03_555 . .
- ^ Oliver Kamm och JB Segur "m-Nitrobenzoic Acid" Org. Synth. 1923, volym 3, 73. doi : 10.15227/orgsyn.003.0073
- ^ Li, Meichao; Shen, Zhenlu; Xu, Liang; Wang, Shengpeng; Chen, Bajin; Hu, Xinquan; Hu, Baoxiang; Jin, Liqun; Sun, Nan (2018-05-16). "Oxidativ C-C-bindningsklyvning för syntes av arylkarboxylsyror från arylalkylketoner". Synlett . 29 (11): 1505–1509. doi : 10.1055/s-0037-1609751 . ISSN 0936-5214 .
- ^ "20.4 Substituenteffekter på surhet" . Kemi LibreTexts . 2017-08-25 . Hämtad 2018-09-25 .
- ^ Ashford, Edith . Benezit Dictionary of Artists. Vol. 1. Oxford University Press. 2011-10-31. doi : 10.1093/benz/9780199773787.article.b00007872 .
- ^ "16.7: Nukleofil aromatisk substitution" . Kemi LibreTexts . 2015-05-03 . Hämtad 2018-09-25 .
- ^ GOV, NOAA Office of Response and Restoration, US. "M-NITROBENSOSYRA | CAMEO-kemikalier | NOAA" . cameochemicals.noaa.gov . Hämtad 2018-09-25 .