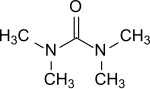
Tetrametylurea
|
|
| Namn | |
|---|---|
|
Föredraget IUPAC-namn
Tetrametylurea |
|
| Andra namn 1,1,3,3-tetrametylurea *TMU |
|
| Identifierare | |
|
3D-modell ( JSmol )
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| ECHA InfoCard | 100.010.159 |
| EG-nummer |
|
|
PubChem CID
|
|
| UNII | |
|
CompTox Dashboard ( EPA )
|
|
|
|
|
|
| Egenskaper | |
| C5H12N2O _ _ _ _ _ _ | |
| Molar massa | 116,164 g·mol -1 |
| Utseende | Färglös vätska |
| Densitet | 0,968 g/ml |
| Smältpunkt | −1,2 °C (29,8 °F; 271,9 K) |
| Kokpunkt | 176,5 °C (349,7 °F; 449,6 K) |
| Faror | |
| GHS- märkning : | |
 
|
|
| Fara | |
| H302 , H360 , H361 | |
| P201 , P202 , P264 , P270 , P281 , P301+P312 , P308+P313 , P330 , P405 , P501 | |
|
Om inte annat anges ges data för material i standardtillstånd (vid 25 °C [77 °F], 100 kPa).
|
|
Tetrametylurea är den organiska föreningen med formeln (Me 2 N) 2 CO. Det är en substituerad urea . Denna färglösa vätska används som ett aprotiskt -polärt lösningsmedel, speciellt för aromatiska föreningar och används t.ex. för Grignard-reagens.
Produktion
Syntesen och egenskaperna hos tetrametylurea beskrevs utförligt.
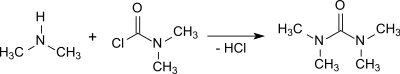
Reaktionen av dimetylamin med fosgen i närvaro av t.ex. 50 % natriumhydroxidlösning och efterföljande extraktion med 1,2-dikloretan ger tetrametylurea i 95 % utbyte.
Reaktionerna med dimetylkarbamoylklorid eller fosgen är mycket exoterma och avlägsnandet av den resulterande dimetylaminhydrokloriden kräver viss ansträngning.
Reaktionen av difenylkarbonat med dimetylamin i en autoklav är också effektiv.
Tetrametylurea bildas vid reaktionen av dimetylkarbamoylklorid med vattenfritt natriumkarbonat i ett utbyte av 96,5 %.
Dimetylkarbamoylklorid reagerar också med överskott av dimetylamin och bildar tetrametylurea. Även om produkten är förorenad och illaluktande kan den renas genom tillsats av kalciumoxid och efterföljande fraktionerad destillation .
Tetrametylurea bildas också under oxidationen av tetrakis(dimetylamino)etylen (TDAE), en mycket elektronrik alken och ett starkt reduktionsmedel, tillgängligt från tris(dimetylamino)metan genom pyrolys eller från klortrifluoreten och dimetylamin.
Tetrakis(dimetylamino)etylen (TDAE) reagerar med syre i en (2+2) cykloadditionsreaktion till en 1,2-dioxetan som sönderdelas till elektroniskt exciterad tetrametylurea. Detta återgår till marktillståndet samtidigt som det avger grönt ljus med ett emissionsmaximum vid 515 nm.
Egenskaper
Tetrametylurea är en klar, färglös vätska med mild aromatisk lukt som är blandbar med vatten och många organiska lösningsmedel. Ovanligt för en urea är det flytande tillståndet för tetrametylurea i ett intervall på > 170 °C.
Ansökningar
Tetrametylurea är blandbar med en mängd olika organiska föreningar, inklusive syror som ättiksyra eller baser som pyridin och ett utmärkt lösningsmedel för organiska ämnen som ε-kaprolaktam eller bensoesyra och löser även vissa oorganiska salter som silvernitrat eller natriumjodid . På grund av dess distinkta lösningsmedelsegenskaper används tetrametylurea ofta som ersättning för den cancerframkallande hexametylfosforamiden (HMPT).
Tetrametylurea är lämpligt som reaktionsmedium för polymerisation av aromatiska disyraklorider (såsom isoftalsyra ) och aromatiska diaminer (såsom 1,3-diaminobensen (m-fenylendiamin)) till aramider såsom poly(m-fenylenisoftalamid) (Nomex) ®)
Polymerisationen av 4-aminobensoesyrakloridhydroklorid i tetrametylurea ger isotropa viskösa lösningar av poly(p-bensamid) (PPB), som kan spinnas direkt till fibrer.
I en tetrametylurea- LiCl -blandning kan stabila isotropa lösningar erhållas upp till en PPB-polymerkoncentration på 14 %.
Tetrametylurea löser också cellulosaester och sväller andra polymerer såsom polykarbonater , polyvinylklorid eller alifatiska polyamider, vanligtvis vid förhöjd temperatur.
Starka och hindrade icke-nukleofila guanidinbaser är tillgängliga från tetrametylurea på ett enkelt sätt, vilket är i motsats till de fusionerade amidinbaserna DBN eller DBU som inte är alkylerade.
En modifiering av Koenigs-Knorr-reaktionen för att bygga glykosider från 2,3,4,6-tetra-O-acetyl-α-D-glukopyranosylbromid (acetobromoglucose) kommer från S. Hanessian som använde silversaltet silvertrifluormetansulfonat ( TfOAg ) och som en protonacceptor tetrametylurea. Denna processvariant kännetecknas av en förenklad processkontroll, hög anomerisk renhet och höga utbyten av produkterna. Om reaktionen utförs med acetobromoglukos och silvertriflat /tetrametylkarbamid vid rumstemperatur, reagerar tetrametylkarbamid inte bara som en bas utan även med glykosylen för att bilda ett bra isolerbart uroniumtriflater med 56 % utbyte.
Säkerhet
Den akuta toxiciteten av tetrametylurea är måttlig. Det är dock embryotoxiskt och teratogent mot flera djurarter.