tert -butylperoxibensoat

|
|
| Namn | |
|---|---|
|
Föredraget IUPAC-namn
tert -butylbensenkarboperoxoat |
|
| Andra namn
tert -butylperbensoat
|
|
| Identifierare | |
|
3D-modell ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard | 100.009.440 |
|
PubChem CID
|
|
| UNII | |
|
CompTox Dashboard ( EPA )
|
|
|
|
|
|
| Egenskaper | |
| C11H14O3 _ _ _ _ _ | |
| Molar massa | 194,230 g·mol -1 |
|
Om inte annat anges ges data för material i standardtillstånd (vid 25 °C [77 °F], 100 kPa).
|
|
tert Butylperoxibensoat C6H5CO2CMe3 ) . - förening med ) Me ( TBPB en organisk formeln ( = CH3 Det är den mest producerade perestern . Det används ofta som en radikalinitiator i polymerisationsreaktioner , såsom framställning av LDPE från eten , och för tvärbindning , såsom för omättade polyesterhartser.
Egenskaper
TBPB, som är svagt gul, förekommer uteslutande som lösning i lösningsmedel som etanol eller ftalat.
Som peroxoförening innehåller TBPB cirka 8,16 viktprocent aktivt syre och har en självaccelererande nedbrytningstemperatur (SADT) på cirka 60 °C. SADT är den lägsta temperatur vid vilken självaccelererande nedbrytning i transportförpackningen kan ske inom en vecka, och som inte bör överskridas under lagring eller transport. TBPB bör därför förvaras mellan minst 10 °C (under stelning ) och maximalt 50 °C. Spädning med ett högkokande lösningsmedel ökar SADT. Halveringstiden för TBPB, i vilken 50 % av peroxiestern sönderdelas, är 10 timmar vid 104 °C, en timme vid 124 °C och en minut vid 165 °C. Aminer, metalljoner , starka syror och baser , samt starka reduktions- och oxidationsmedel påskyndar nedbrytningen av TBPB även i låga koncentrationer. Men TBPB är en av de säkraste perestrarna eller organiska peroxiderna vid hantering. De viktigaste nedbrytningsprodukterna av tert -butylperoxibensoat är koldioxid , aceton , metan , tert -butanol , bensoesyra och bensen .
Produktion
Ett standardförfarande för framställning av perestrar är acylering av tert -butylhydroperoxid med bensoylklorid . I reaktionen används ett stort överskott av tert -butylhydroperoxid och den bildade vätekloriden avlägsnas i vakuum, varigenom ett praktiskt taget kvantitativt utbyte erhålles.
Ansökningar
I polymerkemi
Primärt används TBPB som radikalinitiator , antingen vid polymerisation av t.ex. eten (till LDPE), vinylklorid, styren eller akrylestrar eller som så kallade omättade polyesterhartser (UP-hartser). Mängden som används för härdning av UP-hartser är ca 1-2%.
En nackdel, särskilt vid framställning av polymerer för tillämpningar inom livsmedels- eller kosmetikasektorn, är den möjliga bildningen av bensen som en sönderdelningsprodukt som kan diffundera ut ur polymeren (till exempel en LDPE-förpackningsfilm).
Oorganisk kemi
Skyddsgruppen 2-trimetylsilyletansulfonylklorid (SES-Cl) för primära och sekundära aminogrupper är tillgänglig genom reaktion av vinyltrimetylsilan med natriumvätesulfit och TBPB till natriumsaltet av trimetylsilyletansulfonsyra och den efterföljande reaktionen med tionylklorid till motsvarande sulfonylklorid .
TBPB kan användas för att införa en bensoyloxigrupp i allylpositionen av omättade kolväten.
Från cyklohexen bildas 3-bensoyloxicyklohexen med TBPB i närvaro av katalytiska mängder koppar(I)bromid i 71 till 80 % utbyte.
Denna allyliska oxidation av alkener, även känd som Kharasch-Sosnovsky-oxidation , genererar racemiska allyliska bensoater i närvaro av katalytiska mängder koppar(I)bromid .
En modifiering av reaktionen använder koppar(II)trifluormetansulfonat som katalysator och DBN eller DBU som baser för att uppnå utbyten upp till 80 % vid reaktionen av acykliska olefiner med TBPB till allyliska bensoater.
Substituerade oxazoliner och tiazoliner kan oxideras till motsvarande oxazoler och tiazoler i en modifierad Kharash-Sosnovsky-oxidation med TBPB och en blandning av Cu(I)- och Cu(II)-salter i lämpliga utbyten.
Karboalkoxigruppen i C-4-positionen är väsentlig för en framgångsrik reaktion.
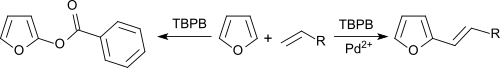
Bensen och furaner kan alkenyleras med olefiner i en oxidativ koppling under palladiumsaltkatalys, med TBPB som väteacceptor.
I frånvaro av Pd2 + -salter bensoxyleras aromaterna.