Polyomaviridae
|
|
| Polyomaviridae | |
|---|---|
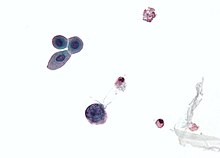
| Mikrofotografi som visar en polyomavirusinfekterad cell – stor (blå) cell under mitten-vänster. Urincytologiskt prov. | |
| Virusklassificering | |
| (orankad): | Virus |
| Rike : | Monodnaviria |
| Rike: | Shotokuvirae |
| Provins: | Cossaviricota |
| Klass: | Papovaviricetes |
| Beställa: | Sepolyvirales |
| Familj: | Polyomaviridae |
| Genera | |
|
|
Polyomaviridae är en familj av virus vars naturliga värdar främst är däggdjur och fåglar. Från och med 2020 finns det sex erkända släkten och 117 arter, varav fem är otilldelade till ett släkte. 14 arter är kända för att infektera människor, medan andra, såsom Simian Virus 40 , har identifierats hos människor i mindre utsträckning. De flesta av dessa virus är mycket vanliga och vanligtvis asymtomatiska i de flesta studerade mänskliga populationer. BK-virus är associerat med nefropati hos njurtransplanterade och icke-njurtransplanterade patienter med solida organ, JC-virus med progressiv multifokal leukoencefalopati och Merkelcellsvirus med Merkelcellscancer .
Struktur och genom

Polyomavirus är icke-höljeförsedda dubbelsträngade DNA- virus med cirkulära genom på cirka 5000 baspar . Genomet är förpackat i en viral kapsid på cirka 40-50 nanometer i diameter, som är icosaedrisk till formen (T=7 symmetri). Kapsiden är sammansatt av 72 pentameriska kapsomerer av ett protein som kallas VP1 , som är kapabelt att självmontera till en sluten ikosaeder; varje pentamer av VP1 är associerad med en molekyl av ett av de andra två kapsidproteinerna, VP2 eller VP3 .

Genomet av ett typiskt polyomavirus kodar för mellan 5 och 9 proteiner , uppdelat i två transkriptionsregioner som kallas de tidiga och sena regionerna på grund av tiden under infektionen då de transkriberas. Varje region transkriberas av värdcellens RNA-polymeras II som ett enda pre-budbärar-RNA som innehåller flera gener. Den tidiga regionen kodar vanligtvis för två proteiner, de små och stora tumörantigenerna, producerade genom alternativ splitsning . Den sena regionen innehåller de tre strukturella kapsidproteinerna VP1, VP2 och VP3, producerade av alternativa translationella startställen. Ytterligare gener och andra variationer på detta tema finns i vissa virus: till exempel har gnagarpolyomavirus ett tredje protein som kallas mellantumörantigen i den tidiga regionen, vilket är extremt effektivt för att inducera cellulär transformation ; SV40 har ett ytterligare kapsidprotein VP4; några exempel har ett ytterligare regulatoriskt protein som kallas agnoprotein uttryckt från den sena regionen. Genomet innehåller också en icke-kodande kontroll- eller regulatorisk region som innehåller de tidiga och sena regionernas promotorer , transkriptionsstartställen och replikationsursprunget .
Replikering och livscykel
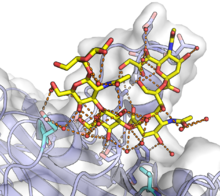
Polyomvirusets livscykel börjar med inträde i en värdcell . Cellulära receptorer för polyomavirus är sialinsyrarester av glykaner , vanligtvis gangliosider . Bindningen av polyomavirus till värdceller medieras av bindningen av VP1 till sialylerade glykaner på cellytan. I vissa speciella virus inträffar ytterligare cell-yta-interaktioner; till exempel JC-viruset kräva interaktion med 5HT2A-receptorn och Merkelcellviruset med heparansulfat . Men i allmänhet medieras virus-cell-interaktioner av vanligt förekommande molekyler på cellytan, och är därför sannolikt inte en stor bidragande orsak till enskilda viruss observerade celltypstropism . Efter bindning till molekyler på cellytan, endocytoseras virionet och går in i det endoplasmatiska retikulum - ett beteende som är unikt bland kända icke-hölje-virus - där den virala kapsidstrukturen sannolikt kommer att störas av verkan av värdcellens disulfid -isomerasenzymer.
Detaljerna för transitering till kärnan är inte tydliga och kan variera mellan individuella polyomvirus. Det har ofta rapporterats att en intakt, om än förvrängd, virionpartikel frisätts från det endoplasmatiska retikulumet in i cellcytoplasman, där genomet frisätts från kapsiden, möjligen på grund av den låga kalciumkoncentrationen i cytoplasman . Både uttryck av virala gener och replikering av det virala genomet sker i kärnan med hjälp av värdcellsmaskineri. De tidiga generna - som minst innefattar det lilla tumörantigenet (ST) och det stora tumörantigenet (LT) - uttrycks först, från en enda alternativt splitsad budbärar-RNA- sträng. Dessa proteiner tjänar till att manipulera värdens cellcykel - dysregulerar övergången från G1-fas till S-fas , när värdcellens genom replikeras - eftersom värdcells-DNA-replikationsmaskineri behövs för replikering av viral genom. Den exakta mekanismen för denna dysreglering beror på viruset; till exempel SV40 LT direkt binda värdcell p53 , men murint polyomavirus LT gör det inte. LT inducerar DNA-replikation från det virala genomets icke-kodande kontrollregion (NCCR), varefter uttrycket av det tidiga mRNA:t reduceras och uttrycket av det sena mRNA:t, som kodar för de virala kapsidproteinerna, börjar. När dessa interaktioner börjar uppvisar LT som tillhör flera polyomavirus, inklusive Merkel cell polyomavirus , onkogen potential. Flera mekanismer har beskrivits för att reglera övergången från tidigt till sent genuttryck, inklusive involveringen av LT-proteinet i att undertrycka den tidiga promotorn, uttrycket av oavslutade sena mRNA med förlängningar som är komplementära till tidigt mRNA och uttrycket av regulatoriskt mikroRNA . Uttryck av de sena generna resulterar i ackumulering av de virala kapsidproteinerna i värdcellens cytoplasma. Kapsidkomponenter kommer in i kärnan för att kapsla in nytt viralt genomiskt DNA. Nya virioner kan sättas ihop i virala fabriker . Mekanismen för virusfrisättning från värdcellen varierar mellan polyomavirus; vissa uttrycker proteiner som underlättar cellexit, såsom agnoproteinet eller VP4 . I vissa fall resulterar höga nivåer av inkapslat virus i cellys, vilket frisätter virionerna.
Virala proteiner
Tumörantigener
Det stora tumörantigenet spelar en nyckelroll för att reglera den virala livscykeln genom att binda till det virala ursprunget för DNA-replikation där det främjar DNA-syntes. Eftersom polyomviruset förlitar sig på värdcellsmaskineriet för att replikera måste värdcellen vara i s-fas för att detta ska börja. På grund av detta modulerar stora T-antigen också cellulära signalvägar för att stimulera progression av cellcykeln genom att binda till ett antal cellulära kontrollproteiner. Detta uppnås genom en tvåbensattack av att hämma tumörhämmande gener p53 och medlemmar av retinoblastomfamiljen ( pRB ) och stimulera celltillväxtvägar genom att binda cellulärt DNA, ATPas-helikas, DNA-polymeras a-association och bindning av transkriptionspreinitieringskomplexfaktorer . Denna onormala stimulering av cellcykeln är en kraftfull kraft för onkogen transformation. [ citat behövs ]
Det lilla tumörantigenproteinet kan också aktivera flera cellulära vägar som stimulerar cellproliferation. Polyomavirus små T-antigener riktar sig vanligen mot proteinfosfatas 2A ( PP2A ), en viktig multisubenhetsregulator för flera vägar inklusive Akt , den mitogenaktiverade proteinkinasvägen (MAPK) och den stressaktiverade proteinkinasvägen (SAPK). Merkel cell polyomavirus small T-antigen kodar för en unik domän, kallad LT-stabiliseringsdomänen (LSD), som binder till och hämmar FBXW7 E3 -ligas som reglerar både cellulära och virala onkoproteiner. Till skillnad från SV40, transformerar MCV-litet T-antigen direkt gnagarceller in vitro.
Det mellersta tumörantigenet används i modellorganismer som utvecklats för att studera cancer, såsom MMTV-PyMT- systemet där mitten T är kopplat till MMTV- promotorn . Där fungerar den som en onkogen , medan vävnaden där tumören utvecklas bestäms av MMTV-promotorn. [ citat behövs ]
Kapsidproteiner
Polyomaviruskapsiden består av en huvudkomponent, huvudkapsidprotein VP1 och en eller två mindre komponenter, mindre kapsidproteiner VP2 och VP3 . VP1- pentamerer bildar den slutna icosaedriska virala kapsiden , och i det inre av kapsiden är varje pentamer associerad med en molekyl av antingen VP2 eller VP3. Vissa polyomavirus, såsom Merkel cell polyomavirus , kodar inte för eller uttrycker inte VP3. Kapsidproteinerna uttrycks från den sena regionen av genomet.
Agnoprotein
Agnoproteinet är ett litet multifunktionellt fosfoprotein som finns i den sena kodande delen av genomet hos vissa polyomavirus, framför allt BK -virus , JC-virus och SV40 . Det är väsentligt för spridning av de virus som uttrycker det och tros vara involverat i att reglera den virala livscykeln, särskilt replikation och viral utträde från värdcellen, men de exakta mekanismerna är oklara.
Taxonomi
Polyomavirusen är medlemmar av grupp I (dsDNA-virus). Klassificeringen av polyomavirus har varit föremål för flera föreslagna revisioner när nya medlemmar i gruppen upptäcks. klassificerades polyomavirus och papillomvirus , som delar många strukturella egenskaper men har mycket olika genomiska organisationer, tillsammans i den nu föråldrade familjen Papovaviridae . (Namnet Papovaviridae kommer från tre förkortningar: Pa för Papillomavirus , Po för Polyomavirus och Va för "vacuolating.") Polyomavirusen delades in i tre huvudklader ( det vill säga genetiskt relaterade grupper): SV40-kladen, fågelkladen och den murina polyomaviruskladden. En efterföljande föreslagen omklassificering av International Committee on Taxonomy of Viruses (ICTV) rekommenderade att dela upp familjen Polyomaviridae i tre släkten:
- Släktet Ortopolyomavirus (typ art SV40 )
- Genus Wukipolyomavirus (typ art KI polyomavirus )
- Släktet Avipolyomavirus (typ art aviärt polyomavirus)
Det nuvarande ICTV-klassificeringssystemet känner igen sex släkten och 117 arter, varav fem inte kunde tilldelas ett släkte. Detta system behåller skillnaden mellan fågel- och däggdjursvirus, och grupperar fågelundergruppen i släktet Gammapolyomavirus . De sex släktena är:
- Alfapolyomvirus
- Betapolyomvirus
- Deltapolyomvirus
- Epsilonpolyomvirus
- Gammapolyomvirus
- Zetapolyomvirus
Följande arter har inte tilldelats ett släkte:
- Centroristis striata polyomavirus 1
- Rhynchobatus djiddensis polyomavirus 1
- Sparus aurata polyomavirus 1
- Trematomus bernacchii polyomavirus 1
- Trematomus pennellii polyomavirus 1
Beskrivning av ytterligare virus pågår. Dessa inkluderar havsuttern polyomavirus 1 och Alpaca polyomavirus Ett annat virus är jättepanda polyomavirus 1. Ett annat virus har beskrivits från sigmodontina gnagare. En annan - näbbmössa polyomavirus 1 - har beskrivits i näbben.
Humana polyomvirus
De flesta polyomavirus infekterar inte människor. Av de polyomvirus som katalogiserades från och med 2017 var totalt 14 kända med mänskliga värdar. Vissa polyomavirus är emellertid associerade med mänskliga sjukdomar, särskilt hos immunförsvagade individer. MCV är mycket avvikande från andra humana polyomavirus och är närmast besläktat med murint polyomavirus. Trichodysplasia spinulosa-associerat polyomavirus (TSV) är avlägset besläktat med MCV. Två virus – HPyV6 och HPyV7 – är närmast besläktade med KI- och WU-virus, medan HPyV9 är närmast besläktat med det afrikanska gröna apans lymfotropiska polyomvirus (LPV). [ citat behövs ]
Ett fjortonde virus har beskrivits. Lyon IARC polyomavirus är besläktat med tvättbjörnspolyomavirus. [ citat behövs ]
Lista över humana polyomavirus
Följande 14 polyomvirus med mänskliga värdar hade identifierats och fått sina genom sekvenserade från och med 2017:
| Arter | Föreslaget släkte | Virusnamn | Förkortning | NCBI RefSeq | År av upptäckt | Klinisk korrelation (om någon) | Referenser |
|---|---|---|---|---|---|---|---|
| Humant polyomvirus 5 | Alfa | Merkel cell polyomavirus | MCPyV | NC_010277 | 2008 | Merkel cell cancer | |
| Humant polyomvirus 8 | Alfa | Trichodysplasia spinulosa polyomavirus | TSPyV | NC_014361 | 2010 | Trichodysplasia spinulosa | |
| Humant polyomvirus 9 | Alfa | Humant polyomvirus 9 | HPyV9 | NC_015150 | 2011 | Ingen känd | |
| Humant polyomvirus 12 | Alfa | Humant polyomvirus 12 | HPyV12 | NC_020890 | 2013 | Ingen känd | |
| Humant polyomvirus 13 | Alfa | New Jersey polyomavirus | NJPyV | NC_024118 | 2014 | Ingen känd | |
| Humant polyomvirus 1 | Beta | BK polyomvirus | BKPyV | NC_001538 | 1971 | Polyomavirus-associerad nefropati ; hemorragisk cystit | |
| Humant polyomvirus 2 | Beta | JC polyomavirus | JCPyV | NC_001699 | 1971 | Progressiv multifokal leukoencefalopati | |
| Humant polyomvirus 3 | Beta | KI polyomvirus | KIPyV | NC_009238 | 2007 | Ingen känd | |
| Humant polyomvirus 4 | Beta | WU polyomavirus | WUPyV | NC_009539 | 2007 | Ingen känd | |
| Humant polyomvirus 6 | Delta | Humant polyomvirus 6 | HPyV6 | NC_014406 | 2010 | HPyV6-associerad pruritisk och dyskeratotisk dermatos (H6PD) | |
| Humant polyomvirus 7 | Delta | Humant polyomvirus 7 | HPyV7 | NC_014407 | 2010 | HPyV7-relaterad epitelial hyperplasi | |
| Humant polyomvirus 10 | Delta | MW polyomavirus | MWPyV | NC_018102 | 2012 | Ingen känd | |
| Humant polyomvirus 11 | Delta | STL polyomavirus | STLPyV | NC_020106 | 2013 | Ingen känd | |
| Humant polyomvirus 14 | Alfa | Lyon IARC polyomavirus | LIPyV | NC_034253.1 | 2017 | Ingen känd |
Deltapolyomavirus innehåller endast de fyra humana virus som visas i tabellen ovan. Alfa- och betagrupperna innehåller virus som infekterar en mängd olika däggdjur. Gammagruppen innehåller fågelvirus. Kliniskt signifikanta sjukdomsassociationer visas endast där kausalitet förväntas.
Antikroppar mot apans lymfotropiska polyomvirus har upptäckts hos människor, vilket tyder på att detta virus - eller ett närbesläktat virus - kan infektera människor.
Klinisk relevans
Alla polyomavirus är mycket vanliga barndoms- och unga vuxna infektioner. De flesta av dessa infektioner verkar orsaka få eller inga symtom. Dessa virus är troligen livslång ihållande bland nästan alla vuxna. Sjukdomar orsakade av humana polyomavirusinfektioner är vanligast bland personer med nedsatt immunförsvar ; sjukdomsassociationer inkluderar BK-virus med nefropati hos njurtransplanterade och icke-njurtransplanterade patienter med solida organ, JC-virus med progressiv multifokal leukoencefalopati och Merkelcellsvirus (MCV) med Merkelcellscancer .
SV40
SV40 replikerar i njurarna på apor utan att orsaka sjukdom, men kan orsaka cancer hos gnagare under laboratorieförhållanden. Under 1950-talet och början av 1960-talet kan över 100 miljoner människor ha exponerats för SV40 på grund av tidigare oupptäckt SV40-kontamination av poliovaccin , vilket väckte oro över möjligheten att viruset kan orsaka sjukdom hos människor. Även om det har rapporterats förekomma i vissa humana cancerformer, inklusive hjärntumörer , bentumörer , mesoteliom och non-Hodgkins lymfom , förväxlas noggrann detektion ofta av höga nivåer av korsreaktivitet för SV40 med utbredda humana polyomavirus. De flesta virologer avfärdar SV40 som en orsak till cancer hos människor.
Diagnos
Diagnosen polyomavirus uppstår nästan alltid efter den primära infektionen eftersom den är antingen asymtomatisk eller subklinisk. Antikroppsanalyser används vanligtvis för att detektera närvaron av antikroppar mot individuella virus. Konkurrensanalyser behövs ofta för att särskilja mycket liknande polyomavirus.
I fall av progressiv multifokal leukoencefalopati (PML) används en korsreaktiv antikropp mot SV40 T-antigen (vanligen Pab419) för att färga vävnader direkt för närvaron av JC-virus T-antigen. PCR kan användas på en biopsi av vävnaden eller cerebrospinalvätskan för att amplifiera polyomavirus-DNA. Detta möjliggör inte bara upptäckt av polyomavirus utan också vilken undertyp det är.
Det finns tre huvudsakliga diagnostiska tekniker som används för diagnos av reaktivering av polyomavirus vid polyomavirusnefropati (PVN): urincytologi, kvantifiering av virusmängden i både urin och blod och en njurbiopsi . Reaktiveringen av polyomavirus i njurarna och urinvägarna orsakar utsöndring av infekterade celler, virioner och/eller virala proteiner i urinen. Detta gör det möjligt för urincytologi att undersöka dessa celler, som om det finns polyomavirus-inklusion av kärnan, är en diagnostisk infektion. Eftersom urinen från en infekterad individ kommer att innehålla virioner och/eller viralt DNA, kan kvantifiering av virusmängden göras genom PCR. Detta gäller även för blodet.
Njurbiopsi kan också användas om de två nyss beskrivna metoderna inte är avgörande eller om den specifika virusbelastningen för njurvävnaden önskas. På samma sätt som urincytologin undersöks njurcellerna under ljusmikroskopi för polyomavirus-inklusion av kärnan, såväl som cellys och virala partialer i den extracellulära vätskan. Den virala mängden som tidigare mäts också med PCR. [ citat behövs ]
Vävnadsfärgning med användning av en monoklonal antikropp mot MCV T-antigen visar användbarhet för att differentiera Merkelcellkarcinom från andra små, runda celltumörer. Blodprover för att upptäcka MCV-antikroppar har utvecklats och visar att infektion med viruset är utbredd även om Merkelcellscancerpatienter har exceptionellt högre antikroppssvar än asymtomatiskt infekterade personer.
Används för att spåra mänsklig migration
JC-viruset erbjuder en lovande genetisk markör för mänsklig evolution och migration. Den bärs av 70–90 procent av människorna och överförs vanligtvis från föräldrar till avkomma. Denna metod verkar inte vara tillförlitlig för att spåra moderna människors nya afrikanska ursprung . [ citat behövs ]
Historia
Murint polyomavirus var det första polyomaviruset som upptäcktes, efter att ha rapporterats av Ludwik Gross 1953 som ett extrakt av musleukemier med förmåga att inducera parotiskörteltumörer . Det orsakande medlet identifierades som ett virus av Sarah Stewart och Bernice Eddy , efter vilka det en gång kallades "SE-polyom". Termen "polyom" hänvisar till virusens förmåga att producera multipla (poly-) tumörer (-oma) under vissa förhållanden. Namnet har kritiserats som en "köttfri språklig smörgås" ("köttfri" eftersom båda morfem i "polyom" är affix) som ger liten inblick i virusens biologi; i själva verket har efterföljande forskning funnit att de flesta polyomavirus sällan orsakar kliniskt signifikant sjukdom i sina värdorganismer under naturliga förhållanden.
Dussintals polyomavirus har identifierats och sekvenserats från och med 2017, som infekterar främst fåglar och däggdjur. Två polyomavirus är kända för att infektera fisk, svart havsabborre och guldgult . Totalt fjorton polyomavirus är kända för att infektera människor.