Nepafenac
 | |
| Kliniska data | |
|---|---|
| Handelsnamn | Nevanac, Ilevro, Amnac, andra |
| AHFS / Drugs.com | Monografi |
| MedlinePlus | a606007 |
| Licensdata | |
Graviditetskategori _ |
|
Administreringsvägar _ |
Aktuella ögondroppar |
| ATC-kod | |
| Rättslig status | |
| Rättslig status |
|
| Identifierare | |
| |
| CAS-nummer | |
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| CompTox Dashboard ( EPA ) | |
| ECHA InfoCard | 100.207.414 |
| Kemiska och fysikaliska data | |
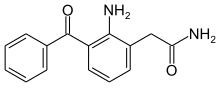
| Formel | C15H14N2O2 _ _ _ _ _ _ _ |
| Molar massa | 254,289 g-mol -1 |
| 3D-modell ( JSmol ) | |
| |
| |
|
| |
Nepafenac , som bland annat säljs under varumärket Nevanac , är ett icke-steroidt antiinflammatoriskt läkemedel (NSAID), vanligtvis säljs som en receptbelagd ögondroppe 0,1 % lösning (Nevanac) eller 0,3 % lösning (Ilevro). Det används för att behandla smärta och inflammation i samband med kataraktkirurgi . Nepafenak är en prodrug av amfenak , en hämmare av COX-1- och COX-2- aktivitet.
Medicinsk användning
Nepafenak är indicerat för behandling av smärta och inflammation efter kataraktkirurgi.
I Europeiska unionen är nepafenak också indicerat för att minska risken för postoperativt makulaödem i samband med kataraktkirurgi hos personer med diabetes.
Farmakologi
Handlingsmekanism
Nepafenak är ett NSAID, som tros vara en prodrug av amfenak efter omvandling av okulära vävnadshydrolaser efter penetrering via hornhinnan . Amfenak, liksom andra NSAID, tros hämma cyklooxygenasverkan .
Biverkningar
Biverkningar inkluderar huvudvärk; rinnande näsa; smärta eller tryck i ansiktet; illamående; kräkningar; och torra, kliande, klibbiga ögon. Allvarliga biverkningar inkluderar röda eller blodiga ögon; främmande kroppskänsla i ögat; känslighet för ljus; minskad synskärpa ; se fläckar eller fläckar; tårfyllda ögon; eller ögonutsläpp eller skorpbildning.
Reglerande
Nevanac
Den 25 februari 2005 lämnade Alcon in en ny läkemedelsansökan (NDA) till US Food and Drug Administration (FDA) för Nevanac 0,1 %. Resultat från de två studier som refereras till i NDA (Fas 2/3-studie C-02-53; Fas 3-studie C-03-32) har inte publicerats. Studie C-02-53 bestod av 228 patienter på 10 centra i USA. Studie C-03-32 bestod av 522 patienter på 22 centra i USA. Effektresultaten som presenterades bekräftades i en studie publicerad 2007.
Nevanac godkändes av FDA den 19 augusti 2005, med ansökningsnummer 021–862.
Ilevro
En NDA för Ilevro lämnades in den 15 december 2011. I en enmånadsstudie uppstod inga nya toxiciteter i den nya formuleringen av nepafenak. Information om säkerhet och effekt härleddes från den tidigare Nevanac-applikationen. I juni 2010 påbörjades en bekräftande studie (Studie C09055) som bestod av över 2000 patienter från 49 amerikanska platser och 37 europeiska platser. En andra fas 3-studie (Studie C11003) genomfördes på en population av 1 342 patienter på 37 ställen i USA som inte visade överlägsenhet gentemot Nevanac i en ändrad doseringsregim.
Ilevro godkändes av FDA den 16 oktober 2012, med ansökningsnummer 203–491.
Kommersialisering
Både Nevanac och Ilevro tillverkas och säljs av Alcon , Inc. Alcon är för närvarande en division av Novartis International AG, som huvudsakligen är baserat i Schweiz. Alcon, Inc. har också platser i både Schweiz och USA. Företaget har gått igenom flera namnbyten, från Alcon Laboratories, Inc. till Alcon Universal, Ltd., till Alcon, Inc.
Nevanac kom in på marknaden 2005 som en produkt från Alcon, då ett dotterbolag till Nestlé. Den 6 april 2008 gick Novartis med på att köpa cirka 74 miljoner aktier i Alcon från Nestlé för 143,18 USD per aktie. Den 4 januari 2010 gick Novartis med på att köpa alla återstående aktier i Alcon från Nestlé, totalt 156 miljoner aktier eller 77 % av aktierna i företaget. Vid tidpunkten för köpet lämnades ett förslag till fusion enligt schweizisk fusionslag till Alcons styrelse. Sammanslagningen kom överens om den 15 december 2010, vilket gör Alcon till "den näst största divisionen inom Novartis." Sammanslagningen slutfördes den 8 april 2011.
Ilevro lanserades av Alcon den 21 januari 2013. Under 2014 och 2015 växte Alcons nettoomsättning, vilket delvis bidrog till den ökade försäljningsvolymen för Ilevro. Det räkenskapsåret rapporterade Novartis 18 miljarder dollar i total finansiell skuld. Den siffran har växt stadigt sedan dess. Under 2016 rapporterade Novartis en total skuld på 23,8 miljarder dollar, upp från de 21,9 miljarder dollar som rapporterades 2015 och de 20,4 miljarder dollar som rapporterades 2014. Från och med maj 2017 beräknas Novartis vara värd 193,2 miljarder dollar.
Den 27 januari 2016 flyttades Alcon till att bli en filial av Innovative Medicines Division på Novartis. Tidigt under 2016 slöt Alcon avtal med både TrueVision och PowerVision och förvärvade Transcend Medical. Från och med januari 2017 väger Novartis alternativ för Alcon i affärsstrukturen.
Kommersiella risker
Alcon mötte av avtagande tillväxt under 2016, efter att ha ställts inför utmaningar inom utveckling och marknadsföring av nya produkter.
Marknadsföring
Novartis har en detaljenhet inriktad på hälso- och sjukvårdspersonal som består av över 3 000 anställda i USA och ytterligare 21 000 över hela världen. Novartis strävar också efter att expandera direkt-till-konsumentannonsering och inträde på marknader för specialprodukter. Novartis noterar också inflytandet av position och preferenser på amerikanska Centers for Medicare & Medicaid formularier när det gäller att utöka deras marknadsvärde.
Nepafenac, Nevanac och Ilevro saknas alla i årsredovisningen för 2016 från Novartis.
Immateriella rättigheter
Det finns för närvarande [ när? ] sju inlämnade amerikanska patent som är direkt associerade med de moderniserade formuleringarna av nepafenak, alla härrörande från Novartis. Det finns tre patent associerade med Nevanac som fortfarande är [ när? ] aktiv och fyra associerade med Ilevro. Det tidigaste patentet relaterade till de moderna formuleringarna av nepafenak godkändes den 11 juni 2002, efter att ha lämnats in 1999, av Bahram Asgharian. Ett patent lämnades in av Warren Wong, associerad med Alcon, Inc. baserat i Fort Worth, Texas , den 2 december 2005, för vattenhaltiga suspensioner av nepafenak. Ett annat patent för ett nepafenakbaserat läkemedel lämnades in den 8 maj 2006 av Geoffrey Owen, Amy Brooks och Gustav Graff. Ett patent lämnades in av Masood A. Chowhan och Huagang Chen den 9 februari 2007 och godkändes den 24 maj 2011, tätt följt av ett patent inlämnat av Warren Wong den 23 september 2010 och godkänt den 6 december 2011. Masood A. Chowhan, Malay Ghosh, Bahram Asgharian och Wesley Wehsin Han lämnade in ytterligare ett patent den 1 december 2010 och godkändes den 30 december 2014. Den senaste [ när ? ] patentet lämnades in av Masood A. Chowhan, Malay Ghosh, Bahram Asgharian och Wesley Weshin Han den 12 november 2014 och godkändes den 30 maj 2017. Dessa patent gäller till datum som sträcker sig mellan 17 juli 2018 och mars 31, 2032.
Novartis har även patent på nepafenak i 26 länder utanför USA.
externa länkar
- "Nepafenac" . Läkemedelsinformationsportal . US National Library of Medicine.