Kynurenin 3-monooxygenas
| kynurenine 3-monooxygenas | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 Struktur av kynurenine 3-monooxygenas dimer, genererad från 4J34. En monomer visas i tecknat format (cyan) och den andra monomeren visas i bandformat (grönt). De flexibla länkområdena (resterna 96-104) är färgade röda. Flavinadenindinukleotid (FAD) visas som sfärer färgkodade enligt atomtyp.
| |||||||||
| Identifierare | |||||||||
| EG nr. | 1.14.13.9 | ||||||||
| CAS-nr. | 9029-61-2 | ||||||||
| Databaser | |||||||||
| IntEnz | IntEnz-vy | ||||||||
| BRENDA | BRENDA inträde | ||||||||
| ExPASy | NiceZyme-vy | ||||||||
| KEGG | KEGG inträde | ||||||||
| MetaCyc | Metabolisk väg | ||||||||
| PRIAM | profil | ||||||||
| PDB- strukturer | RCSB PDB PDBe PDB summa | ||||||||
| Genontologi | AmiGO / QuickGO | ||||||||
| |||||||||
Inom enzymologi är ett kynurenin 3-monooxygenas ( EC 1.14.13.9 ) ett enzym som katalyserar den kemiska reaktionen
- L -kynurenin + NADPH + H + + O 2 ⇌ 3-hydroxi - L -kynurenin + NADP + + H 2 O
Kynurenin 3-monooxygenas är uttrycksprodukten av KMO (genen) . Det systematiska namnet på denna enzymklass är L -kynurenin, NADPH:oxygenoxidoreduktas (3-hydroxylerande) . Andra namn i vanlig användning inkluderar kynurenin-3-hydroxylas , kynurenin-hydroxylas och L -kynurenin-3-hydroxylas . Det deltar i tryptofanmetabolismen genom den kataboliska vägen kynurenin . Detta enzym tillhör familjen oxidoreduktaser , närmare bestämt, de som verkar på parade donatorer, med O 2 som oxidant. Kynurenin 3-monooxygenas katalyserar införandet av molekylärt syre i den aromatiska ringen av kynurenin för att producera 3-hydroxi- L -kynurenin. Den använder en kofaktor , FAD . Kynurenin 3-monooxygenas fungerar som en viktig grenpunkt i kynureninvägen och är som ett resultat ett attraktivt läkemedelsmål för immunologiska , neurodegenerativa och neuroinflammatoriska sjukdomar . För närvarande har den mesta forskningen om kynurenin 3-monooxygenasenzymet fokuserats främst på råttmodeller och på jäst , som båda har visat sig ha hög sekvenshomologi med det humana kynurenin 3-monooxygenasproteinet. Studier har visat de fördelaktiga effekterna av enzymhämning i dessa eukaryota kynurenin 3-monooxygenas aktiva platser, vilket gör detta enzym till ett attraktivt mål för human läkemedelsdesign.
Strukturera
Kynurenine 3-monooxygenas är en dimer som innehåller asymmetriska subenheter och har en FAD-bindande domän som sin protesgrupp. Kynurenin 3-monooxygenas innehåller en länkregion involverad i substratbindning efter en andra sträng av ett antiparallellt β-ark , en sexsträngad antiparallell β-sheetdomän och en α-helix vid karboxiterminalen. Den hydrofoba C-terminalen fungerar som den mitokondriella förankringsdomänen och deltar i enzymatisk aktivitet.
Aktiv sida
Även om ingen vetenskaplig litteratur rapporterar en kristallbild av ett kynurenin-3-monooxygenaskomplex med L -kynurenin, visar strukturella studier av enzymet i jäst samkristalliserad med UPF 648 hur FAD-kofaktorn och substratet är bundna i det aktiva stället. Kemiska likheter mellan UPF 648 och L -kynurenin tyder på att substratet binder intill flavoproteinets Re -face . En slinga som innehåller resterna Pro 321 – Gln 325 tros vara det syrebindande stället ovanför återsidan av FAD-protesgruppen.
Varje monomer innehåller en konserverad hydrofob ficka (rester Leu 221 , Met 230 , Ile 232 , Leu 234 , Phe 246 , Pro 321 , Phe 322 ) placerad runt substratets aromatiska bensendel. En konserverad Gln 325 polär rest är också involverad i vätebindning på L -kynureninkarbonylgruppen, såväl som på vätet på FAD N3-atomen. Arg 83 och Tyr 97 bildar också polära kontakter med karboxylatet i aminosyradelen på substratet.
Mekanism
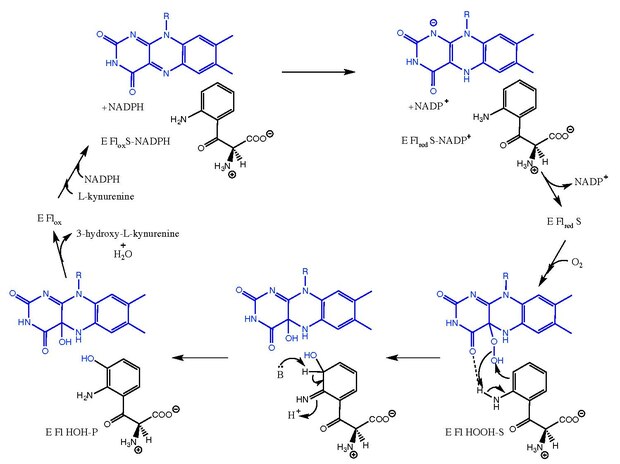
Kynurenin-3-monooxygenas katalyserar hydroxyleringen av L - kynurenin till 3-hydroxi- L -kynurenin med åtföljande omvandling av NADPH till NADP + . Reaktionsmekanismen är inte helt känd, men tros följa mekanismer relaterade till de flavinberoende monooxygenaserna . Efter att L -kynurenin binder, minskar NADPH FAD och lämnar som NADP + . Syre binder sedan och skapar en L -kynurenin-FAD-hydroperoxid-mellanprodukt. Denna mellanprodukt är den elektrofila källan för hydroxyleringsreaktionen, vilket ger en primär ketiminform av produkten och C4a-hydroxi-FAD. Tautomerisering ger 3-hydroxi- L -kynurenin i komplex med enzymet (EFl HOH-P). Dissociation av 3-hydroxi L -kynurenin och H 2 O leder till det fria enzymet (E Fl ox ).
Biologisk funktion
Kynurenin 3-monooxygenas katalyserar omvandlingen av L -kynurenin till 3-hydroxi- L -kynurenin, en viktig bioaktiv metabolit i kynureninvägen . Kyureninvägen är ansvarig för över 95 % av tryptofan oxidativ nedbrytning. L -Kynurenin är en viktig förgreningspunkt för denna metaboliska väg, som omvandlas till neurotoxinet 3-hydroxi - L -kynurenin via kynurenin-3-monooxygenas, den neuroprotektanta kynureninsyran genom kynureninaminotransferaser, eller antranilsyra genom kynureninas .
Kynurenine 3-monooxygenas reglerar nedströms produktionen av kinolinsyra , som kan generera reaktiva fria radikaler och aktiverar NMDA -subtypen av glutamatreceptorer, vilket producerar excitotoxiska lesioner i däggdjurens centrala nervsystem. Kinolinsyra är också bioprekursorn för NAD + .
Hämning av kynurenin 3-monooxygenas leder till en ökning av kynureninsyra i kynureninvägen. Denna metabolit fungerar som en antagonist av α7 nikotinacetylkolinreceptorn och som en antagonist vid glycinstället för NMDA-receptorn. Som ett resultat bestämmer reglering av kynurenin-3-monooxygenasenzymet den neurotoxiska och neuroprotektiva potentialen hos kynureninvägen.
Sjukdomsrelevans
Kynurenin 3-monooxygenas är ett attraktivt läkemedelsmål för flera neurodegenerativa och neuroinflammatoriska sjukdomar, särskilt Huntingtons , Alzheimers och Parkinsons sjukdom . Administrering av potenta enzyminhibitorer har visat lovande farmakologiska resultat. Specifikt har genetisk eliminering av kynurenin 3-monooxygenasenzymet visats undertrycka toxiciteten hos huntingtinproteinet i jäst- och Drosophila -modeller av Huntingtons sjukdom.
Kynurenin 3-monooxygenasbrist, som kan orsakas av genetiska polymorfismer , cytokiner eller båda, leder till en ackumulering av kynurenin och till en förskjutning inom tryptofanmetaboliska vägen mot kynureninsyra och antranilsyra . Ny forskning tyder på att hyperfysiologiska koncentrationer av kynurenin hos patienter med kynurenin 3-monooxygenasbrist resulterar i en förändring mot produktion av kynureninsyra, som tros vara relaterad till kognitiva brister i prediktiv strävan och visuospatialt arbetsminne . Kynurenin-3-monooxygenasbrist är associerad med störningar i hjärnan (t.ex. schizofreni , tic-störningar ) och i levern.
- Foucher AL, McIntosh A, Douce G, Wastling J, Tait A, Turner CM (2006). "En proteomisk analys av arsenikaldrogresistens i Trypanosoma brucei". Proteomik . 6 (9): 2726–2732. doi : 10.1002/pmic.200500419 . PMID 16526094 . S2CID 24074942 .
- Okamoto H, Hayaishi O (1967). "Flavinadenindinukleotidkrav för kynureninhydroxylas från råttlevermitokondrier". Biochem. Biophys. Res. Commun . 29 (3): 394–399. doi : 10.1016/0006-291X(67)90469-X . PMID 6076241 .
- Saito Y, Hayaishi O, Rothberg S (1957). "Studier om oxygenaser; enzymatisk bildning av 3-hydroxi- L -kynurenin från L -kynurenin" . J. Biol. Chem . 229 (2): 921–934. doi : 10.1016/S0021-9258(19)63696-3 . PMID 13502353 .