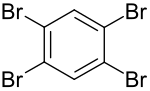
1,2,4,5-tetrabrombensen
|
|
| Namn | |
|---|---|
|
Föredraget IUPAC-namn
1,2,4,5-tetrabrombensen |
|
| Identifierare | |
|
3D-modell ( JSmol )
|
|
| ECHA InfoCard | 100.010.231 |
| EG-nummer |
|
|
PubChem CID
|
|
| UNII | |
|
CompTox Dashboard ( EPA )
|
|
|
|
|
|
| Egenskaper | |
| C6H2Br4 _ _ _ _ _ | |
| Utseende | vit fast substans |
| Densitet | 2,518 g/cm 3 |
| Smältpunkt | 180–182 °C (356–360 °F; 453–455 K) |
| Faror | |
| GHS- märkning : | |

|
|
| Varning | |
| H315 , H319 , H335 , H413 | |
| P261 , P264 , P271 , P273 , P280 , P302+P352 , P304+P340 , P305+P351+P338 , P312, P321 , P332 + P313 , P337 + P3 , P337+ P3 , P337 + P30 5 , P501 | |
|
Om inte annat anges ges data för material i standardtillstånd (vid 25 °C [77 °F], 100 kPa).
|
|
1,2,4,5 - tetrabrombensen är en organobrominförening med formeln C6H2Br4 . Det är en av tre isomerer av tetrabrombensen. Föreningen är en vit fast substans. 1,2,4,5-tetrabrombensen är en viktig metabolit av det flamskyddsmedel hexabrombensen .
Förberedelse
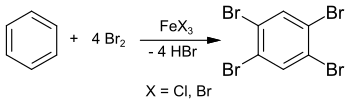
Syntesen av 1,2,4,5-tetrabrombensen har redan rapporterats 1865 från bensen och överskott av brom i ett förseglat rör vid 150 °C. Den klart reducerade smältpunkten på cirka 160 °C indikerar emellertid föroreningar i slutprodukten. från 1885 publicerade Adolf Scheufelen syntesen av ett renare prov med användning av järn(III)klorid FeCl3 som katalysator , isolerad som "snygga nålar" ("schönen Nadeln").
Syntesen kan också utföras i lösning i kloroform eller tetraklormetan och ger 1,2,4,5-tetrabrombensen i 89 % utbyte. Denna reaktion kan också utföras i ett laboratorieexperiment med överskott av brom och järnspik (som utgångsmaterial för järn(III)bromid FeBr3 ) . Mellansteget är 1,4-dibrombensen , som reagerar vidare med överskott av brom för att ge 1,2,4,5-tetrabrombensen.
Reaktioner
Byggsten för flytande kristaller och fluorescerande färgämnen
På grund av sin symmetriska struktur och reaktivitet är 1,2,4,5-tetrabrombensen en föregångare till nematiska flytande kristaller med korsade mesogener och för kolumnära (diskotiska) flytande kristaller med en omfattande plan, "brädliknande" tetrabensoantracenkärna.
I en enkärlsreaktion reagerar 1,2,4,5-tetrabrombensen med 4-hydroxibensaldehyd , alkyleringsmedlet 1-brompentan, Wittig-reagenset metyltrifenylfosfoniumjodid, basen kaliumkarbonat , fasöverföringskatalysatorn tetrabutylammoniumbromid- reagenset Heck-reagenset, palladium(II)acetat och Heck -samkatalysatorn 1,3-bis(difenylfosfino)propan (dppp) i dimetylacetamid vilket ger direkt en symmetrisk tetraalkoxylstilben som E-isomer i 17 % utbyte.
På grund av deras uttalade π-konjugering kan sådana föreningar potentiellt användas som optiska vitmedel , OLED-material eller flytande kristaller.
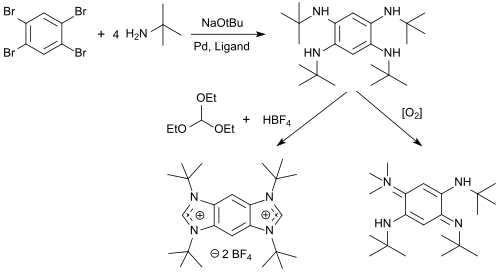
N -alkyl-tetraaminobensener är tillgängliga från 1,2,4,5-tetrabrombensen i höga utbyten, som kan cykliseras med trietylortoformiat och syror till bensobis(imidazolium)salter (BBI-salter) och oxideras med syre för att bilda 1,4- bensokinon-diiminer.
BBI-salter är mångsidiga fluorescerande färgämnen med emissionsvåglängder λ em mellan 329 och 561 nm, uttalad solvatokromism och starkt lösningsmedelsberoende Stokes shift , som kan användas som proteintagg för fluorescerande märkning av proteiner.
Utgångsmaterial för arynes
Från 1,2,4,5-tetrabrombensen kan en 1,4-monoarin framställas in situ med en ekvivalent n -butyllitium genom bromatraktion, som reagerar omedelbart med furan och bildar 6,7-dibromo-1,4 -epoxi-1,4-dihydronaftalen (6,7-dibromonaftalen-1,4-endoxid) i 70 % utbyte.
När 2,5-dialkylfuraner (t.ex. 2,5-(di-n-oktyl)furan) används bildas den dibromerade monoendoxiden i 64 % utbyte, av vilken dibrom-5,8-di-n-oktylnaftalen bildas med zinkpulver/ titantetraklorid i 88 % utbyte.
Vid behandling med titantetraklorid och zinkdamm deoxideras endoxiden och ger 2,3-dibromnaftalen.
Endoxiden reagerar med 3-sulfolen i en Diels-Alder-reaktion vid eliminering av svaveldioxid . Den resulterande tricykliska addukten omvandlas till 2,3-dibromantracen i gott utbyte.
Om dibromenoxiden tillåts reagera vidare med furan, i närvaro av n -butyllitium- eller kaliumamid eller via en intermediär 1,4-aryn den tricykliska 1,4-addukten 1,4:5,8-diepoxi-1,4, 5,8-tetrahydroantracen bildas i 71 % utbyte som en syn-anti-blandning . Med natriumamid i etylenglykoldimetyleter (DME) beter sig dock dibromenoxiden som en 1,3-arynekvivalent och bildar med furan en fenantrenliknande tricyklisk 1,3-addukt, som kan reagera med furan och natriumamid till ett trifenylenderivat (1,3,5-tris-aren).
[2+4] cykloadditioner med 1,2,4,5-tetrabrombensen fortgår ibland i mycket höga utbyten, såsom reaktionen av en dihalogen-substituerad 1,3-difenyl-isobensofuran till ett tetrahalogenerat antracenderivat (98 %), vilket omvandlas successivt ytterligare med 1,3-difenylisobensofuran i 65 % utbyte till ett pentacenderivat och furan till ett hexacenderivat (67 %).
Tvärbindningen av bensimidazolmodifierade polymerer ger material med hög absorptionsförmåga för koldioxid , vilket skulle kunna vara lämpligt för CO 2 -separation från gasblandningar.
Det är utgångsmaterialet för mono- och bisaryiner.
Säkerhet
1,2,4,5-Tetrabrombensen är en levertoxisk nedbrytningsprodukt av det flamskyddsmedel hexabrombensen och upptäcktes redan 1987 i Japan i modersmjölksprover.