Xenon oxytetrafluorid
|
|

|
|
| Identifierare | |
|---|---|
|
3D-modell ( JSmol )
|
|
| ChemSpider | |
|
|
|
|
| Egenskaper | |
| XeOF 4 | |
| Molar massa | 223,23 g/mol |
| Utseende | färglös vätska |
| Densitet | 3,17 g/cm3 , flytande |
| Smältpunkt | −46,2 °C (−51,2 °F; 227,0 K) |
| Reagerar med vatten | |
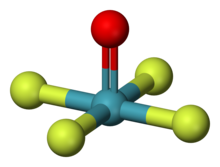
| Strukturera | |
| fyrkantig pyramidform | |
|
Om inte annat anges ges data för material i standardtillstånd (vid 25 °C [77 °F], 100 kPa).
|
|
Xenonoxytetrafluorid ( Xe O F4
) är en oorganisk kemisk förening . Det är en färglös stabil vätska med en smältpunkt på −46,2 °C (−51,2 °F; 227,0 K) som kan syntetiseras genom partiell hydrolys av XeF
6 , eller reaktion av XeF
6 med kiseldioxid eller NaNO
3 :
En högutbytesyntes fortsätter genom reaktionen av XeF
6 med POF
3 vid -196 ° C (-320,8 ° F; 77,1 K).
Liksom de flesta xenonoxider är det extremt reaktivt och instabilt och hydrolyseras i vatten för att ge farligt farliga och frätande produkter, inklusive vätefluorid :
Dessutom bildas en del ozon och fluor.
Reaktioner
XeOF
4 reagerar med H
2 O i följande steg:
Den bildade XeO
3 är ett farligt sprängämne som sönderfaller explosivt till Xe och O
2 :
-
2 XeO3
+ O2
→ 2 Xe 3
I sin flytande form uppvisar XeOF
4 amfotärt beteende och bildar komplex med både starka Lewis-baser som CsF och starka Lewis-syror som SbF
5 . Den bildar en 1:1-addukt med XeF
2 , isostrukturell med XeF
2 · IF
5 , såväl som olika tunga alkalimetallfluorider.
Reaktionen XeO2F2
av en
bekväm XeOF4
för med XeO3
. ger syntesväg
externa länkar
- Xenon-tetrafluoridoxid i Linström, Peter J.; Mallard, William G. (red.); NIST Chemistry WebBook , NIST Standard Reference Database Number 69 , National Institute of Standards and Technology, Gaithersburg (MD) (hämtad 2022-04-13)