Väteperoxid - urea
|
|
|||

|
|||
| Namn | |||
|---|---|---|---|
| Andra namn Ureaperoxid, perkarbamid, UHP
|
|||
| Identifierare | |||
|
3D-modell ( JSmol )
|
|||
| ChEBI | |||
| ChemSpider | |||
| ECHA InfoCard | 100.004.275 | ||
|
PubChem CID
|
|||
| UNII | |||
|
CompTox Dashboard ( EPA )
|
|||
|
|||
|
|||
| Egenskaper | |||
| CH 6 N 2 O 3 _ | |||
| Molar massa | 94,070 g·mol -1 | ||
| Utseende | Vitt fast material | ||
| Densitet | 1,50 g/cm 3 | ||
| Smältpunkt | 75 till 91,5 °C (167,0 till 196,7 °F; 348,1 till 364,6 K) (sönderdelas) | ||
| Farmakologi | |||
| D02AE01 ( WHO ) | |||
| Faror | |||
| GHS- märkning : | |||
 
|
|||
| Fara | |||
| H272 , H315 , H318 | |||
| P210 , P220 , P264 , P280 , P302+P352 , P305+P351+P338 | |||
| Flampunkt | 60 °C (140 °F; 333 K) | ||
| Säkerhetsdatablad (SDS) | Externt MSDS | ||
|
Om inte annat anges ges data för material i standardtillstånd (vid 25 °C [77 °F], 100 kPa).
|
|||
Väteperoxid-urea (även kallad Hyperol , artizon , urea väteperoxid och UHP ) är ett fast ämne som består av lika mängder väteperoxid och urea . Denna förening är ett vitt kristallint fast ämne som löses i vatten för att ge fri väteperoxid. Väteperoxid - urea innehåller fast och vattenfri väteperoxid, vilket ger en högre stabilitet och bättre kontrollerbarhet än flytande väteperoxid när den används som oxidationsmedel. Ofta kallad karbamidperoxid på tandläkarmottagningen, den används som en källa till väteperoxid för blekning, desinfektion och oxidation.
Produktion
För framställning av komplexet löses urea i 30 % väteperoxid (molförhållande 2:3) vid temperaturer under 60 °C. vid kylning av denna lösning fälls väteperoxid - urea ut i form av små blodplättar.
Bestämning av väteperoxidhalten genom titrering med kaliumpermanganatlösning ger ett värde på 35,4 % vilket motsvarar 97,8 % av det teoretiska maxvärdet. Den återstående föroreningen består av urea.
I likhet med kristallisationsvatten samkristalliseras väteperoxid med urea med stökiometrin 1:1. Föreningen framställs helt enkelt (i en skala av flera hundra ton per år) genom upplösning av urea i överskott av koncentrerad väteperoxidlösning , följt av kristallisation . Laboratoriesyntesen är analog.
Struktur och egenskaper
Fasttillståndsstrukturen för denna addukt har bestämts genom neutrondiffraktion .
Väteperoxid-urea är ett lätt vattenlösligt, luktfritt, kristallint fast ämne, som finns som vitt pulver eller färglösa nålar eller blodplättar. Vid upplösning i olika lösningsmedel dissocierar 1:1-komplexet tillbaka till urea och väteperoxid. Så precis som väteperoxid är den (felaktigt) så kallade addukten ett oxidationsmedel men frisättningen vid rumstemperatur i närvaro av katalysatorer sker på ett kontrollerat sätt. Således är föreningen lämplig som ett säkert substitut för den instabila vattenhaltiga lösningen av väteperoxid. På grund av tendensen till termisk nedbrytning, som accelererar vid temperaturer över 82 °C, bör den inte värmas över 60 °C, särskilt i ren form.
Lösligheten för kommersiella prover varierar från 0,05 g/ml till mer än 0,6 g/ml.
Ansökningar
Desinfektionsmedel och blekmedel
Väteperoxid - urea används främst som ett desinfektions- och blekmedel i kosmetika och läkemedel. Som ett läkemedel används denna förening i vissa preparat för blekning av tänder . Det används också för att lindra mindre inflammationer i tandkött, munslemhinnor och läppar inklusive kräftsår och tandirritation, och för att emulgera och sprida öronvax .
Karbamidperoxid är också lämplig som desinfektionsmedel, t.ex. för bakteriedämpning på kontaktlinsytor eller som antiseptisk medel för munvatten , örondroppar eller för ytliga sår och sår .
Reagens i organisk syntes
I laboratoriet används den som en mer lätthanterlig ersättning för väteperoxid . Det har visat sig vara ett stabilt, lätthanterligt och effektivt oxidationsmedel som lätt kan kontrolleras genom ett lämpligt val av reaktionsbetingelser. Den levererar oxidationsprodukter på ett miljövänligt sätt och ofta i högt utbyte, särskilt i närvaro av organiska katalysatorer som cis -butendisyraanhydrid eller oorganiska katalysatorer som natriumvolframat .
Den omvandlar tioler selektivt till disulfider, sekundära alkoholer till ketoner, sulfider till sulfoxider och sulfoner, nitriler till amider och N -heterocykler till aminoxider .
Hydroxibensaldehyder omvandlas till dihydroxibensener ( Dakin-reaktion ) [ bättre källa behövs ] och ger, under lämpliga förhållanden, motsvarande bensoesyror.
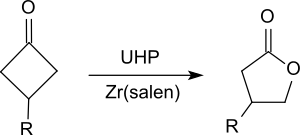
Det oxiderar ketoner till estrar, i synnerhet cykliska ketoner, såsom substituerade cyklohexanoner eller cyklobutanoner för att ge laktoner ( Baeyer-Villiger-oxidation) .
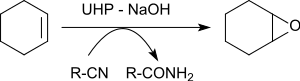
Epoxideringen av olika alkener i närvaro av bensonitril ger oxiraner i utbyte av 79 till 96 %.
Syreatomen som överförs till alkenen härrör från peroxoimidsyran som bildas mellanliggande från bensonitril. Den resulterande imidinsyran tautomeriseras till bensamiden.
Säkerhet
Sammansättningen fungerar som ett starkt oxidationsmedel och kan orsaka hudirritation och allvarliga ögonskador.
Se även
externa länkar
- "Väteperoxidkarbamidaddukt, UHP" . Organisk kemiportal.
- "Karbamidperoxidmonografi" . Drugs.com.