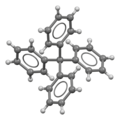
Tetrafenylmetan
|
|
|||
| Namn | |||
|---|---|---|---|
|
Föredraget IUPAC-namn
1,1′,1′′,1′′′-Metanetrayltetrabensen |
|||
| Identifierare | |||
|
3D-modell ( JSmol )
|
|||
| ChemSpider | |||
| ECHA InfoCard | 100.010.132 | ||
| EG-nummer |
|
||
|
PubChem CID
|
|||
| UNII | |||
|
CompTox Dashboard ( EPA )
|
|||
|
|||
|
|||
| Egenskaper | |||
| C25H20 _ _ _ | |||
| Molar massa | 320,44 g/mol | ||
| Smältpunkt | 282 °C (540 °F; 555 K) | ||
| Kokpunkt | 431°C | ||
| Strukturera | |||
| tetragonal | |||
| P 4 2 1 c, nr 114 | |||
| S 4 | |||
|
a = 10,896 Å, c = 7,280 Å
(20 °C)
|
|||
|
Formelenheter ( Z )
|
2 | ||
| Faror | |||
| GHS- märkning : | |||

|
|||
| Fara | |||
| H350 | |||
| P201 , P202 , P281 , P308+P313 , P405 , P501 | |||
|
Om inte annat anges ges data för material i standardtillstånd (vid 25 °C [77 °F], 100 kPa).
|
|||
Tetrafenylmetan är en organisk förening som består av en metankärna med fyra fenylsubstituenter . Det syntetiserades första gången av Moses Gomberg 1898.
Syntes
Gombergs klassiska organiska syntes som visas nedan börjar med att reagera trifenylmetylbromid 1 med fenylhydrazin 2 till hydrazinet 3 . Oxidation med salpetersyra producerar sedan azoföreningen 4 från vilken kvävgas utvecklas vid uppvärmning över smältpunkten med bildning av tetrafenylmetan 5 .
Gomberg kunde särskilja denna förening från trifenylmetan ( elementanalys var inte ett alternativ med tanke på de små skillnaderna i vätefraktionerna på 6,29% och 6,60%) genom nitrering av 5 med salpetersyra till 6 . En stark bas skulle kunna abstrahera metinprotonen i den nitrerade trifenylmetylföreningen om den finns och bilda en starkt färgad förening.
Han fick ytterligare bevis för bildandet av tetrafenylmetan genom att reducera nitrogrupperna till aminogrupper med zinkdamm i ättiksyra till leukofärgämnet 7 , som vid exponering för saltsyra eliminerar anilin till den kända föreningen pararosanilin 8 .
Gombergs framgång med att syntetisera tetraphenylmethane satte honom på försöket att förbereda nästa homolog hexaphenylethane , vilket ledde honom till upptäckten av trifenylmetylradikalen .
Se även
- ^ Robbins, A.; Jeffrey, GA; Chesick, JP; Donohue, J.; Bomull, FA; Frenz, BA; Murillo, CA (1975-10-01). "En förfining av kristallstrukturen hos tetrafenylmetan: tre oberoende ombestämningar" . Acta Crystallographica Avsnitt B: Strukturell kristallografi och kristallkemi . 31 (10): 2395–2399. doi : 10.1107/S0567740875007686 . ISSN 0567-7408 .
- ^ Gomberg, M. (1898). "På tetrafenylmetan" . J. Am. Chem. Soc. 20 (10): 773–780. doi : 10.1021/ja02072a009 .