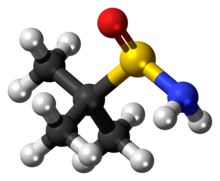
tert -butansulfinamid
|
|||
|
|||
| Namn | |||
|---|---|---|---|
|
Föredraget IUPAC-namn
2-metylpropan-2-sulfinamid |
|||
| Identifierare | |||
|
|||
|
3D-modell ( JSmol )
|
|
||
| ECHA InfoCard | 100.108.188 | ||
|
PubChem CID
|
|||
| UNII |
|
||
|
CompTox Dashboard ( EPA )
|
|||
|
|||
|
|||
| Egenskaper | |||
| (CH3 ) 3CS ( O) NH2 | |||
| Molar massa | 121,20 g/mol | ||
| Utseende | vitt till benvitt kristallint fast ämne | ||
| Smältpunkt | 102 till 105 °C (216 till 221 °F; 375 till 378 K) | ||
|
Om inte annat anges ges data för material i standardtillstånd (vid 25 °C [77 °F], 100 kPa).
|
|||
tert -butansulfinamid (även känd som 2-metyl-2-propansulfinamid eller Ellmans sulfinamid) är en organosvavelförening och en medlem av klassen sulfinamider . Båda enantiomera formerna är kommersiellt tillgängliga och används i asymmetrisk syntes som kirala hjälpämnen , ofta som kirala ammoniakekvivalenter för syntes av aminer . tert -butansulfinamid och den associerade syntetiska metodiken introducerades 1997 av Jonathan A. Ellman et al .
Enantiopen syntes
Enantioren tert -butansulfinamid kan framställas genom enantioselektiv oxidation av billig di- tert -butyldisulfid till tiosulfinatet följt av disulfidbindningsklyvning med litiumamid . I den ursprungliga omfattningen framställdes den kirala liganden som användes tillsammans med vanadylacetylacetonat genom att kondensera en optiskt ren kiral aminoindanol med 3,5-di- tert -butylsalicylaldehyd .
| tert -butansulfinamidsyntes |
|---|
Enantioselektiv aminsyntes
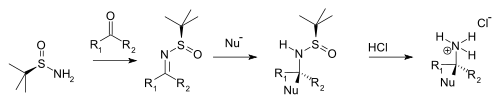
Kondensation med ketoner och aldehyder ger motsvarande N - tert -butansulfinyl aldiminer och ketiminer . Dessa intermediärer är mer resistenta mot hydrolys än andra iminer men mer reaktiva mot nukleofiler . En nukleofil adderas diastereoselektivt över imingruppen i en elektrofil addition med tert -butansulfinylgruppen som fungerar som ett kiralt hjälpmedel. Denna tert -butansulfinylgrupp är också en skyddsgrupp . Vid tillsats av saltsyra avlägsnas tert-butansulfinylgruppen och bildar det kirala primära ammoniumsaltet eller aminen (från aldehydprekursorn) eller den kirala sekundära aminen (ketonprekursorn) .
| tert -butansulfinamid kiral aminsyntes |
|---|
Typiska nukleofiler är Grignard-reagenser , organozinkföreningar , organolitiumföreningar och enolater .
Chirala sulfiniminer som mellanprodukter för den asymmetriska syntesen av aminer har också utvecklats av Franklin A. Davis .
Ansökningar
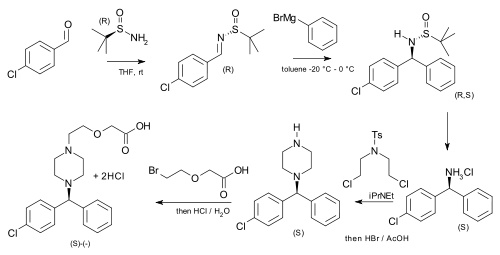
tert -butansulfinamid har använts som ett hjälpmedel i en asymmetrisk syntes av cetirizin (mer potent än den racemiska blandningen av läkemedlet) utgående från p-klorbensaldehyd och fenylmagnesiumbromid , den kan också användas i asymmetrisk syntes av Rivastigmin från 3-Ethoxy- 4-metoxibensaldehyd .
| Asymmetrisk cetirizinsyntes |
|---|