N- sulfinylimin
N -sulfinyliminer ( N -sulfinyliminer , sulfiniminer , tiooxim S -oxider ) är en klass av iminer som bär en sulfinylgrupp bunden till kväve. Dessa iminer uppvisar användbar stereoselektivitetsreaktivitet och på grund av närvaron av den kirala elektronavdragande N -sulfinylgruppen. De tillåter 1,2-addition av organometalliska reagenser till iminer. N - sulfinylgruppen utövar kraftfulla och förutsägbara stereoriktande effekter som resulterar i höga nivåer av asymmetrisk induktion . Racemisering av det nyskapade kol-kväve- stereocentret förhindras eftersom anjoner stabiliseras vid kväve (dvs. sulfinylgruppen är en mångsidig aminskyddsgrupp). Det kirala sulfinylhjälpmedlet avlägsnas lätt genom enkel syrahydrolys . Tillsatsen av organometalliska reagens till N -sulfinyliminer är den mest tillförlitliga och mångsidiga metoden för asymmetrisk syntes av aminderivat . Dessa byggstenar har använts i den asymmetriska syntesen av många biologiskt aktiva föreningar.
Syntes
De första N -sulfinyliminerna i racemisk form bildades genom oxidation av p -toluen-sulfenyliminer med m-CPBA . Enantioren p -toluen-sulfinyl-iminer uppstår genom reaktionen av det kommersiellt tillgängliga Andersen-reagenset (mentyl- p -toluensulfinat) med metallo-ketiminer men är begränsat till keton-härledda N -sulfinyl-iminer. En mer allmän metod för framställning av N -sulfinyliminer är den asymmetriska oxidationen av akirala sulfenyliminer med en kiral oxaziridin . Användbarheten av denna metod begränsas av tillgängligheten av N -sulfonyloxaziridin, som är svår att framställa. Mer praktiskt är förfarandet i en behållare från Andersen-reagenset som gör en mängd olika p -toluen-sulfinyliminer tillgängliga från både aromatiska och alifatiska aldehyder.
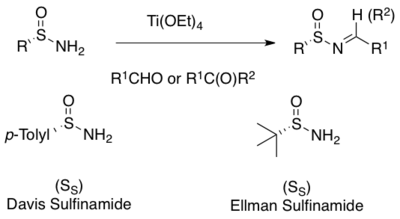
En allmänt använd metod för asymmetrisk syntes av N -sulfinyliminer är kondensationen av enantioren primära sulfinamider med aldehyd eller ketoner. En mild Lewis-syra dehydrerande reagenser som titanetoxid underlättar kondensationen. Många sulfinamider är kommersiellt tillgängliga i både ( R )- och ( S )-former. De två mest använda är Davis p -toluensulfinamid och Ellman tert -butansulfinamid
Ansökningar
p - toluen -sulfinyliminerna har använts för den mycket diastereoselektiva asymmetriska syntesen av α- aminosyror , β-aminosyror, syn- och anti-2,3-diaminoestrar, α-aminoaldehyder och ketoner, β-aminoketoner. a-aminofosfonater, aziridin-2-karboxylater och aziridin-2-fosfonater. Många av dessa transformationer kan utföras med tert-butylsulfinyliminer. För den asymmetriska syntesen av aminer krävs tert-butylsulfinyliminer eftersom litium- och Grignard-reagenser reagerar vid sulfinylsvavel i p -toluen-sulfinyliminer. Mild syrabehandling avlägsnar lätt N -sulfinylgruppen i sulfinamidprodukterna, vilket ger de fria aminderivaten. En fördel med tert-butylsulfinyliminer är att syrabehandling av motsvarande sulfinamider leder till lätt avlägsnande av biprodukter