Spirotryprostatin B

|
|
| Namn | |
|---|---|
|
Föredraget IUPAC-namn
(2S , 3S , 5aS ) -2'-hydroxi-3-(2-metylprop-1-en-1-yl)-5a,6,7,8-tetrahydro- 3H , 5H , 10H -spiro[dipyrrolo[1,2- a :1',2'- d ]pyrazol-2,3'-indol]-5,10-dion |
|
| Identifierare | |
|
3D-modell ( JSmol )
|
|
| ChemSpider | |
|
PubChem CID
|
|
|
|
|
|
| Egenskaper | |
| C21H21N3O3 _ _ _ _ _ _ _ | |
| Molar massa | 363,417 g·mol -1 |
|
Om inte annat anges ges data för material i standardtillstånd (vid 25 °C [77 °F], 100 kPa).
|
|
Spirotryprostatin B är en indolalkaloid som finns i svampen Aspergillus fumigatus som tillhör en klass av naturligt förekommande 2,5- diketopiperaziner . Spirotryprostatin B och flera andra indoliska alkaloider (inklusive Spirotryprostatin A , samt andra tryprostatiner och cyklotryprostatiner) har visat sig ha antimitotiska egenskaper och som sådana har de blivit av stort intresse som läkemedel mot cancer . På grund av detta är den totala syntesen av dessa föreningar en stor strävan av organiska kemister, och ett antal olika synteser har publicerats i den kemiska litteraturen.
Total syntes
Den första totala syntesen utfördes 2000 av Danishefsky-gruppen vid Columbia University , med ett antal andra synteser som följde kort därefter av Williams, Ganesan, Fuji, Carreira, Horne, Overman och nu senast Trost.
Ur en syntetisk synvinkel är de mest utmanande strukturella egenskaperna hos molekylen den C3 spirocykliska ringövergången och det intilliggande prenylsubstituerade kolet. Tillvägagångssätt för att förbereda skelettet av spirotryprostatin B har varierat avsevärt.
Danishefsky spirotryprostatin B-syntes
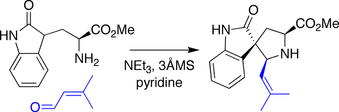
I Danishefsky-syntesen kondenserades en amin härledd från tryptofan med en aldehyd , vilket utlöste en reaktion av Mannich-typ där den vidhängande oxindolen fungerade som en nukleofil mot den intermediära iminiumarten .
Williams spirotryprostatin B-syntes
Syntesen av Williams-gruppen använde en 3-komponent kopplingsreaktion. En sekundär amin kombinerades med en aldehyd för att bilda en intermediär azometin- ylid , som genomgick en 1,3-dipolär cykloaddition med en omättad oxindol som också fanns i reaktionsblandningen.
Ganesan spirotryprostatin B syntes
Ganesan använde sig av en biomimetisk strategi i sin syntes av spirotryprostatin B. En indol behandlades med N -bromsuccinimid för att utlösa en oxidativ omarrangemang, vilket bildade det kvartära stereocentret på ett diastereoselektivt sätt.
Fuji spirotryprostatin B syntes
I syntesen som utvecklats av Fuji-gruppen fastställdes stereokemin vid det spirocykliska kolet genom en nitroolefineringsreaktion. En oxindol med vidhängande prenylgrupp omsattes med en nitroolefin som bär en kiral lämnande grupp .
Carreira spirotryprostatin B syntes
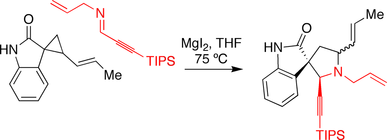
Carreira-gruppen använde sig av en magnesiumjodid-befrämjad annuleringsreaktion i sin strategi mot spirotryprostatin B. En oxindol som bär en cyklopropan reagerades med en imin i närvaro av magnesiumjodiden, vilket utlöste ringexpansionsreaktionen.
Hornspirotryprostatin B-syntes
Hornes syntes av spirotryprostatin B använde också en process av Mannich-typ , där en klorindol fungerade som pronukleofil . Cykliseringen utlöstes genom att behandla den hängande iminen med acylkloriden som härrör från prolin . Den resulterande iminiumarten attackerades av klorindolen och bildade den spirocykliska bindningen.
Overman spirotryprostatin B syntes
Overman-gruppen använde en Heck-reaktion för att förbereda molekylen. En jodanilin med en bunden alken utsattes för palladiumkatalys . Den intermediära palladium-allyl-arten fångades upp av det vidhängande amidkvävet för att generera prenylstereocentret i samma reaktion.
Trost spirotryprostatin B syntes
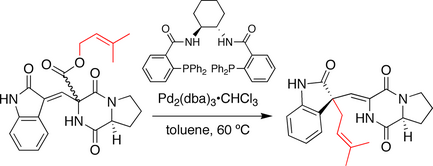
I syntesen som utvecklats av Trost-gruppen etableras stereokemin vid den spirocykliska ringövergången av en dekarboxylerings-prenyleringssekvens, som påminner om Carroll-reaktionen . Här fungerar en prenylester som både nukleofil och elektrofil prekursor. Vid behandling med en kiral palladiumkatalysator joniseras prenylgruppen och dekarboxyleras. Det resulterande jonparet rekombinerar därefter för att generera den prenylerade produkten. Noterbart sker dubbelbindningsmigrering och prenylgruppen attackeras vid oxindolkolet .
- ^ Borthwick AD; et al. (2012). "2,5-Diketopiperaziner: syntes, reaktioner, medicinsk kemi och bioaktiva naturprodukter". Kemiska recensioner . 112 (7): 3641–3716. doi : 10.1021/cr200398y . PMID 22575049 .
- ^ Cui, CB (1996). "Spirotryprostatin B, en ny cellcykelhämmare för däggdjur producerad av Aspergillus fumigatus" . J. Antibiot . 49 (8): 832–835. doi : 10.7164/antibiotika.49.832 . PMID 8823522 .
- ^ von Nussbaum, F; Danishefsky, SJ (2000). "En snabb total syntes av Spirotryprostatin B: Bevis på dess relativa och absoluta stereokemi". Angew. Chem. Int. Ed . 39 (12): 2175–2178. doi : 10.1002/1521-3773(20000616)39:12<2175::AID-ANIE2175>3.0.CO;2-J . PMID 10941053 .
- ^ Sebahar, PR; Williams, RM (2000). "Den asymmetriska totala syntesen av (+)- och (-)-Spirotryprostatin B". J. Am. Chem. Soc . 122 (23): 5666–5667. doi : 10.1021/ja001133n .
- ^ Wang, H; Ganesan, A (2000). "En biomimetisk total syntes av (-)-Spirotryprostatin B och relaterade studier". J. Org. Chem . 65 (15): 4685–4693. doi : 10.1021/jo000306o . PMID 10959875 .
- ^ Bagul, TD; et al. (2002). "Total syntes av spirotryprostatin B via asymmetrisk nitroolefinering" . Org. Lett . 4 (2): 249–251. doi : 10.1021/ol016999s . PMID 11796062 .
- ^ Meyers, C; Carreira, EM (2003). "Total syntes av (−)-Spirotryprostatin B". Angew. Chem. Int. Ed . 42 (6): 694–696. doi : 10.1002/anie.200390192 . PMID 12575009 .
- ^ Miyake, FY; et al. (2004). "Förberedelse och syntetiska tillämpningar av 2-halotryptofanmetylestrar: syntes av spirotryprostatin B". Angew. Chem. Int. Ed . 43 (40): 5357–5360. doi : 10.1002/anie.200460419 . PMID 15468070 .
- ^ Overman, LE; Rosen, MD (2000). "Total syntes av (-)-Spirotryprostatin B och tre stereoisomerer". Angew. Chem. Int. Ed . 39 (24): 4596–4599. doi : 10.1002/1521-3773(20001215)39:24<4596::AID-ANIE4596>3.0.CO;2-F .
- ^ Trost, BM; Stiles, DT (2007). "Total syntes av spirotryprostatin B via diastereoselektiv prenylering". Org. Lett . 9 (15): 2763–2766. doi : 10.1021/ol070971k . PMID 17592853 .