Metylmagnesiumklorid
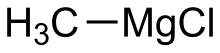
|
|
| Namn | |
|---|---|
|
IUPAC-namn
klorid(metyl)magnesium
|
|
| Andra namn (kloromagnesio)metan
|
|
| Identifierare | |
|
3D-modell ( JSmol )
|
|
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard | 100.010.573 |
| EG-nummer |
|
|
PubChem CID
|
|
| UNII |
|
|
CompTox Dashboard ( EPA )
|
|
|
|
|
|
| Egenskaper | |
| CH3MgCl _ _ | |
| Molar massa | 74,79 g/mol |
| Utseende | färglöst fast material |
| Reagerar med vatten | |
| Löslighet | löslig i dietyleter och THF |
| Faror | |
| Arbetssäkerhet och hälsa (OHS/OSH): | |
|
Huvudsakliga faror
|
Brandfarligt, reagerar med vatten |
| GHS- märkning : | |
 
|
|
| Fara | |
| H225 , H250 , H260 , H314 | |
| P210 , P222 , P223 , P231+P232 , P233 , P240 , P241 , P242 , P243 , P260 , P264 , P280 , P301 +P330+P331 , P33 + P1 , P332 + , P332+ , P332+ 04+ P340 , P305 +P351+ P338 , P310 , P321 , P335+P334 , P363 , P370 +P378 , P402+P404 , P403+P235 , P405 , P422 , P501 | |
| NFPA 704 (branddiamant) | |
| Flampunkt | −17 °C (1 °F; 256 K) |
| Besläktade föreningar | |
|
Besläktade föreningar
|
Fenylmagnesiumbromid , Dibutylmagnesium |
|
Om inte annat anges ges data för material i standardtillstånd (vid 25 °C [77 °F], 100 kPa).
|
|
Metylmagnesiumklorid är en organometallisk förening med den allmänna formeln CH3MgCl . Detta mycket brandfarliga, färglösa och fuktkänsliga material är det enklaste Grignard-reagenset och är kommersiellt tillgängligt, vanligtvis som en lösning i tetrahydrofuran .
Syntes och reaktioner
I förhållande till den vanligare förekommande metylmagnesiumbromiden och metylmagnesiumjodiden erbjuder metylmagnesiumklorid fördelarna med låg ekvivalentvikt och låg kostnad. Den framställs genom reaktion mellan metylklorid och magnesium i etyleter .
Som med de flesta Grignard-reagenser är metylmagnesiumklorid starkt solvatiserat av eterlösningsmedel via koordination från två syreatomer för att ge ett tetraedriskt bundet magnesiumcentrum.
Liksom metyllitium är det den syntetiska motsvarigheten till metylkarbanjonsyntonen . Det reagerar med vatten och andra protiska reagenser för att ge metan, t.ex.
- CH3MgCl + ROH → CH4 + MgCl (OR)
När de behandlas med dioxan reagerar eterlösningar av metylmagnesiumklorid för att ge den olösliga koordinationspolymeren med formeln MgCl2 ( dioxan ) 2 . Kvar i lösningen är dioxanaddukten av dimetylmagnesium . Denna omvandling utnyttjar Schlenk-jämvikten , som drivs till höger av utfällningen av magnesiumhalogeniden:
- 2 CH 3 MgCl + 2 dioxan → (CH 3 ) 2 Mg + MgCl 2 (dioxan) 2
Se även
Vidare läsning
- Sakai, Shogo; Jordan, KD (1982). "Ab initio studie av strukturen och vibrationsfrekvenserna hos Grignard-reagenset metylmagnesiumklorid". Journal of the American Chemical Society . 104 (14): 4019. doi : 10.1021/ja00378a047 .
-
^
Raymond Paul, Olivier Riobé, Michel Maumy (1976). "(E)-4-hexen-1-ol". Org. Synth. 55 : 62. doi : 10.15227/orgsyn.055.0062 .
{{ citera journal }}: CS1 underhåll: använder författarens parameter ( länk ) - ^ ER Coburn (1947). "3-Penten-2-ol". Org. Synth. 27 : 65. doi : 10.15227/orgsyn.027.0065 .
- ^ Fischer, Reinald; Görls, Helmar; Meisinger, Philippe R.; Suxdorf, Regina; Westerhausen, Matthias (2019). "Struktur-löslighetssamband mellan 1,4-dioxankomplex av di(hydrokarbyl)magnesium" . Kemi – En europeisk tidskrift . 25 (55): 12830–12841. doi : 10.1002/chem.201903120 . PMC 7027550 . PMID 31328293 .

