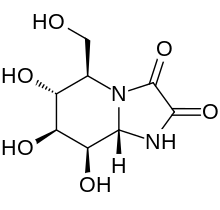
Kifunensine
|
|
| Namn | |
|---|---|
|
Föredraget IUPAC-namn
(5R , 6R , 7S , 8R , 8aS ) -6,7,8-trihydroxi-5-(hydroximetyl)hexahydroimidazo[1,2- a ]pyridin-2,3-dion |
|
| Identifierare | |
|
3D-modell ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard | 100.162.542 |
|
PubChem CID
|
|
| UNII | |
|
CompTox Dashboard ( EPA )
|
|
|
|
|
|
| Egenskaper | |
| C8H12N2O6 _ _ _ _ _ _ _ | |
| Molar massa | 232,192 g·mol -1 |
| Löslig till 50 mM i vatten med försiktig uppvärmning, även om den går långsamt att lösas upp | |
|
Om inte annat anges ges data för material i standardtillstånd (vid 25 °C [77 °F], 100 kPa).
|
|
Kifunensine är en alkaloid som ursprungligen isolerades från Kitasatosporia kifunense , en actinobacterium (tidigare kallad en actinomycete ). Det är en neutral, stabil förening. [ citat behövs ]
Kifunensine är en potent hämmare av mannosidas I -enzymet och används främst i cellodling för att framställa höga mannosglykoproteiner. Inuti en cell förhindrar det endoplasmatiskt retikulum mannosidas I (ERM1) från att trimma mannosrester från prekursorglykoproteiner. Kifunensine visar ingen hämmande verkan mot mannosidas II eller det endoplasmatiska reticulum alfa-mannosidas, och det hämmar svagt arylmannosidas.
När det inkorporeras i cellodlingsmedia har kifunensin inte visat någon signifikant inverkan på celltillväxt eller glykoproteinproduktionsutbytet .
Kifunensine har visat potential för behandling av sarkoglykanopatier och lysosomala lagringsstörningar .
Historia
Kifunensine isolerades först av Iwami et al. 1987, och beskrivs som en ny typ av immunoaktiv substans. Den framställdes ursprungligen genom att odla actinobacterium Kitasatosporia kifunense i ett lämpligt medium vid 25–33 °C under flera dagar, följt av extraktion av alkaloiden.
Strukturen av kifunensine publicerades 1989 av Kayakiri et al.
Enzyminhibering
Kifunensine är en potent hämmare av mannosidas I-enzymet. Det är 50 till 100 gånger mer potent än deoxymannojirimycin – en alkaloid med liknande struktur. Kifunensine hämmar humant endoplasmatiskt retikulum α-1,2-mannosidas I och Golgi klass I mannosidas IA, IB och IC med Ki-värden på 130 respektive 23 nM.
Eftersom den är en neutral molekyl (jfr andra mannosidashämmare som deoxymannojirimycin), kan den tränga in i cellerna. Väl inne i en cell blockerar kifunensine endoplasmatiskt retikulum (ER) mannosidas I (ERM1). Detta blockerar bearbetning av glykoproteiner i ER, för att lämna dem med glykoformer med huvudsakligen nio mannosrester bundna till två N-acetylglukosaminrester (Man9GlcNAc2).
Tillsatsen av 5–20 μM kifunensin till däggdjurscellodlingsmedia är tillräckligt för att uppnå fullständig mannosidas I-hämning.
Kifunensine hämmar inte mannosidas II eller det endoplasmatiska retikulum alfa-mannosidas. Det hämmar svagt arylmannosidas.
Syntes
Kayakiri et al. publicerade en syntes av kifunensin från D-glukos 1990 och en syntes av 8-epi-kifunensine 1991. En syntes av kifunensin och några analoger, från L-askorbinsyra, publicerades av Hering et al. 2005. Kifunensine tillverkas nu av GlycoSyn i en kommersiell process av N-acetylmannosamin i åtta steg via en patenterad process.
Används
Produktion av höga mannosglykoproteiner i cellkultur
Kifunensines hämmande verkan har lett till dess användning vid framställning av högmannosglykoproteiner genom odling av transformerade däggdjursceller. Det är lättare att modifiera glykosyleringen av ett glykoprotein genom att använda en odlingsmedieingrediens med en existerande transformerad cellinje än genom att generera en ny cellinje, speciellt om många cellinjer eller ledningar screenas.
Terapeutiska användningsområden
Kifunensines användning som läkemedel forskas för närvarande i flera tillstånd som drar nytta av dess förmåga att hämma mannosidas I.
Sarkoglykanopatier
Sarkoglykanopatier är autosomala recessiva muskelsjukdomar i gruppen lem-gördel muskeldystrofi (LMGD). Fyra former, LGMD 2C, 2D, 2E och 2F har identifierats, vilka är resultatet av defekter i γ-, α-, β- och δ-sarkoglykangenerna. Det finns färre än 1 500 patienter med sarkoglykanopati i Europeiska unionen .
I cellbaserade analyser och i en djurmodell visade sig kifunensine vara särskilt lämpat för att behandla LGMD 2D (R77C-substitution), som har diagnostiserats hos patienter i Europa , Afrika , Japan och Brasilien .
Kifunensine beviljades särläkemedelsstatus för behandling av var och en av γ-, α-, β- och δ-sarkoglykanopati av European Medicines Agency i oktober 2011.
Ett patent för behandling av sarkoglykanopatier innehas av Genethon. Krav 11 hänför sig till användningen av kifunensin som en inhibitor av den endoplasmatiska retikulumassocierade nedbrytningsvägen (ERAD), speciellt av mannosidas I. Utvecklingen av kifunensin ställdes på is på grund av biverkningar som behöver analyseras ytterligare.
Lysosomala lagringsstörningar
Vid lysosomala lagringsstörningar – Gauchers sjukdom och Tay–Sachs sjukdom – förhindrar endoplasmatisk retikulum-associerad nedbrytning (ERAD) den naturliga veckningen av muterade lysosomala enzymer i en patients fibroblaster .
Kifunensine, givet i mycket låg koncentration (50 nM), hämmar det endoplasmatiska retikulum mannosidas I och stör tidig substratigenkänning, förlängd ER-retention och substratveckning. Det orsakade inte att oåterkalleligt felveckade proteiner ackumulerades eller inducerade apoptos i cellerna. Dessutom resulterade kombinationen av ERAD-hämning med användning av kifunensine med proteostasmodulering (MG-132 = Z-Leu-Leu-Leu-al) för att förbättra den cellulära veckningskapaciteten i en synergistisk räddning av muterade enzymer.
Ett patent som innehas av William Marsh Rice University gör följande påståenden:
- #9: En metod som innefattar administrering till en patient av en terapeutiskt effektiv mängd av minst en hämmare av ER-associerad nedbrytning
- #10: Metoden enligt krav 9, varvid patienten har Gauchers sjukdom eller Tay-Sachs sjukdom
- #11: Förfarande enligt krav 9, varvid inhibitorn är eeyarestatin I eller kifunensine.