Diazald
|
|
| Namn | |
|---|---|
|
Föredraget IUPAC-namn
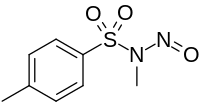
N ,4-dimetyl- N -nitrosobensen-1-sulfonamid |
|
| Andra namn
N -metyl- N -nitroso-4-metylbensensulfonamid; N -metyl- N -nitroso- p -toluensulfonamid; N -metyl- N -nitroso-4-metylbensensulfonamid
|
|
| Identifierare | |
|
3D-modell ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard | 100.001.139 |
| EG-nummer |
|
| Maska | C418734 |
|
PubChem CID
|
|
| UNII | |
|
CompTox Dashboard ( EPA )
|
|
|
|
|
|
| Egenskaper | |
| C8H10N2O3S _ _ _ _ _ _ _ _ | |
| Molar massa | 214,24 g·mol -1 |
| Utseende | Ljusgul fast substans |
| Smältpunkt | 61–62 °C (142–144 °F; 334–335 K) |
| Faror | |
| Arbetssäkerhet och hälsa (OHS/OSH): | |
|
Huvudsakliga faror
|
Hudsensibiliserande, irriterande, explosivt |
| NFPA 704 (branddiamant) | |
| Säkerhetsdatablad (SDS) | Externt MSDS |
|
Om inte annat anges ges data för material i standardtillstånd (vid 25 °C [77 °F], 100 kPa).
|
|
Diazald ( N -metyl - N -nitroso- p -toluensulfonamid ) används som en relativt säker och lätthanterlig prekursor till diazometan , som är giftigt och instabilt. Diazald har blivit den gynnade kommersiellt tillgängliga prekursorn för syntes av diazometan, jämfört med reagenser som N -metyl -N- nitrosourea och N- metyl- N' -nitro- N- nitrosoguanidin , som är mindre termiskt stabila och mer toxiska och mutagena, respektive.
Vid tillsats av en bas som natriumhydroxid eller kaliumhydroxid och mild upphettning ( 65–70 °C) i en blandning av vatten, dietyleter och ett högkokande polärt hjälplösningsmedel (t.ex. dietylenglykolmonometyleter ), nitrososulfonamid genomgår successiva elimineringsreaktioner för att producera diazometan (som samdestilleras som en eterlösning) såväl som ett p -toluensulfonatsalt som en biprodukt, enligt följande mekanism:
Liksom andra nitrosoföreningar är den termiskt känslig, som ett resultat av dess svaga N–NO-bindning vars bindningsdissociationsenergi uppmättes till 33,4 kcal/mol.

