Blastulation
| Blastulation | |
|---|---|
 Blastulation: från 1 . morula till 2 . blastula
| |
| Detaljer | |
| dagar | 4 |
| Föregångare | Morula |
| Ger upphov till | Gastrula |
| Identifierare | |
| Maska | D036703 |
| Anatomisk terminologi | |
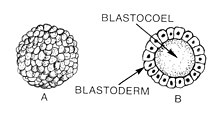
Blastulation är det stadium i tidig embryonal utveckling av djur som producerar blastula . Vid utveckling av däggdjur utvecklas blastula till blastocysten med en differentierad inre cellmassa och en yttre trophectoderm . Blastula (från grekiska βλαστός ( blastos som betyder grodd )) är en ihålig sfär av celler som kallas blastomerer som omger en inre vätskefylld hålighet som kallas blastocoel . Embryonal utveckling börjar med att en spermie befruktar en äggcell för att bli en zygot , som genomgår många klyvningar för att utvecklas till en boll av celler som kallas morula . Först när blastocoel bildas blir det tidiga embryot en blastula. Blastula föregår bildandet av gastrula där embryots groddlager bildas.
Ett gemensamt drag hos en blastula hos ryggradsdjur är att den består av ett lager av blastomerer, känd som blastoderm , som omger blastocoel. Hos däggdjur innehåller blastocysten en embryoblast (eller inre cellmassa) som så småningom kommer att ge upphov till fostrets definitiva strukturer, och en trofoblast som fortsätter att bilda de extra-embryonala vävnaderna.
Under blastulation sker en betydande mängd aktivitet inom det tidiga embryot för att fastställa cellpolaritet , cellspecifikation , axelbildning och för att reglera genuttryck . Hos många djur, såsom Drosophila och Xenopus , är mid blastula transition (MBT) ett avgörande steg i utvecklingen under vilket moderns mRNA bryts ned och kontroll över utvecklingen överförs till embryot. Många av interaktionerna mellan blastomerer är beroende av cadherinuttryck , särskilt E-cadherin hos däggdjur och EP-cadherin hos amfibier .
Studiet av blastula och cellspecifikation har många implikationer inom stamcellsforskning och assisterad reproduktionsteknologi . Hos Xenopus beter sig blastomerer som pluripotenta stamceller som kan migrera längs flera vägar, beroende på cellsignalering . Genom att manipulera cellsignalerna under blastula-stadiet av utvecklingen kan olika vävnader bildas. Denna potential kan vara avgörande för regenerativ medicin för sjukdoms- och skadefall. Provrörsbefruktning innebär överföring av ett embryo till en livmoder för implantation .
Utveckling
Blastulastadiet av tidig embryoutveckling börjar med uppkomsten av blastocoel. Ursprunget till blastocoel i Xenopus har visat sig vara från den första klyvningsfåran , som breddas och förseglas med täta förbindelser för att skapa en kavitet .
Hos många organismer styrs embryots utveckling fram till denna punkt och under den tidiga delen av blastulastadiet av moderns mRNA, så kallat eftersom det producerades i ägget före befruktningen och därför uteslutande kommer från modern.
Midblastula övergång
I många organismer inklusive Xenopus och Drosophila sker midblastula -övergången vanligtvis efter ett visst antal celldelningar för en given art, och definieras av slutet av de synkrona celldelningscyklerna för den tidiga blastulautvecklingen och förlängningen av cellcyklerna genom tillägg av G1- och G2-faserna . Före denna övergång sker klyvning med endast syntes- och mitosfaserna i cellcykeln. Tillägget av de två tillväxtfaserna i cellcykeln gör att cellerna kan öka i storlek, eftersom blastomererna fram till denna punkt genomgår reduktiva delningar där embryots totala storlek inte ökar utan fler celler skapas. Denna övergång börjar tillväxten i organismens storlek.
Mid-blastula-övergången kännetecknas också av en markant ökning av transkriptionen av nytt, icke-modernt mRNA som transkriberats från organismens genom. Stora mängder av moderns mRNA förstörs vid denna tidpunkt, antingen av proteiner såsom SMAUG i Drosophila eller av mikroRNA . Dessa två processer flyttar kontrollen av embryot från moderns mRNA till kärnorna.
Strukturera
En blastula ( blastocyst hos däggdjur ), är en sfär av celler som omger en vätskefylld hålighet som kallas blastocoel . Blastocoel innehåller aminosyror , proteiner , tillväxtfaktorer , sockerarter, joner och andra komponenter som är nödvändiga för cellulär differentiering . Blastocoel tillåter också blastomerer att röra sig under gastrulationsprocessen .
Hos Xenopus embryon består blastula av tre olika regioner. Djurkåpan bildar blastocoelns tak och fortsätter i första hand att bilda ektodermala derivat. Ekvatorial- eller marginalzonen, som utgör väggarna i blastocoel, differentierar sig främst till mesodermal vävnad. Växtmassan är sammansatt av blastocoel-golvet och utvecklas i första hand till endodermal vävnad.
I däggdjursblastocysten finns tre linjer som ger upphov till senare vävnadsutveckling. Epiblasten ger upphov till själva fostret medan trofoblasten utvecklas till en del av moderkakan och den primitiva endodermen blir gulesäcken . I musembryot börjar blastocoelbildningen vid 32-cellsstadiet. Under denna process kommer vatten in i embryot, med hjälp av en osmotisk gradient som är resultatet av natrium-kaliumpumpar som producerar en hög natriumgradient på den basolaterala sidan av trophectoderm. Denna rörelse av vatten underlättas av aquaporiner . En tätning skapas av täta förbindelser mellan epitelcellerna som kantar blastocoel.
Cellulär vidhäftning
Tight junctions är mycket viktiga för embryoutveckling. I blastula är dessa cadherinmedierade cellinteraktioner väsentliga för utvecklingen av epitel som är viktigast för paracellulär transport , upprätthållande av cellpolaritet och skapandet av en permeabilitetstätning för att reglera blastocoelbildning. Dessa tight junctions uppstår efter att polariteten hos epitelceller har fastställts, vilket lägger grunden för vidare utveckling och specifikation. Inuti blastula är inre blastomerer i allmänhet opolära medan epitelceller uppvisar polaritet.
Däggdjursembryon genomgår komprimering runt 8-cellsstadiet där E-cadheriner samt alfa- och beta - cateniner uttrycks. Denna process skapar en boll av embryonala celler som är kapabla att interagera, snarare än en grupp av diffusa och odifferentierade celler. E-cadherin vidhäftning definierar den apiko-basala axeln i det utvecklande embryot och förvandlar embryot från en otydlig boll av celler till en mer polariserad fenotyp som sätter scenen för vidare utveckling till en fullt bildad blastocyst.
Xenopus membranpolaritet etableras med den första cellklyvningen. Amfibie EP-cadherin och XB/U cadherin spelar en liknande roll som E-cadherin hos däggdjur och etablerar blastomerpolaritet och stelnar cell-cell-interaktioner som är avgörande för vidare utveckling.
Kliniska implikationer
Befruktningsteknik
Experiment med implantation i möss visar att hormonell induktion , superovulation och artificiell insemination framgångsrikt producerar preimplantationsmössembryon. Hos mössen inducerades nittio procent av honorna genom mekanisk stimulering att genomgå graviditet och implantera minst ett embryo. Dessa resultat visar sig vara uppmuntrande eftersom de ger en grund för potentiell implantation i andra däggdjursarter, såsom människor.
Stamceller
Blastula-stadiumceller kan bete sig som pluripotenta stamceller hos många arter. Pluripotenta stamceller är utgångspunkten för att producera organspecifika celler som potentiellt kan hjälpa till att reparera och förebygga skador och degeneration. Att kombinera uttrycket av transkriptionsfaktorer och lokalisering av blastulacellerna kan leda till utvecklingen av inducerade funktionella organ och vävnader. Pluripotenta Xenopus- celler kunde, när de användes i en in vivo-strategi, formas till funktionella näthinnor . Genom att transplantera dem till ögonfältet på neurala plattan , och genom att inducera flera felaktiga uttryck av transkriptionsfaktorer, var cellerna engagerade i näthinnan och kunde styra synbaserat beteende i Xenopus .
Se även
Bibliografi
- Forgács, G. & Newman, Stuart A. (2005). "Klyvning och blastulabildning" . Biologisk fysik hos det utvecklande embryot . Cambridge University Press. ISBN 978-0-521-78337-8 .
- Cullen, KE (2009). "embryologi och tidig djurutveckling" . Encyclopedia of life science, volym 2 . Infobas. ISBN 978-0-8160-7008-4 .
- McGeady, Thomas A., red. (2006). "Gastrulation" . Veterinär embryologi . Wiley-Blackwell. ISBN 978-1-4051-1147-8 .