4-toluensulfonylklorid
|
|
|
|
| Namn | |
|---|---|
|
Föredraget IUPAC-namn
4-metylbensen-l-sulfonylklorid |
|
| Andra namn Tosylklorid, p -toluensulfonylklorid, p -TsCl, TsCl
|
|
| Identifierare | |
|
3D-modell ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard | 100.002.441 |
|
PubChem CID
|
|
| UNII | |
|
CompTox Dashboard ( EPA )
|
|
|
|
|
|
| Egenskaper | |
| C7H7ClO2S _ _ _ _ _ _ | |
| Molar massa | 190,65 g/mol |
| Utseende | Vitt fast material |
| Smältpunkt | 65 till 69 °C (149 till 156 °F; 338 till 342 K) |
| Kokpunkt | 134 °C (273 °F; 407 K) vid 10 mmHg |
| Reagerar med vatten | |
| Faror | |
| Arbetssäkerhet och hälsa (OHS/OSH): | |
|
Huvudsakliga faror
|
Frigör HCl vid kontakt med vatten |
| NFPA 704 (branddiamant) | |
| Flampunkt | 128 °C (262 °F; 401 K) |
|
Om inte annat anges ges data för material i standardtillstånd (vid 25 °C [77 °F], 100 kPa).
|
|
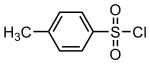
4-toluensulfonylklorid ( p toluensulfonylklorid - , toluen- - ) p sulfonylklorid är en organisk förening med formeln CH3C6H4SO2Cl . Detta vita, illaluktande fasta ämne är ett reagens som används ofta i organisk syntes . Förkortat TsCl eller TosCl , det är ett derivat av toluen och innehåller en funktionell sulfonylkloridgrupp (−SO 2 Cl) .
Används
På ett karakteristiskt sätt omvandlar TsCl alkoholer (förkortat ROH) till motsvarande toluensulfonatestrar, eller tosylderivat ("tosylater"):
- CH 3 C 6 H 4 SO 2 Cl + ROH → CH 3 C 6 H 4 SO 2 ELLER + HCl
Tosylater kan klyvas med litiumaluminiumhydrid:
- 4 CH 3 C 6 H 4 SO 2 ELLER + LiAlH 4 → LiAl(O 3 SC 6 H 4 CH 3 ) 4 + 4 RH
Således tillåter tosylering följt av reduktion avlägsnande av en hydroxylgrupp.
På samma sätt används TsCl för att framställa sulfonamider från aminer:
- CH 3 C 6 H 4 SO 2 Cl + R 2 NH → CH 3 C 6 H 4 SO 2 NR 2 + HCl
De resulterande sulfonamiderna är icke-basiska och, när de härrör från primära aminer, är de till och med sura.
TsCl reagerar med hydrazin för att ge p-toluensulfonylhydrazid .
Framställningen av tosylestrar och amider utförs i närvaro av en bas som absorberar väteklorid. Valet av bas är ofta avgörande för effektiviteten av tosylering. Typiska baser inkluderar pyridin och trietylamin . Ovanliga baser används också; till exempel är katalytiska mängder trimetylammoniumklorid i närvaro av trietylamin mycket effektiva tack vare trimetylaminen .
Andra reaktioner
Eftersom TsCl är ett allmänt tillgängligt reagens har TsCl undersökts mycket ur reaktivitetsperspektivet. Det används vid uttorkning för att göra nitriler , isocyanider och diimider . I en ovanlig reaktion med fokus på svavelcentrum reducerar zink TsCl till sulfinatet, CH 3 C 6 H 4 SO 2 Na.
Tillverkning
Detta reagens är billigt tillgängligt för laboratorieanvändning. Det är en biprodukt från produktionen av orto -toluensulfonylklorid (en prekursor för syntesen av den vanliga livsmedelstillsatsen och katalysatorsackarin ) , via klorsulfonering av toluen :
- CH 3 C 6 H 5 + SO 2 Cl 2 → CH 3 C 6 H 4 SO 2 Cl + HCl
Faror
Tosylklorid anses vara ett giftigt och frätande ämne.
