NAPQI
 | |
| Kliniska data | |
|---|---|
| Andra namn | N -acetyl- p -bensokinonimin; N- acetylimidokinon |
| Identifierare | |
| |
| CAS-nummer | |
| PubChem CID | |
| IUPHAR/BPS | |
| ChemSpider | |
| UNII | |
| ChEBI | |
| ChEMBL | |
| CompTox Dashboard ( EPA ) | |
| ECHA InfoCard | 100.168.312 |
| Kemiska och fysikaliska data | |
| Formel | C 8 H 7 N O 2 |
| Molar massa | 149,149 g·mol -1 |
| 3D-modell ( JSmol ) | |
| |
| |
|
| |
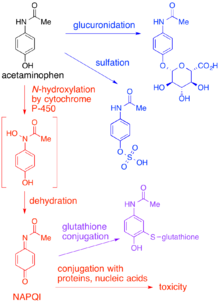
NAPQI , även känd som NAPBQI eller N -acetyl- p -bensokinonimin, är en giftig biprodukt som produceras under den främlingsfientliga metabolismen av det analgetiska paracetamolet (acetaminophen). Det produceras normalt endast i små mängder och avgiftas sedan nästan omedelbart i levern.
Men under vissa förhållanden där NAPQI inte effektivt avgiftas (vanligtvis vid överdos av paracetamol ), orsakar det allvarliga leverskador. Detta blir uppenbart 3–4 dagar efter intag och kan leda till dödsfall från fulminant leversvikt flera dagar efter överdosen.
Ämnesomsättning
Hos vuxna är den primära metaboliska vägen för paracetamol glukuronidering . Detta ger en relativt ogiftig metabolit, som utsöndras i gallan och passerar ut ur kroppen. En liten mängd av läkemedlet metaboliseras via cytokrom P-450 -vägen (för att vara specifik, CYP3A4 och CYP2E1 ) till NAPQI, som är extremt giftigt för levervävnad, samt är ett starkt biokemiskt oxidationsmedel. Hos en genomsnittlig vuxen produceras endast en liten mängd (cirka 10 % av en terapeutisk paracetamoldos) NAPQI, som inaktiveras genom konjugering med glutation (GSH). Mängden NAPQI som produceras skiljer sig i vissa populationer. [ citat behövs ]
Den minsta dos vid vilken paracetamol orsakar toxicitet är vanligtvis 7,5 till 10 g hos en genomsnittlig person. Den dödliga dosen är vanligtvis mellan 10 g och 15 g. [ citat behövs ] Samtidigt alkoholintag sänker dessa trösklar avsevärt. Kroniska alkoholister kan vara mer mottagliga för negativa effekter på grund av minskade glutationnivåer. Andra populationer kan uppleva effekter vid lägre eller högre doser beroende på skillnader i P-450-enzymaktivitet och andra faktorer som påverkar mängden producerad NAPQI. I allmänhet är dock det primära problemet oavsiktlig eller avsiktlig överdosering av paracetamol.
När en giftig dos av paracetamol intas, mättas den normala glukuronidvägen och stora mängder NAPQI produceras. Leverreserver av glutation utarmas genom konjugering med detta överskott av NAPQI. Mekanismen genom vilken toxicitet uppstår är komplex, men tros involvera reaktion mellan okonjugerad NAPQI och kritiska proteiner samt ökad känslighet för oxidativ stress orsakad av utarmningen av glutation.
Förgiftning
Prognosen är god vid överdosering av paracetamol om behandlingen påbörjas upp till 8 timmar efter att läkemedlet har tagits. De flesta sjukhus har motgiften ( acetylcystein ), som fyller på leverns förråd av glutation , vilket gör att NAPQI kan metaboliseras säkert. Utan tidig administrering av motgiftet fulminant leversvikt , ofta i kombination med njursvikt, och döden inträffar vanligtvis inom flera dagar.
Mekanism och motgift
NAPQI blir giftigt när GSH utarmas av en överdos av paracetamol, Glutation är ett viktigt motgift mot överdos. Glutation konjugerar till NAPQI och hjälper till att avgifta det. I denna egenskap skyddar den cellulära proteintiolgrupper, som annars skulle bli kovalent modifierade; när all GSH har förbrukats börjar NAPQI reagera med cellproteinerna och dödar cellerna i processen. Den föredragna behandlingen för en överdos av detta smärtstillande medel är administrering av N -acetyl- L -cystein (antingen via oral eller IV administrering)), som bearbetas av celler till L -cystein och används i de novo- syntesen av GSH.
Se även
externa länkar
- Alsalim W, Fadel M (juli 2003). "Mot evidensbaserad akutmedicin: bästa BET från Manchester Royal Infirmary. Oralt metionin jämfört med intravenöst N-acetylcystein för överdosering av paracetamol" . Emerg Med J . 20 (4): 366–7. doi : 10.1136/emj.20.4.366 . PMC 1726135 . PMID 12835357 .
- van de Straat R, de Vries J, Debets AJ, Vermeulen NP (juli 1987). "Mekanismen för att förhindra paracetamol-inducerad levertoxicitet genom 3,5-dialkylsubstitution. Rollerna av glutationutarmning och oxidativ stress". Biochem. Pharmacol . 36 (13): 2065–70. doi : 10.1016/0006-2952(87)90132-8 . PMID 3606627 .
- Cytokrom P-450 inducerare, inhibitorer och substrat